名校
1 . “侯氏制碱法”曾为全球制碱工业做出了巨大贡献。该工艺反应之一如下:NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl,下列说法正确的是
| A.NH4Cl仅含离子键 | B.电负性:O>N>H |
| C.CO2与SiO2晶体类型相同 | D.氨气的电子式为: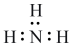 |
您最近一年使用:0次
2022-12-27更新
|
524次组卷
|
5卷引用:河北省部分学校2022-2023学年高三上学期期末考试变式汇编(1-9)
名校
解题方法
2 . 完成下列问题
(1)C、N、Mg、Al、Si、Cu 是常见的六种元素,按要求回答下列问题:
①Cu位于元素周期表第_______ 周期第_______ 族。
②基态C原子核外电子排布式为_______ ;基态N原子核外有_______ 种运动状态的电子。
③基态Si原子核外电子占据的最高能级的电子云轮廓图为_______ 形。
④Mg、Al 两种元素中第一电离能较大的是_______ (填元素符号),原因为_______ 。
(2)几种元素的电负性数据如下表:
①AlF3的熔点_______ AlBr3的熔点(填“大于”、“小于”或“等于”),原因是_______ 。
②根据同一主族元素电负性递变规律,预测碘元素的电负性数值范围为_______ 。
③卤族元素之间可以形成化合物,则氯元素与碘元素形成的化合物ICl中,碘元素的化合价为_______ 。
(1)C、N、Mg、Al、Si、Cu 是常见的六种元素,按要求回答下列问题:
①Cu位于元素周期表第
②基态C原子核外电子排布式为
③基态Si原子核外电子占据的最高能级的电子云轮廓图为
④Mg、Al 两种元素中第一电离能较大的是
(2)几种元素的电负性数据如下表:
| O | F | Al | Br | …… |
| 3.5 | 4.0 | 1.5 | 2.8 | …… |
②根据同一主族元素电负性递变规律,预测碘元素的电负性数值范围为
③卤族元素之间可以形成化合物,则氯元素与碘元素形成的化合物ICl中,碘元素的化合价为
您最近一年使用:0次
3 . W、X、Y、Z、M、Q是原子序数依次增大的前四周期元素,其元素性质或原子结构如下表所示。
(1)W、Z、Q的元素符号分别为_______ 、_______ 、_______ 。
(2)X的基态原子有_______ 种空间运动状态不同的电子,其中能量最高的电子所占据的原子轨道呈_______ 形。
(3)与Y处于同一周期的所有元素中,第一电离能比Y大的元素有_______ 种。
(4)M位于元素周期表的_______ 区, 简化的电子排布式为
简化的电子排布式为_______ 。
(5)Q位于元素周期表的第_______ 周期_______ 族,其价层电子排布图为_______
(6)W、X、Y、Z的电负性由大到小的顺序为_______ (填元素符号)。
| 元素 | 元素性质或原子结构 | ||||||||||||||||||
| W | 电子只有一种自旋取向 | ||||||||||||||||||
| X | 最外层电子排布式为 | ||||||||||||||||||
| Y | 非金属元素,且s能级上的电子总数与p能级上的电子总数相等 | ||||||||||||||||||
| Z |
| ||||||||||||||||||
| M | 前四周期元素中原子核外未成对电子数最多 | ||||||||||||||||||
| Q | 与X同主族 | ||||||||||||||||||
(2)X的基态原子有
(3)与Y处于同一周期的所有元素中,第一电离能比Y大的元素有
(4)M位于元素周期表的
 简化的电子排布式为
简化的电子排布式为(5)Q位于元素周期表的第
(6)W、X、Y、Z的电负性由大到小的顺序为
您最近一年使用:0次
4 . 一种无机纳米晶体材料,仅由铯、铅、溴三种元素构成,在太阳能电池方向有巨大应用前景。回答下列问题:
(1)基态 原子核外电子占据能量最高的能级的电子云轮廓图形状为
原子核外电子占据能量最高的能级的电子云轮廓图形状为_______ 。 属于
属于_______ 区元素。
(2)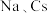 位于同主族,
位于同主族,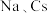 元素的第一电离能分别为
元素的第一电离能分别为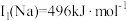 、
、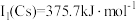 。
。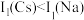 的原因是
的原因是_______ 。
(3) 三种元素的电负性如下表。
三种元素的电负性如下表。 具有较高的熔点(855℃),PbBr2具有较低的熔点(373℃),原因是
具有较高的熔点(855℃),PbBr2具有较低的熔点(373℃),原因是_______ 。
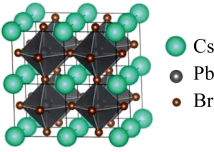
(4)该晶体材料的立方结构如图所示,其化学式为_______ 。若其晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体密度=
,则该晶体密度=_______  。
。
(5)该晶体材料电池并未实现商业化,原因在于自身的不稳定性。
①该晶体材料在潮湿环境中易从固体变成溶液(发生相变),导致器件效率降低,其原因是_______ 。
②某大学采用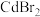 对该材料进行钝化处理可有效提高其稳定性,钝化机理如图所示。根据晶格应变驰豫,
对该材料进行钝化处理可有效提高其稳定性,钝化机理如图所示。根据晶格应变驰豫,_______ (离子)脱离晶格,用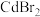 钝化后的晶体比原晶体材料更稳定,其原因是
钝化后的晶体比原晶体材料更稳定,其原因是_______ 。
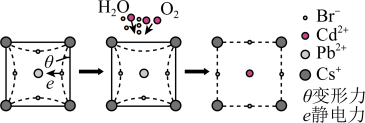
(已知:应力与应变相伴而生,从原子尺度上来理解,应力为单位晶格上的作用力,应变即为晶格的拉伸或收缩,对应于拉伸应变和压缩应变。对应出现的驰豫是指一个宏观平衡系统由于受到外界的作用变为非平衡状态,再从非平衡状态过渡到新的平衡态的过程。)
(1)基态
 原子核外电子占据能量最高的能级的电子云轮廓图形状为
原子核外电子占据能量最高的能级的电子云轮廓图形状为 属于
属于(2)
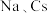 位于同主族,
位于同主族,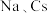 元素的第一电离能分别为
元素的第一电离能分别为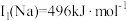 、
、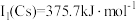 。
。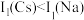 的原因是
的原因是(3)
 三种元素的电负性如下表。
三种元素的电负性如下表。 具有较高的熔点(855℃),PbBr2具有较低的熔点(373℃),原因是
具有较高的熔点(855℃),PbBr2具有较低的熔点(373℃),原因是| 电负性 | ||
| F | Br | Pb |
| 4.0 | 2.8 | 1.9 |
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体密度=
,则该晶体密度= 。
。
(5)该晶体材料电池并未实现商业化,原因在于自身的不稳定性。
①该晶体材料在潮湿环境中易从固体变成溶液(发生相变),导致器件效率降低,其原因是
②某大学采用
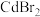 对该材料进行钝化处理可有效提高其稳定性,钝化机理如图所示。根据晶格应变驰豫,
对该材料进行钝化处理可有效提高其稳定性,钝化机理如图所示。根据晶格应变驰豫,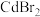 钝化后的晶体比原晶体材料更稳定,其原因是
钝化后的晶体比原晶体材料更稳定,其原因是
(已知:应力与应变相伴而生,从原子尺度上来理解,应力为单位晶格上的作用力,应变即为晶格的拉伸或收缩,对应于拉伸应变和压缩应变。对应出现的驰豫是指一个宏观平衡系统由于受到外界的作用变为非平衡状态,再从非平衡状态过渡到新的平衡态的过程。)
您最近一年使用:0次
名校
5 . F、Cl、Br元素的某种性质Y随核电荷数的变化趋势如图所示,则坐标轴Y不可以代表的是
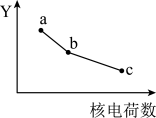

| A.元素的电负性 | B.元素的第一电离能 |
| C.氢化物的稳定性 | D.简单离子的还原性 |
您最近一年使用:0次
解题方法
6 . 我国科学家及其合作团队研究发现,六方相(hep)Fe—H、Fe—C和Fe—O合金在地球内核温压下转变成超离子态。该研究表明地球内核并非传统认知的固态,而是由固态铁和流动的轻元素组成的超离子态。请用所学知识回答下列问题:
(1)基态铁原子最外层电子所在能级的电子云轮廓图为_______ 形。
(2)H、C、O三种元素的电负性由大到小的排序为_______ (填元素符号)。
(3)锰和铁处于同一周期,锰、铁电离能数据如表所示:
请解释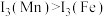 的主要原因:
的主要原因:_______ 。
(4)H、C、O三种元素可以组成很多种物质。
① 、
、 、
、 、
、 、
、 中属于非极性分子的有
中属于非极性分子的有_______ (填化学式)。
②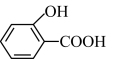 的沸点
的沸点_______ (填“大于”、“小于”或“等于”)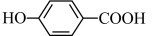 的沸点。
的沸点。
(5)用X射线衍射仪测定发现铁晶体有两种晶胞结构,如图1、图2所示。
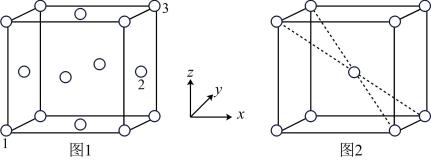
①原子坐标参数可以描述晶胞内部各微粒的相对位置。设图1中1号原子的坐标参数为(0,0,0),3号原子的坐标参数为(1,1,1),则2号原子的坐标参数为_______ 。
②若图2中晶胞参数为apm,则该晶胞的空间利用率(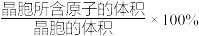 )为
)为_______ (用含π的式子表示)%。
(1)基态铁原子最外层电子所在能级的电子云轮廓图为
(2)H、C、O三种元素的电负性由大到小的排序为
(3)锰和铁处于同一周期,锰、铁电离能数据如表所示:
| 元素 | 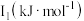 |  | 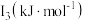 |
| Mn | 717.3 | 1509.9 | 3248 |
| Fe | 762.5 | 1561.9 | 2953 |
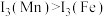 的主要原因:
的主要原因:(4)H、C、O三种元素可以组成很多种物质。
①
 、
、 、
、 、
、 、
、 中属于非极性分子的有
中属于非极性分子的有②
 的沸点
的沸点 的沸点。
的沸点。(5)用X射线衍射仪测定发现铁晶体有两种晶胞结构,如图1、图2所示。

①原子坐标参数可以描述晶胞内部各微粒的相对位置。设图1中1号原子的坐标参数为(0,0,0),3号原子的坐标参数为(1,1,1),则2号原子的坐标参数为
②若图2中晶胞参数为apm,则该晶胞的空间利用率(
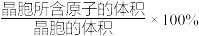 )为
)为
您最近一年使用:0次
2022-07-06更新
|
243次组卷
|
2卷引用:河北省邢台市2021-2022学年高二下学期期末考试化学试题
7 . 某课题组借用足球烯核心成功实现了高效且选择性可精准定制的离子跨膜运输。示意图如图所示。
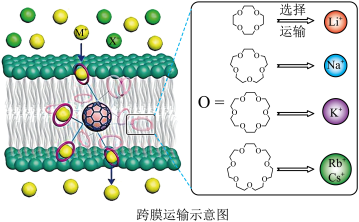
已知:图中有机物称为冠醚,含C、H、O三种元素。
请回答下列问题:
(1)基态Rb原子的价层电子排布式为____________ 。基态K原子核外有_____ 种空间运动状态不同的电子,含钾元素的物质在灼烧时火焰呈________ 色。
(2)冠醚中所含非金属元素的电负性由小到大的顺序是____________ 。
(3)几种冠醚与识别的碱金属离子如表所示。
冠醚识别碱金属离子的必要条件是______________________ 。 Li+、Na+、K+、Rb+、Cs+的离子半径依次增大的原因是___________________________________ 。
(4)足球烯如图1所示。足球烯为_______ (填晶体类型)晶体。
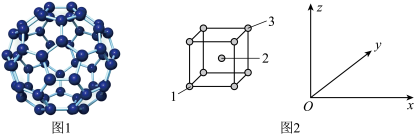
(5)铷晶胞为体心立方堆积,如图2所示,晶胞参数为a nm,设1号原子坐标参数为(0,0,0) 、3号原子坐标参数为(1,1,1)。
①2号原子坐标参数为___________ 。
②设NA为阿伏加德罗常数的值,则该晶胞的密度为____________ g· cm-3。

已知:图中有机物称为冠醚,含C、H、O三种元素。
请回答下列问题:
(1)基态Rb原子的价层电子排布式为
(2)冠醚中所含非金属元素的电负性由小到大的顺序是
(3)几种冠醚与识别的碱金属离子如表所示。
| 冠醚 | 冠醚空腔直径/pm | 适合的粒子(直径/pm) |
| 12-冠(醚)-4 | 120~150 | Li+ (152) |
| 15-冠(醚)-5 | 170~ 220 | Na+ (204) |
| 18-冠(醚)-6 | 260~320 | K+ (276) |
| 21-冠(醚)-7 | 340~430 | Rb+ (304) |
| 21-冠(醚)-7 | 340~430 | Cs+ (334) |
冠醚识别碱金属离子的必要条件是
(4)足球烯如图1所示。足球烯为

(5)铷晶胞为体心立方堆积,如图2所示,晶胞参数为a nm,设1号原子坐标参数为(0,0,0) 、3号原子坐标参数为(1,1,1)。
①2号原子坐标参数为
②设NA为阿伏加德罗常数的值,则该晶胞的密度为
您最近一年使用:0次
解题方法
8 . 核酸检测样品盛放在含有胍盐的标本保存液中,胍盐可以灭活病毒,有效保存多种病毒核酸。胍的结构简式如图,分子构型为平面型,有关说法正确的是
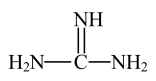
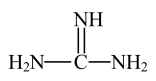
A.胍是含氮有机物,所含元素的电负性大小顺序为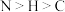 |
| B.胍分子中C原子和3个N原子的杂化方式相同 |
C.晶体易吸收空气中 生成碳酸盐 生成碳酸盐 |
| D.胍分子中两个单键N原子与C原子形成的N−C−N键角大于120° |
您最近一年使用:0次
名校
解题方法
9 . 我国科研人员发现了一种新型超导体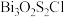 ,由
,由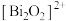 和
和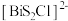 交替堆叠构成。已知
交替堆叠构成。已知 位于第六周期VA族,下列有关说法错误的是
位于第六周期VA族,下列有关说法错误的是
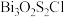 ,由
,由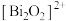 和
和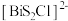 交替堆叠构成。已知
交替堆叠构成。已知 位于第六周期VA族,下列有关说法错误的是
位于第六周期VA族,下列有关说法错误的是A. 的价电子排布式为 的价电子排布式为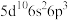 |
B.有关元素的电负性: |
C.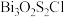 属于含共价键的离子化合物 属于含共价键的离子化合物 |
| D.该新型超导体的组成元素全部位于元素周期表p区 |
您最近一年使用:0次
2020-05-12更新
|
839次组卷
|
17卷引用:河北省石家庄市第二十三中学2021-2022学年高二下学期期中考试化学试题
河北省石家庄市第二十三中学2021-2022学年高二下学期期中考试化学试题山东省青岛市2020届高三4月统一质量检测(一模)化学试题山东省烟台市中英文学校2021届高三上学期期末考试化学试题福建省泉州实验中学2021届高三3月测试(二)化学试题(已下线)2021年高考化学押题预测卷(湖北卷)03(含考试版、答题卡、参考答案、全解全析)山东省潍坊第四中学2022届高三上学期第一次过程检测化学试题专题1~2 综合检测(提升卷)第二节综合拔高练山西省临汾市尧都区山西师范大学实验中学2021-2022学年高二下学期第一次月考化学考试试题山东省青岛市即墨区第一中学2022-2023学年高三上学期10月月考化学试题山东省济宁市育才中学2022-2023学年高二上学期第二次学情检测化学试题广东省深圳市盐田高级中学2021-2022学年高二下学期4月考试化学试题广东省潮阳一中、宝安中学等七校联考2022-2023学年高三上学期第二次(11月)联考化学试题吉林省松原市前郭尔罗斯蒙古族自治县第五高级中学(前郭五中)2023-2024学年高三上学期第三次考试 化学试卷 河南省郑州市宇华实验学校2023-2024学年高三上学期1月期末化学试题新疆维吾尔自治区阿克苏地区第二中学2023-2024学年高二下学期第一次月考化学试卷河南省郑州市宇华实验学校2023-2024学年高二下学期5月月考化学试题
名校
解题方法
10 . 硫氰酸甲基铵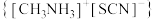 用于抗生素的分离、分析农药含量、硫氰酸络盐的合成以及用作聚合催化剂。通过气相辅助生长技术,利用硫氰酸甲基铵可制得钙钛矿型甲脒铅碘(
用于抗生素的分离、分析农药含量、硫氰酸络盐的合成以及用作聚合催化剂。通过气相辅助生长技术,利用硫氰酸甲基铵可制得钙钛矿型甲脒铅碘(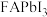 )和一种新型光电材料铯铜卤化物
)和一种新型光电材料铯铜卤化物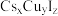 。请回答下列问题:
。请回答下列问题:
(1)基态Cu原子的电子排布式为_______ 。基态I原子的价电子排布图为_______ 。
(2)硫氰酸甲基铵所含元素中第一电离能最大的是_______ (填元素符号)。
(3)Cs、Cu、I的电负性由大到小的顺序是_______ 。
(4)甲脒( )与丙烷的相对分子质量相同,但甲脒的熔点比丙烷的熔点高得多,其原因是
)与丙烷的相对分子质量相同,但甲脒的熔点比丙烷的熔点高得多,其原因是_______ 。甲脒中碳原子的杂化方式为_______ 。
(5)水中铅的测定方法是用双硫腙与铅反应生成红色双硫腙铅络合物(结构如图)。_______ 。
②该络合物分子内不存在的微粒间作用力有_______ (填标号)。
a. 键 b.
键 b. 键 c.非极性键 d.离子键 e.配位键
键 c.非极性键 d.离子键 e.配位键
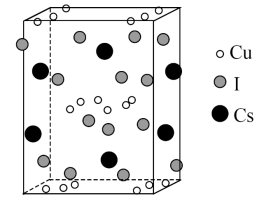
(6)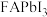 的晶体结构单元如图所示,图中X表示FA,Y表示Pb,位于八面体中心,则X的碘配位数为
的晶体结构单元如图所示,图中X表示FA,Y表示Pb,位于八面体中心,则X的碘配位数为_______ 。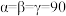 °,晶胞的棱上有8个Cu原子,面上有8个Cu原子、4个Cs原子和4个I原子,其余原子均位于体内,该晶体的密度为
°,晶胞的棱上有8个Cu原子,面上有8个Cu原子、4个Cs原子和4个I原子,其余原子均位于体内,该晶体的密度为_______  。
。
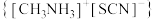 用于抗生素的分离、分析农药含量、硫氰酸络盐的合成以及用作聚合催化剂。通过气相辅助生长技术,利用硫氰酸甲基铵可制得钙钛矿型甲脒铅碘(
用于抗生素的分离、分析农药含量、硫氰酸络盐的合成以及用作聚合催化剂。通过气相辅助生长技术,利用硫氰酸甲基铵可制得钙钛矿型甲脒铅碘(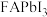 )和一种新型光电材料铯铜卤化物
)和一种新型光电材料铯铜卤化物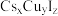 。请回答下列问题:
。请回答下列问题:(1)基态Cu原子的电子排布式为
(2)硫氰酸甲基铵所含元素中第一电离能最大的是
(3)Cs、Cu、I的电负性由大到小的顺序是
(4)甲脒(
 )与丙烷的相对分子质量相同,但甲脒的熔点比丙烷的熔点高得多,其原因是
)与丙烷的相对分子质量相同,但甲脒的熔点比丙烷的熔点高得多,其原因是(5)水中铅的测定方法是用双硫腙与铅反应生成红色双硫腙铅络合物(结构如图)。
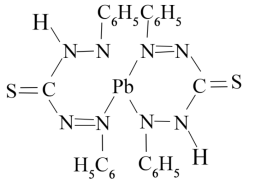
②该络合物分子内不存在的微粒间作用力有
a.
 键 b.
键 b. 键 c.非极性键 d.离子键 e.配位键
键 c.非极性键 d.离子键 e.配位键(6)
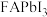 的晶体结构单元如图所示,图中X表示FA,Y表示Pb,位于八面体中心,则X的碘配位数为
的晶体结构单元如图所示,图中X表示FA,Y表示Pb,位于八面体中心,则X的碘配位数为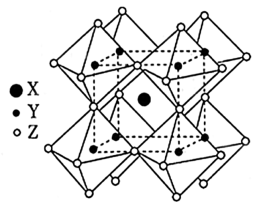
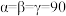 °,晶胞的棱上有8个Cu原子,面上有8个Cu原子、4个Cs原子和4个I原子,其余原子均位于体内,该晶体的密度为
°,晶胞的棱上有8个Cu原子,面上有8个Cu原子、4个Cs原子和4个I原子,其余原子均位于体内,该晶体的密度为 。
。
您最近一年使用:0次
2022-03-08更新
|
420次组卷
|
3卷引用:河北省部分名校2021-2022学年高三下学期3月份联考考试化学试题