名校
解题方法
1 . 下列是元素周期表中的部分元素,请回答下列有关问题:
(1)①元素的价层电子排布式___________ ,⑦元素基态原子的价层电子轨道表示式为___________ 。
(2)上述表中的元素中,电负性最小的元素是___________ (填元素符号,下同),第三周期第一电离能最大的元素是___________ 。
(3)上述表中元素的最高价氧化物对应的水化物中,酸性最强的是___________ (填化学式,下同),碱性最强的是___________ 。
| 周期 | 族 | |||||||
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ | |||||
(2)上述表中的元素中,电负性最小的元素是
(3)上述表中元素的最高价氧化物对应的水化物中,酸性最强的是
您最近一年使用:0次
名校
2 . 下列说法正确的是( )
| A.元素原子的最外层电子数等于元素的最高正化合价 |
| B.多电子原子中,在离核较近的区域内运动的电子能量较高 |
| C.S、Cl的电负性和单质的氧化性均依次增强 |
| D.元素周期表中位于金属元素和非金属元素分界线附近的元素属于过渡元素 |
您最近一年使用:0次
2020-03-26更新
|
93次组卷
|
4卷引用:河北省正定中学2019-2020学年高二3月线上月考化学试题
名校
3 . 由于钒的化合物颜色鲜艳而多彩,因此以神话中斯堪的纳维亚女神“Vanadis"的名字命名。钒有多种化合价,如:+2、+3、+4、+5等,其化合物具有广泛的用途。请回答下列问题:
(1)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ ,表示,与之相反的用 -
,表示,与之相反的用 - 表示,称为电子的自旋磁量子数,则基态V3+核外电子的自旋磁量子数之和为
表示,称为电子的自旋磁量子数,则基态V3+核外电子的自旋磁量子数之和为___________ 。
(2)钒的一种配合物的结构简式为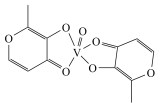 ,该配合物的组成元素的电负性由大到小的顺序是
,该配合物的组成元素的电负性由大到小的顺序是_______ (用元素符号表示),氧原子的杂化轨道类型为__________ ,该配合物分子中含有的化学键类型有________ (填标号)。
A.离子键 B.极性键 C.非极性键 D.配位键
(3)钒的含氧酸有正钒酸(H3VO4)、偏钒酸(HVO3)等,正钒酸、偏钒酸的酸性由强到弱的顺序是_____________ (用分子式表示),原因为________ 。
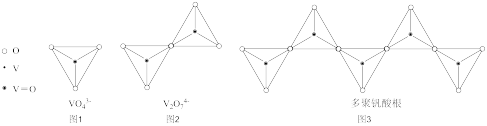
(4)钒的多种含氧酸根离子的结构如图所示,图3为一种无限长单链结构的多聚钒酸根,其化学式为__ 。
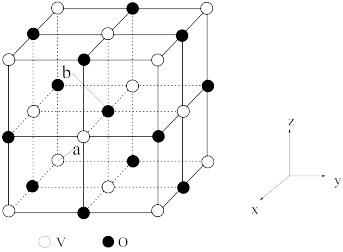
(5)钒的某种氧化物的立方晶胞如图所示,该氧化物的化学式为________________________ ;以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,若a点原子的分数坐标为(0,0,0),则b点原子的分数坐标为____________________ ;钒原子构成的八面体空隙与氧原子构成的八 面体空隙的数量比为_________________________ ;已知该氧化物晶体的密度为ρg·cm-3。则晶胞中距离最近的两个氧原子的核间距为_________________ pm(用NA表示阿伏加德罗常数的值,列出计算式即可)。
(1)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 ,表示,与之相反的用 -
,表示,与之相反的用 - 表示,称为电子的自旋磁量子数,则基态V3+核外电子的自旋磁量子数之和为
表示,称为电子的自旋磁量子数,则基态V3+核外电子的自旋磁量子数之和为(2)钒的一种配合物的结构简式为
 ,该配合物的组成元素的电负性由大到小的顺序是
,该配合物的组成元素的电负性由大到小的顺序是A.离子键 B.极性键 C.非极性键 D.配位键
(3)钒的含氧酸有正钒酸(H3VO4)、偏钒酸(HVO3)等,正钒酸、偏钒酸的酸性由强到弱的顺序是
(4)钒的多种含氧酸根离子的结构如图所示,图3为一种无限长单链结构的多聚钒酸根,其化学式为

(5)钒的某种氧化物的立方晶胞如图所示,该氧化物的化学式为

您最近一年使用:0次
解题方法
4 . 我国秦俑彩绘和汉代器物上用的颜料被称为中国蓝”、“中国紫”,近年来,人们对这些颜料的成分进行了研究,发现其成分主要为BaCuSi4O10、BaCuSi2O6
(1)基态Cu原子核外有_______ 个运动状态不同的电子,其在周期表中的位置_______ 。Si、O、Ba元素电负性由大到小的顺序为_______ 。
(2)“中国蓝”的发色中心是以Cu2+为中心离子的配合物,其中提供孤电子对的是_______ 元素。
(3)比较Si、SiC、 CO2 三种物质晶体状态时熔点由高到低的顺序为_______ ,原因为_______ 。
(4)C、N元素与颜料中的氧元素同周期。
①写出CO的一种常见等电子体分子的电子式_______ ;NO 的VSEPR模型为
的VSEPR模型为_______ ,酸性:HNO2_______ HNO3(填“强于”或“弱于”)。
②C、N元素能形成一种类石墨的聚合物半导体g-C3N4其单层平面结构如图1,晶胞结构如图2。
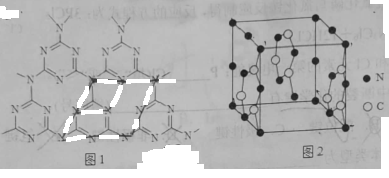
i.g-C3N4中氮原子的杂化类型是_______ 。
ii.已知该晶胞的体积为Vcm3,中间层原子均在晶胞内部。设阿伏加德罗常数的值为NA,则g-C3N4的密度为_______ 。
iii.根据图2,在图1中用平行四边形画出个最小重复单元_____ 。
(1)基态Cu原子核外有
(2)“中国蓝”的发色中心是以Cu2+为中心离子的配合物,其中提供孤电子对的是
(3)比较Si、SiC、 CO2 三种物质晶体状态时熔点由高到低的顺序为
(4)C、N元素与颜料中的氧元素同周期。
①写出CO的一种常见等电子体分子的电子式
 的VSEPR模型为
的VSEPR模型为②C、N元素能形成一种类石墨的聚合物半导体g-C3N4其单层平面结构如图1,晶胞结构如图2。

i.g-C3N4中氮原子的杂化类型是
ii.已知该晶胞的体积为Vcm3,中间层原子均在晶胞内部。设阿伏加德罗常数的值为NA,则g-C3N4的密度为
iii.根据图2,在图1中用平行四边形画出个最小重复单元
您最近一年使用:0次
名校
解题方法
5 . 已知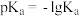 ,如图下表是几种不同有机酸的
,如图下表是几种不同有机酸的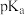 大小,由此产生的推测正确的是
大小,由此产生的推测正确的是
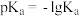 ,如图下表是几种不同有机酸的
,如图下表是几种不同有机酸的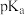 大小,由此产生的推测正确的是
大小,由此产生的推测正确的是| 有机酸 |  |  | 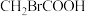 | 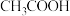 |
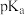 | 2.66 | 2.86 | 2.9 | 4.74 |
A.对键合电子吸引力: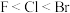 | B.酸性: |
C. | D.碱性: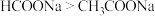 |
您最近一年使用:0次
2024-02-19更新
|
187次组卷
|
3卷引用:河北正定中学本部2023-2024学年高二上学期期末考试化学试题



