1 . 钾、氟及锌的相关化合物用途非常广泛。回答下列问题:
(1)基态锌原子的价电子排布式为___________ ;K、F、Zn的电负性从大到小的顺序为___________ 。
(2)Zn与Ca位于同一周期且最外层电子数相等,钙的熔点与沸点均比锌高,其原因是_______________ 。
(3)OF2分子的几何构型为___________ ,中心原子的杂化类型为___________ 。
(4)KOH 与O3反应可得到KO3(臭氧化钾),KO3 中除σ键外,还存在___________ ;与O3-互为等电子体的分子为___________ (任 写一种 )。
(5)K、F、Zn组成的一种晶体结构如图所示,其晶胞参数为a=0.4058 nm。
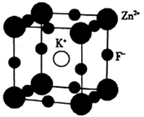
①晶胞中Zn2+的配位数为___________ 个。
②晶胞中紧邻的两个F-间的距离为_______________________ (列出算式即可)nm。
③该晶体的密度为___________ (列出算式即可,用NA表示阿伏伽德罗常数的数值)g·cm-3。
(1)基态锌原子的价电子排布式为
(2)Zn与Ca位于同一周期且最外层电子数相等,钙的熔点与沸点均比锌高,其原因是
(3)OF2分子的几何构型为
(4)KOH 与O3反应可得到KO3(臭氧化钾),KO3 中除σ键外,还存在
(5)K、F、Zn组成的一种晶体结构如图所示,其晶胞参数为a=0.4058 nm。

①晶胞中Zn2+的配位数为
②晶胞中紧邻的两个F-间的距离为
③该晶体的密度为
您最近一年使用:0次
2018-01-07更新
|
409次组卷
|
6卷引用:陕西省榆林市2018届高三第二次模拟考试理综化学试题
2 . [2016·新课标I]锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar]_______________ ,有__________ 个未成对电子。
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是______________________________ 。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因______________________________ 。
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是______________________________ 。
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______________ ,微粒之间存在的作用力是_______________ 。
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为_______________ 。_____ g·cm−3(列出计算式即可)。
(1)基态Ge原子的核外电子排布式为[Ar]
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | −49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为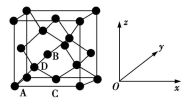
您最近一年使用:0次
2016-12-09更新
|
7035次组卷
|
32卷引用:陕西省汉中市2022届高三下学期第五次校级联考理科综合化学试题
陕西省汉中市2022届高三下学期第五次校级联考理科综合化学试题湖南省衡阳市2020年高中毕业班教学质量监测卷理科综合化学云南省陆良县2019届高三毕业班第二次教学质量摸底考化学试题陕西省武功县2021-2022学年高三上学期第二次质量检测理科综合化学试题 2016年全国普通高等学校招生统一考试化学(新课标1卷精编版)2015-2016学年云南省德宏州芒一中高二下学期期末化学试卷河南省郑州市八校2016-2017学年高二下学期期中联考化学试题2017届山东省潍坊市实验中学高三下学期第四次单元过关测试理科综合化学试卷云南民族大学附属中学2017-2018学年高二下学期第一次月考化学试题(已下线)《考前20天终极攻略》5月30日 物质结构与性质(已下线)解密21 物质的结构与性质(教师版)——备战2018年高考化学之高频考点解密云南省澄江县第一中学2019届高三9月月考理科综合化学试题云南省玉溪市峨山一中2019届高三9月上学期月考化学试题云南省玉溪市新平县第一中学2019届高三第一次月考理综化学试题云南省新平一中2019届高三上学期12月考试化学试题2016年全国普通高等学校招生统一考试化学(全国1卷参考版)广东省深圳外国语学校2019届高三第一次月考理综化学试题鲁科版高中化学选修3模块综合测评卷新疆乌鲁木齐县柴窝堡林场中学2019届高三四月调研考试理综化学试题百所名校联考-物质结构与性质云南省玉溪市江川二中2019-2020学年高三上学期期中考试化学试题贵州省三都水族自治县高级中学2019-2020学年高三上学期期末考试理综化学试题贵州省剑河县第二中学2019-2020学年高三上学期期末考试化学试题宁夏石嘴山市第三中学2019-2020学年高二下学期期中考试化学试题宁夏海原县第一中学2019-2020学年高二下学期第一次月考化学试题吉林省松原市前郭尔罗斯蒙古族自治县第五中学2021届高三下学期5月月考化学试题广东省深圳市罗湖区2022届高三上学期第一次质量检测化学试题贵州省威宁县第八中学2021-2022学年高三上学期第一次月考化学试题云南省曲靖市宣威市第七中学2021-2022学年高三下学期3月考试化学试题湖南省岳阳市汨罗市第二中学2022届高三下学期期中考试化学试题山东省德州市2021-2022学年高二下学期物质结构与性质模块综合测评化学试题山东省青岛一中2023-2024学年高二下学期第二次月考化学试卷
2013·陕西延安·一模
名校
解题方法
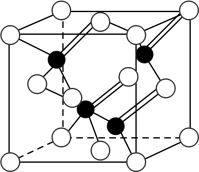
3 . 2010年上海世博会场馆,大量的照明材料或屏幕都使用了发光二极管(LED)。目前市售LED品片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、lnGaN(氮化铟镓)为主。已知镓是铝同族下一周期的元素。砷化镓的晶胞结构如图。试回答:
(1)镓的基态原子的电子排布式是_________________ 。
(2)砷化镓晶胞中所包含的砷原子(白色球)个数为___________ ,与同一个镓原子相连的砷原子构成的空间构型为______________ 。
(3)N、P、As处于同一主族,其氢化物沸点由高到低的顺序是________ 。 (用氢化物分子式表示)
(4)砷化镓可由(CH3)3Ga和AsH3在700℃时制得。(CH3)3Ga中镓原子的杂化方式为___________ 。
(5)比较二者的第一电离能:As______ Ga(填“<”、“>”或“=”)。
(6)下列说法正确的是_____________(填字母)。

(1)镓的基态原子的电子排布式是
(2)砷化镓晶胞中所包含的砷原子(白色球)个数为
(3)N、P、As处于同一主族,其氢化物沸点由高到低的顺序是
(4)砷化镓可由(CH3)3Ga和AsH3在700℃时制得。(CH3)3Ga中镓原子的杂化方式为
(5)比较二者的第一电离能:As
(6)下列说法正确的是_____________(填字母)。
| A.砷化镓晶胞结构与NaCl相同 | B.GaP与GaAs互为等电子体 |
| C.电负性:As>Ga | D.砷化镓晶体中含有配位键 |
您最近一年使用:0次
2016-12-09更新
|
996次组卷
|
3卷引用:2013届陕西省延安市秋高考模拟理综化学试卷
(已下线)2013届陕西省延安市秋高考模拟理综化学试卷2016-2017学年高中化学选修3(人教版)第三章 晶体结构与性质 章末检测新疆乌鲁木齐市第四中学2021-2022学年高二下学期期末考试化学试题
2012·陕西·一模
4 . C、Si、S和N元素在化学中占有极其重要的地位。
(1)写出Si的基态原子价电子排布式______ 。从电负性角度分析,C、Si和O元素的非金属活泼性由强至弱的顺序为______ 。
(2)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为______ ,微粒间存在的作用力是______ 。
(3)氧化物MO的电子总数与SiC的相等,MO是优良的耐高温材料,其晶体结构与NaCl晶体相似。MO的熔点比CaO的高,其原因是______ 。
(4)SO2、NO2、H2S同属于______ 结构(填“三角锥形”、“直线型”或“V字型”)。从微观结构角度分析,其中一种分子又与另二种分子有不同之处,该分子的化学式是______ 。
(1)写出Si的基态原子价电子排布式
(2)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为
(3)氧化物MO的电子总数与SiC的相等,MO是优良的耐高温材料,其晶体结构与NaCl晶体相似。MO的熔点比CaO的高,其原因是
(4)SO2、NO2、H2S同属于
您最近一年使用:0次
2011·陕西西安·三模
解题方法
5 . A、B、C、D、E、F、G、H八种元素都是前4周期元素,且原子序数依次增大。已知:元素A的原子中没有成对电子。元素B、C、D同周期,元素B、G同主族,且B、D、G三原子P轨道上均有2个未成对电子元素E、F、G在同一周期,且E原子中没有未成对电子。元素H的基态原子核外有6个未成对电子。
请回答下列问题:
(1)B、C、D三元素的电负性由大到小排列顺序为_______ (用元素符号表示);E、F、G三元素的原子的第一电离能由大到小排列顺序为_______ (用元素符号表示)。
(2)元素D与G所形成的晶体和元素D与B所形成的晶体熔沸点由高到低的顺序为___ (填化学式),其原因是_________ 。
(3)元素B与C的气态氢化物在A B中溶解性由大到小的顺序为
B中溶解性由大到小的顺序为___ (填化学式),其原因是________ 。
(4)B、D两元素形成的阴离子BD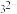 中的B的杂化类型为
中的B的杂化类型为______ ,空间结构为______ ,与BD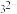 互为等电子体且含C、D两元素的微粒的化学式为
互为等电子体且含C、D两元素的微粒的化学式为______ 。
(5)A、B、C三元素各一个原子形成的分子中 键与
键与 键的个数比为
键的个数比为______ ,该分子的VSERR模型______ 。
(6)元素H的基态原子的核外电子排布为_______ ,在周期表中处于_____ 区。
请回答下列问题:
(1)B、C、D三元素的电负性由大到小排列顺序为
(2)元素D与G所形成的晶体和元素D与B所形成的晶体熔沸点由高到低的顺序为
(3)元素B与C的气态氢化物在A
 B中溶解性由大到小的顺序为
B中溶解性由大到小的顺序为(4)B、D两元素形成的阴离子BD
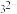 中的B的杂化类型为
中的B的杂化类型为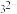 互为等电子体且含C、D两元素的微粒的化学式为
互为等电子体且含C、D两元素的微粒的化学式为(5)A、B、C三元素各一个原子形成的分子中
 键与
键与 键的个数比为
键的个数比为(6)元素H的基态原子的核外电子排布为
您最近一年使用:0次



