10-11高二下·河北衡水·阶段练习
解题方法
1 .
(1)菠菜营养丰富,素有“蔬菜之王”之称,在营养价值上是一种高效的补铁剂。某化学小组欲设计实验方案,探究菠菜中是否存在铁元素与草酸及可溶性草酸盐。甲同学查阅资料得知:草酸又名乙二酸,化学式为H2C2O4,是一种二元有机弱酸,具有较强的还原性。甲同学依据上述信息推测,菠菜中铁元素呈____ 价,其理由是____________________ 。甲同学同时设计实验方案,验证其推测是否正确。请简述实验方案_______________________________________ 。
(2)乙炔是有机合成工业的一种原料。工业上曾用 与水反应生成乙炔。
与水反应生成乙炔。
① 中
中 与
与 互为等电子体,
互为等电子体, 的电子式可表示为
的电子式可表示为_______________ ;1mol 中含有的
中含有的 键数目为
键数目为________ 。
②乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是___________________ ;分子中处于同一直线上的原子数目最多为_____ 。
(1)菠菜营养丰富,素有“蔬菜之王”之称,在营养价值上是一种高效的补铁剂。某化学小组欲设计实验方案,探究菠菜中是否存在铁元素与草酸及可溶性草酸盐。甲同学查阅资料得知:草酸又名乙二酸,化学式为H2C2O4,是一种二元有机弱酸,具有较强的还原性。甲同学依据上述信息推测,菠菜中铁元素呈
(2)乙炔是有机合成工业的一种原料。工业上曾用
 与水反应生成乙炔。
与水反应生成乙炔。①
 中
中 与
与 互为等电子体,
互为等电子体, 的电子式可表示为
的电子式可表示为 中含有的
中含有的 键数目为
键数目为②乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是
您最近一年使用:0次
名校
2 . Ⅰ.溴化铜 Ⅱ
Ⅱ 甲基咪唑配合物是一种制备有机玻璃的催化剂,其合成方法如下:
甲基咪唑配合物是一种制备有机玻璃的催化剂,其合成方法如下:

 溴化铜
溴化铜 Ⅱ
Ⅱ 甲基咪唑中
甲基咪唑中 与
与 甲基咪唑间形成的化学键称为
甲基咪唑间形成的化学键称为_______________ ; 基态核外电子排布式为
基态核外电子排布式为_________________________________ 。
 与
与 互为等电子体的阴离子为
互为等电子体的阴离子为_______________ 。
 中碳原子杂化轨道类型为
中碳原子杂化轨道类型为_______________ ;1molMIm中含 键数目为
键数目为______ mol。
Ⅱ.碳、氧、氮、镁、铬、铁、铜是几种重要的元素,请回答下列问题:
(4)Mg、O、C、N四种元素的第一电离能从大到小的顺序为________ 。
(5)查阅相关资料发现MgO的熔点比CuO的熔点高得多,其原因是_______ 。
(6)金属铬是一种银白色,极硬,耐腐蚀的金属,铬的化合物种类繁多,如:Cr2(SO4)3、 以及配离子
以及配离子 。
。
 具有很强的氧化性,能直接将
具有很强的氧化性,能直接将 氧化成
氧化成 ,试写出基态铬原子的价层电子排布式:
,试写出基态铬原子的价层电子排布式:__________________________________________ 。
 该配离子
该配离子 中,中心离子的配位数为
中,中心离子的配位数为______________ , 的VSEPR模型为
的VSEPR模型为________________________ 。
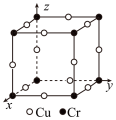
 已知晶胞中Cr和Cu原子间的最近距离为
已知晶胞中Cr和Cu原子间的最近距离为 ,则该晶体的密度为
,则该晶体的密度为___________ 
 用含a的代数式表示,设N
用含a的代数式表示,设N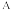 为阿伏加 德罗常数的值
为阿伏加 德罗常数的值 。
。
 Ⅱ
Ⅱ 甲基咪唑配合物是一种制备有机玻璃的催化剂,其合成方法如下:
甲基咪唑配合物是一种制备有机玻璃的催化剂,其合成方法如下:
 溴化铜
溴化铜 Ⅱ
Ⅱ 甲基咪唑中
甲基咪唑中 与
与 甲基咪唑间形成的化学键称为
甲基咪唑间形成的化学键称为 基态核外电子排布式为
基态核外电子排布式为 与
与 互为等电子体的阴离子为
互为等电子体的阴离子为 中碳原子杂化轨道类型为
中碳原子杂化轨道类型为 键数目为
键数目为Ⅱ.碳、氧、氮、镁、铬、铁、铜是几种重要的元素,请回答下列问题:
(4)Mg、O、C、N四种元素的第一电离能从大到小的顺序为
(5)查阅相关资料发现MgO的熔点比CuO的熔点高得多,其原因是
(6)金属铬是一种银白色,极硬,耐腐蚀的金属,铬的化合物种类繁多,如:Cr2(SO4)3、
 以及配离子
以及配离子 。
。 具有很强的氧化性,能直接将
具有很强的氧化性,能直接将 氧化成
氧化成 ,试写出基态铬原子的价层电子排布式:
,试写出基态铬原子的价层电子排布式: 该配离子
该配离子 中,中心离子的配位数为
中,中心离子的配位数为 的VSEPR模型为
的VSEPR模型为 已知晶胞中Cr和Cu原子间的最近距离为
已知晶胞中Cr和Cu原子间的最近距离为 ,则该晶体的密度为
,则该晶体的密度为
 用含a的代数式表示,设N
用含a的代数式表示,设N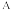 为阿伏加 德罗常数的值
为阿伏加 德罗常数的值 。
。
您最近一年使用:0次
真题
名校
3 . 科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是
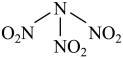

| A.分子中N、O间形成的共价键是非极性键 |
| B.分子中四个氮原子共平面 |
| C.该物质既有氧化性又有还原性 |
D.15.2g该物资含有6.02× 个原子 个原子 |
您最近一年使用:0次
2019-01-30更新
|
1467次组卷
|
38卷引用:河北省唐山市曹妃甸区第一中学2016-2017学年高二下学期期末考试化学试题
河北省唐山市曹妃甸区第一中学2016-2017学年高二下学期期末考试化学试题河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第二章 综合检测22011年普通高等学校招生全国统一考试化学卷(安徽)(已下线)2012届湖北省襄阳五中高三上学期期中考试化学试卷(已下线)2011-2012学年浙江省杭州十四中高二上学期期末化学试卷(已下线)2011-2012学年江苏省重点中学高二5月质量检测化学试卷(已下线)2011-2012学年福建省三明一中高二下学期第一次月考化学试卷(已下线)2013届江西省九江市第一中学高三入学考试化学试卷(已下线)2012-2013学年四川省成都七中高二10月阶段性考试化学试卷(已下线)2012--2013学年新疆乌鲁木齐市一中高二下学期期中考试化学试卷(特长班)(已下线)2012-2013学年四川省昭觉中学高二10月月考化学试卷(已下线)2012-2013学年江苏省启东中学高二下学期期中考试化学试卷(已下线)2013-2014甘肃省兰州一中下学期期中考试高二化学试卷(已下线)2013-2014甘肃省兰州一中下学期期中考试高二化学试卷(已下线)2013届新疆乌鲁木齐市一中高二下学期特长班期中考试化学试卷(已下线)2015届江西省南昌市三校高三上第一次联考化学试卷2014-2015宁夏银川市唐徕回民中学高二下学期3月月考化学试卷2014-2015福建省长泰县第一中学高二下学期期中化学试卷(A)2016-2017学年安徽省六安市第一中学高二下学期第一次阶段检测化学试卷甘肃省兰州第一中学2016-2017学年高一下学期期中考试化学试题安徽省定远重点中学2017-2018学年高一下学期第一次月考化学试题福建省长汀一中2017-2018学年高二实验班下学期第一次月考化学试题【全国百强校】黑龙江省实验中学2017-2018学年高二下学期期中考试(理)化学试题贵州省六盘水盘县四中2017-2018学年高二下学期期末考试化学试题(已下线)2019年3月10日 《每日一题》人教选修3-每周一测上海市交通大学附属中学2018-2019学年高一下学期期中考试化学试题山西省平遥中学校2018-2019学年高二下学期第二次月考化学试题(已下线)上海交大附中2018-2019学年高一下学期期中化学试题2020高三总复习二轮复习——物质结构与性质复习卷云南省金平县第一中学2019-2020学年高二上学期期末考试化学试题苏教版高一化学必修2专题一第二单元第二课时《共价键》(夯基提能)山东省滕州市第一中学2020届高三3月线上模拟考试化学试题(已下线)上海市奉贤区2013年高考二模化学试题安徽省六安市舒城中学2019-2020学年高二下学期第一次月考化学试题黑龙江省哈尔滨市阿城区龙涤中学2020-2021学年高二4月月考化学试题重庆市第七中学校2021-2022学年高一下学期3月月考化学试题福建省德化第一中学2021-2022学年高二下学期第一次质检化学试题安徽省青阳县第一中学2021-2022学年高二下学期3月月考化学试卷
名校
4 . 前四周期元素X、Y、Z、W核电荷数依次增大,核电荷数之和为58;Y原子的M层p轨道有3个未成对电子;Z与Y同周期,且在该周期中电负性最大;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:2。
(1)写出Z元素在元素周期表中的位置:___________ 。
(2) 与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是
与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是___________  写分子式
写分子式 。
。
(3) 的最高价氧化物的水化物的化学式为
的最高价氧化物的水化物的化学式为___________ ;
(4) 单质
单质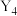 与
与 在一定条件下恰好完全反应生成
在一定条件下恰好完全反应生成 化合物C,一个C分子中所含有的σ键数目为
化合物C,一个C分子中所含有的σ键数目为___________ ;
(5)含W元素的最高化合价的含氧酸根离子是___________ ,该含氧酸根离子在分析化学中有重要作用,在酸性条件下该含氧酸根离子可将 氧化成
氧化成 ,请写出该反应的离子方程式
,请写出该反应的离子方程式___________ 。
(1)写出Z元素在元素周期表中的位置:
(2)
 与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是
与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是 写分子式
写分子式 。
。(3)
 的最高价氧化物的水化物的化学式为
的最高价氧化物的水化物的化学式为(4)
 单质
单质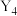 与
与 在一定条件下恰好完全反应生成
在一定条件下恰好完全反应生成 化合物C,一个C分子中所含有的σ键数目为
化合物C,一个C分子中所含有的σ键数目为(5)含W元素的最高化合价的含氧酸根离子是
 氧化成
氧化成 ,请写出该反应的离子方程式
,请写出该反应的离子方程式
您最近一年使用:0次
2021-04-21更新
|
559次组卷
|
5卷引用:河北省张家口宣化一中2020-2021学年高二下学期4月月考化学试题
名校
5 . 蔬菜和水果中富含维生素C,维生素C具有还原性,在酸性溶液中可以被 等氧化剂氧化为脱氢维生素C(已知:阿伏加德罗常数的值为
等氧化剂氧化为脱氢维生素C(已知:阿伏加德罗常数的值为 )。下列有关说法错误的是
)。下列有关说法错误的是
 等氧化剂氧化为脱氢维生素C(已知:阿伏加德罗常数的值为
等氧化剂氧化为脱氢维生素C(已知:阿伏加德罗常数的值为 )。下列有关说法错误的是
)。下列有关说法错误的是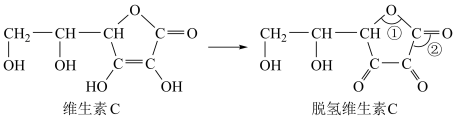
| A.脱氢维生素C中,键角①<键角② |
| B.维生素C分子中含有2个手性碳原子 |
C. 维生素C中含 维生素C中含 键数目为 键数目为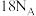 |
D.维生素C与 发生氧化还原反应时, 发生氧化还原反应时, 维生素C被氧化转移的电子数为 维生素C被氧化转移的电子数为 |
您最近一年使用:0次
2024-01-30更新
|
470次组卷
|
4卷引用:河北省武邑中学2023-2024学年高三上学期三模化学试题
名校
解题方法
6 . “证据推理与模型认知”是化学学科学习的基本素养。下列推论合理的是
| 选项 | 已知信息 | 推论 |
| A | 酸性:HI>HBr>HCl | 酸性: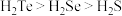 |
| B | 非金属性:F>O>N | 还原性: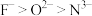 |
| C | 原子半径:Na>Mg>O | 离子半径: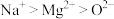 |
| D | 熔点:C>Si>Ge | 熔点: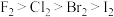 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-11更新
|
438次组卷
|
4卷引用:河北省石家庄市第二中学2022-2023学年高二下学期期末考试化学试题
河北省石家庄市第二中学2022-2023学年高二下学期期末考试化学试题湖南省衡阳市2023届高三上学期第一次统一考试(一模)化学试题(已下线)专题07 元素周期表和元素周期律(已下线)专题06 物质结构与性质
名校
解题方法
7 . 化合物A是一种绿色生态消毒剂,由原子序数依次增大的三种短周期元素X、Y、Z组成,其结构式如图,已知Z的常见单质在常温常压下为气态,下列叙述正确的是

| A.化合物A具有强氧化性 |
B.该化合物中Z的化合价均呈 价 价 |
| C.该结构中所有原子均满足8电子稳定结构 |
| D.仅有X、Y两种元素形成的化合物中不可能含有非极性共价键 |
您最近一年使用:0次
2024-03-28更新
|
58次组卷
|
2卷引用:河北省张家口市尚义县第一中学等校2023-2024学年高二下学期3月月考化学试题
8 . 光触媒是一种以纳米级TiO2为代表的具有光催化功能的光半导体材料的总称。光触媒在紫外线及可见光的照射下,会产生类似光合作用的光催化反应,产生羟基自由基和活性氧,能杀灭细菌和除去环境中的有机污染物。光触媒除去甲醛的示意图如图,下列说法错误的是
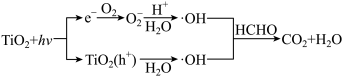

| A.·OH和活性氧具有强氧化性 |
B.HCHO的电子式为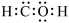 |
| C.除甲醛步骤的反应为4·OH+HCHO=CO2+3H2O |
| D.CO2中σ键与π键数目之比为1:1 |
您最近一年使用:0次
2023-04-19更新
|
87次组卷
|
2卷引用:河北省部分重点高中2022-2023年高二下学期4月期中考试化学试题
名校
解题方法
9 . 已知H和O可以形成 和
和 两种化合物,H和N可以形成
两种化合物,H和N可以形成 和
和 两种化合物,回答下列问题:
两种化合物,回答下列问题:
(1) 和
和 形成
形成 ,
, 的电子式为
的电子式为___________ 。
(2)键角:
___________ (填“>”“<”或“=”) ,理由为
,理由为___________ 。
(3) 的结构式为
的结构式为___________ ,含有___________ (填“极性”、“非极性”或“极性和非极性”)键。
(4) 是常用的氧化剂,其分子结构如图所示:
是常用的氧化剂,其分子结构如图所示:

①键能:
___________ (填“>”“<”或“=”) 。
。
② 与
与 反应生成一种空气中含量最多的气体和一种生活中最常见的液体,其化学方程式为
反应生成一种空气中含量最多的气体和一种生活中最常见的液体,其化学方程式为___________ ,氧化性:
___________ (填“>”“<”或“=”) 。
。
(5)H、N、O三种元素的第一电离能由大到小的顺序为___________ (填元素符号)。
 和
和 两种化合物,H和N可以形成
两种化合物,H和N可以形成 和
和 两种化合物,回答下列问题:
两种化合物,回答下列问题:(1)
 和
和 形成
形成 ,
, 的电子式为
的电子式为(2)键角:

 ,理由为
,理由为(3)
 的结构式为
的结构式为(4)
 是常用的氧化剂,其分子结构如图所示:
是常用的氧化剂,其分子结构如图所示:
①键能:

 。
。②
 与
与 反应生成一种空气中含量最多的气体和一种生活中最常见的液体,其化学方程式为
反应生成一种空气中含量最多的气体和一种生活中最常见的液体,其化学方程式为
 。
。(5)H、N、O三种元素的第一电离能由大到小的顺序为
您最近一年使用:0次
10 . 向重铬酸盐酸性溶液中加入乙醚和H2O2,水层发生反应:Cr2O +4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是
+4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是
 +4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是
+4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是A.由水层反应可知,氧化性:Cr2O >CrO5 >CrO5 |
| B.乙醚在检验过程中作稳定剂和萃取剂,不可用乙醇代替 |
| C.CrO5•O(C2H5)2中不存在非极性键 |
| D.水相变为绿色的离子反应为4CrO5+12H+=4Cr3++6H2O+7O2↑ |
您最近一年使用:0次



