31. 镍废料中主要含有Ni,还有少量的Cu、Fe、Pb等。现从中制取Ni
2O
3,可用于制造人造卫星、宇宙飞船的高能电池,也可用于制成镍镉碱性电池。生产流程见下:
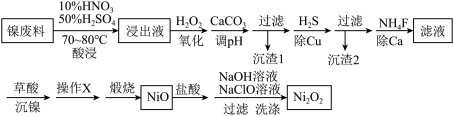
已知0.010mol/L金属离子在不同pH下的沉淀情况如下:
| Fe3+ | Cu2+ | Ni2+ | Fe2+ |
| 开始沉淀pH | 3.0 | 5.0 | 7.4 | 9.7 |
| 完全沉淀pH | 4.0 | 6.5 | 9.0 | 11 |
回答下列问题:
(1)加入碳酸钙调pH的目的是
____________________________________________,“沉渣2”的主要成分是
____________,必须先过滤“沉渣1”后再进行“除Cu”的原因是
______________________________________________________________________。
(2)用离子方程式解释加入NH
4F“除Ca”的过程
_________________。
(3)“酸浸”时参与反应的H
2SO
4与HNO
3物质的量比保持为3∶2,此时Ni单质所发生的化学方程式为
___________________________________________。
(4)“操作X”是
__________、
__________,煅烧时产生两种气体的成分是
________。
(5)向NiO中加入盐酸溶解,待完全溶解后,加入足量NaOH溶液,再加入NaClO溶液,写出其中和NaClO相关的反应的离子方程式为
_________________________________。
(6)根据上表数据,计算当0.010mol/LNiSO
4溶液中Ni
2+完全沉淀时的c(Ni
2+)=
______mol/L。