2024·江苏·模拟预测
1 . 氮的常见氢化物有氨(NH3)和肼(N2H4)。Mg3N2与水反应可产生NH3,液氨发生微弱电离产生 ,NH3中一个H被-NH2取代可得N2H4,下列有关氮及其化合物的说法正确的是
,NH3中一个H被-NH2取代可得N2H4,下列有关氮及其化合物的说法正确的是
 ,NH3中一个H被-NH2取代可得N2H4,下列有关氮及其化合物的说法正确的是
,NH3中一个H被-NH2取代可得N2H4,下列有关氮及其化合物的说法正确的是| A.N2中σ键与π键的数目比例为1∶1 |
B.液氨电离可表示为:2NH3⇌ + + |
C.N2H4的结构式为 |
| D.Mg3N2中存在Mg与N2之间的强烈相互作用 |
您最近半年使用:0次
2024·江苏·模拟预测
2 . 氟是已知元素中电负性最大、单质氧化性最强的元素,与稀有气体Xe形成的XeF2分子是非极性分子,与其他卤素形成的卤素互化物(如ClF、ClF3)具有与Cl2相似的化学性质,与氮形成的NF3可与NH3反应生成N2F2 (结构式:F—N=N—F)。自然界中,含氟矿石有萤石(CaF2)、冰晶石(Na3AlF6)等,萤石可与浓硫酸共热制取HF气体。工业上,可通过电解KF的无水HF溶液(含F-和HF 离子)制取F2。下列物质的结构、性质、用途具有对应关系的是
离子)制取F2。下列物质的结构、性质、用途具有对应关系的是
 离子)制取F2。下列物质的结构、性质、用途具有对应关系的是
离子)制取F2。下列物质的结构、性质、用途具有对应关系的是| A.浓硫酸具有脱水性,可用于干燥Cl2 |
| B.ClF3具有强氧化性,可用作火箭助燃剂 |
| C.冰晶石微溶于水,可用作电解铝工业的助熔剂 |
| D.HF(g)分子之间形成氢键,HF(g)的热稳定性比HCl(g)的高 |
您最近半年使用:0次
名校
3 . W、X、Y、Q、R为前四周期元素且原子序数依次增大。W的基态原子有3个不同能级,各能级中的电子数相等;Y原子核外电子有8种不同的运动状态,Q和 具有相同数目的未成对电子,
具有相同数目的未成对电子, 的价电子数是
的价电子数是 的二分之一,
的二分之一, 的核外电子充满三个电子层。请回答下列问题:
的核外电子充满三个电子层。请回答下列问题:
(1)基态X原子的核外电子轨道表示式为___________ 。
(2)W、X、Y的第一电离能由小到大的顺序是___________ 。(用对应元素符号作答)
(3)X、Y的气态氢化物的稳定性由大到小的顺序是___________ 。(用对应化学式作答)
(4)基态Q原子核外有___________ 种能量不同的电子,R元素在周期表中处于___________ 区。
(5) 分子中
分子中 键与
键与 键的个数比为
键的个数比为___________ 。
 具有相同数目的未成对电子,
具有相同数目的未成对电子, 的价电子数是
的价电子数是 的二分之一,
的二分之一, 的核外电子充满三个电子层。请回答下列问题:
的核外电子充满三个电子层。请回答下列问题:(1)基态X原子的核外电子轨道表示式为
(2)W、X、Y的第一电离能由小到大的顺序是
(3)X、Y的气态氢化物的稳定性由大到小的顺序是
(4)基态Q原子核外有
(5)
 分子中
分子中 键与
键与 键的个数比为
键的个数比为
您最近半年使用:0次
名校
4 . 砷化镓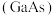 是第二代半导体材料的代表,主要用于制作高速、高频、大功率和抗辐射电子器件。一种制备砷化镓的方法为
是第二代半导体材料的代表,主要用于制作高速、高频、大功率和抗辐射电子器件。一种制备砷化镓的方法为 。
。
(1)基态As原子的核外电子排布式为___________ 。
(2)As、Ga、Se的电负性由大到小的顺序为___________ 。
(3) 中
中 键的数目为
键的数目为___________ 。
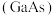 是第二代半导体材料的代表,主要用于制作高速、高频、大功率和抗辐射电子器件。一种制备砷化镓的方法为
是第二代半导体材料的代表,主要用于制作高速、高频、大功率和抗辐射电子器件。一种制备砷化镓的方法为 。
。(1)基态As原子的核外电子排布式为
(2)As、Ga、Se的电负性由大到小的顺序为
(3)
 中
中 键的数目为
键的数目为
您最近半年使用:0次
5 . 如图是某无机化合物的二聚分子,该分子中A、B两种元素都只有3个能层,分子中所有原子的最外层都达到8个电子的稳定结构。下列说法不正确 的是
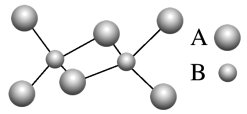
| A.元素B位于元素周期表第三周期ⅢA族 |
| B.该化合物是共价化合物,在熔融状态下能导电 |
| C.该化合物在固态时所形成的晶体是分子晶体 |
| D.该化合物中存在极性共价键,无非极性共价键 |
您最近半年使用:0次
名校
解题方法
6 .  具有还原性,一种催化氧化乙醇的反应为:
具有还原性,一种催化氧化乙醇的反应为: 。下列有关叙述正确的是
。下列有关叙述正确的是
 具有还原性,一种催化氧化乙醇的反应为:
具有还原性,一种催化氧化乙醇的反应为: 。下列有关叙述正确的是
。下列有关叙述正确的是A. 原子中的中子数为16 原子中的中子数为16 |
B. 的空间构型是直线型 的空间构型是直线型 |
C. 与 与 互溶是因为 互溶是因为 存在分子间氢键 存在分子间氢键 |
D. 分子中 分子中 键和 键和 键的数目之比为 键的数目之比为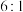 |
您最近半年使用:0次
名校
7 . 下列有关[Ni(NH3)6]SO4的说法正确的是
| A.配体为NH3,NH3的空间结构为平面三角形 |
| B.1mol[Ni(NH3)6]2+中含有18molσ键 |
| C.[Ni(NH3)6]2+中H—N—H的键角大于NH3中的键角 |
| D.由于[Ni(NH3)6]SO4是配合物,故向其中滴加BaCl2溶液不会生成沉淀 |
您最近半年使用:0次
8 . 氮、磷及其化合物应用广泛。磷元素有白磷、红磷等单质,白磷(P4)分子结构及晶胞如下图所示,实验室常用CuSO4溶液吸收有毒气体PH3,生成H3PO4、H2SO4和Cu。P元素可形成多种含氧酸,其中次磷酸(H3PO2)为一元弱酸;磷酸可与铁反应,在金属表面生成致密且难溶于水的磷酸盐膜。

| A.P4分子中的P-P-P键角为109°28′ |
| B.白磷和红磷互为同位素 |
| C.白磷晶体中1个P4分子周围有8个紧邻的P4分子 |
| D.白磷属于非极性分子 |
您最近半年使用:0次
名校
9 . 据报道,我国科学家研制出以石墨烯为载体的催化剂,在25℃下用H2O2直接将CH4转化为含氧有机物,其主要原理如图所示,下列说法正确的是
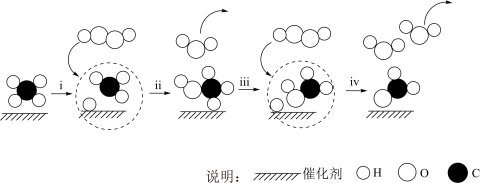
| A.CH4和H2O2含有相同的电子数 |
B.图中 表示CH4,该模型也可以表示CCl4 表示CH4,该模型也可以表示CCl4 |
| C.步骤ii涉及碳氢键的断裂与生成和碳氧键的断裂与生成 |
D.步骤i到iv的总反应为:CH4+2H2O2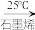 HCHO+3H2O HCHO+3H2O |
您最近半年使用:0次
名校
10 . Cu2S可用于钾离子电池的负极材料.冶炼铜时可使Cu2S在高温下与O2反应转化为Cu2O,生成的Cu2O与Cu2S进一步反应得到Cu。Cu2O在酸性溶液中会转化为Cu和Cu2+;Cu2S能被浓硝酸氧化为Cu(NO3)2.Cu在O2存在下能与氨水反应生成[Cu(NH3)4]2+;Cu(OH)2能与NaOH反应生成Na2[Cu(OH)4]。O3、O2的沸点分别为-111℃、-182℃。下列说法正确的是
| A.SO2的键角比SO3的大 | B.SO2是非极性分子 |
| C.1mol[Cu(NH3)4]2+含有16mol的σ键 | D.O2分子间作用力比O3的大 |
您最近半年使用:0次



