1 . 研究发现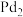 团簇可催化CO的氧化,在催化过程中路径不同可能生成不同的过渡态和中间产物(过渡态已标出),下图为路径1和路径2催化的能量变化。下列说法正确的是
团簇可催化CO的氧化,在催化过程中路径不同可能生成不同的过渡态和中间产物(过渡态已标出),下图为路径1和路径2催化的能量变化。下列说法正确的是
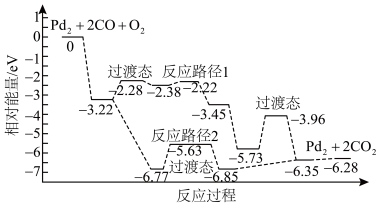
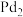 团簇可催化CO的氧化,在催化过程中路径不同可能生成不同的过渡态和中间产物(过渡态已标出),下图为路径1和路径2催化的能量变化。下列说法正确的是
团簇可催化CO的氧化,在催化过程中路径不同可能生成不同的过渡态和中间产物(过渡态已标出),下图为路径1和路径2催化的能量变化。下列说法正确的是
| A.该过程中有极性键和非极性键的断裂和生成 |
| B.路径1中最大能垒(活化能)E正=1.77eV,为路径1的决速步 |
C.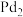 团簇可有效提高CO的平衡转化率 团簇可有效提高CO的平衡转化率 |
| D.反应路径1的催化效果更好 |
您最近一年使用:0次
名校
解题方法
2 . 已知A、B、C、D都是周期表中的短周期元素,它们的核电荷数依次增大。A原子、C原子的L能层中都有两个未成对的电子,C、D同主族。E、F都是第四周期元素,E原子核外有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满。根据以上信息填空:
(1)D的最高价氧化物的空间构型为_________ 。
(2)E2+的价层电子排布图是___________ ,F原子的电子排布式是___________ 。
(3)A的最高价氧化物对应的水化物分子结构式为_______ ,其中心原子采取的轨道杂化方式为_________ ,B的简单气态氢化物的空间构型经过分析为三角锥形,判断依据是_________ 。
(4)化合物AC2、B2C和阴离子DAB-互为等电子体,含DAB-的水溶液可以用于实验室中E3+的定性检验,检验E3+的离子方程式为________ 。
(1)D的最高价氧化物的空间构型为
(2)E2+的价层电子排布图是
(3)A的最高价氧化物对应的水化物分子结构式为
(4)化合物AC2、B2C和阴离子DAB-互为等电子体,含DAB-的水溶液可以用于实验室中E3+的定性检验,检验E3+的离子方程式为
您最近一年使用:0次
名校
解题方法
3 . 化合物A是一种新型锅炉水除氧剂,其结构式如图,下列说法不正确的是
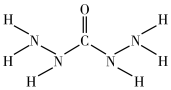

| A.A分子中既含极性键,又含非极性键 |
| B.A是有机化合物,由分子结构可知其难溶于水 |
| C.A分子中的共用电子对数为12 |
| D.A除氧时N元素被氧化 |
您最近一年使用:0次
名校
4 . 许多元素及它们的化合物在科学研究和工业生产中具有许多用途。请回答下列有关问题:
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。基态Ti原子的价层电子排布式为___________ ,电负性B___________ H (填“大于”或“小于”)。
(2)CH 、 —CH3、CH3-都是重要的有机反应中间体。CH
、 —CH3、CH3-都是重要的有机反应中间体。CH 的空间构型为
的空间构型为___________ ; 分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数( 如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数( 如苯分子中的大π键可表示为 ,则CO
,则CO 中的大π键应表示为
中的大π键应表示为___________ 。
(3)血红蛋白的结构如图所示,其中N原子的杂化方式为___________ 。

(4)焦炭、金刚石和C60都是碳的单质。已知金刚石中碳碳键的键长为154.45pm,C60中碳碳键的键长为140~ 145pm,二者比较熔点高的是___________ ,理由是___________ 。
(5)已知,铁有 、
、 、δ三种晶体结构,并且在一定条件下可以相互转化(如图), 请回答相关的问题:
、δ三种晶体结构,并且在一定条件下可以相互转化(如图), 请回答相关的问题:

①相同体积的 、
、 、δ三种晶体的质量比为
、δ三种晶体的质量比为___________ 。
②一种由铁、碳形成的间隙化合物的晶体结构如图所示,其中碳原子位于铁原子形成的八面体的中心,每个铁原子又为两个八面体共用,则该化合物的化学式为___________ ,该晶体中铁原子配位数为___________ 。

(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。基态Ti原子的价层电子排布式为
(2)CH
 、 —CH3、CH3-都是重要的有机反应中间体。CH
、 —CH3、CH3-都是重要的有机反应中间体。CH 的空间构型为
的空间构型为 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数( 如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数( 如苯分子中的大π键可表示为 ,则CO
,则CO 中的大π键应表示为
中的大π键应表示为(3)血红蛋白的结构如图所示,其中N原子的杂化方式为

(4)焦炭、金刚石和C60都是碳的单质。已知金刚石中碳碳键的键长为154.45pm,C60中碳碳键的键长为140~ 145pm,二者比较熔点高的是
(5)已知,铁有
 、
、 、δ三种晶体结构,并且在一定条件下可以相互转化(如图), 请回答相关的问题:
、δ三种晶体结构,并且在一定条件下可以相互转化(如图), 请回答相关的问题: 
①相同体积的
 、
、 、δ三种晶体的质量比为
、δ三种晶体的质量比为②一种由铁、碳形成的间隙化合物的晶体结构如图所示,其中碳原子位于铁原子形成的八面体的中心,每个铁原子又为两个八面体共用,则该化合物的化学式为

您最近一年使用:0次
5 . 下列说法正确的是
| A.单质晶体硅为分子晶体 |
| B.乙烯分子中,碳原子的sp2杂化轨道形成σ键,未杂化的2p轨道形成π键 |
| C.键长H—F<H—Cl<H—Br<H—I,因此晶体熔点HF<HCl<HBr<HI |
| D.PH3分子中孤电子对与成键电子对的排斥作用比成键电子对之间的排斥作用弱 |
您最近一年使用:0次
名校
解题方法
6 . 设NA为阿伏加德罗常数值,下列有关叙述正确的是
| A.4.5gSiO2中含有的硅氧键的数目为0.3NA |
| B.标准状况下,11.2L甲烷和乙烯混合物中含氢原子数目为4NA |
| C.100mL1.0mol•L-1Na2CO3溶液中所含氧原子数目为0.3NA |
| D.加热条件下,将足量Fe投入含有1mol硫酸的浓硫酸中,生成0.5NA个SO2分子 |
您最近一年使用:0次
7 . 已知H-H键的键能为
 ,I-I键的键能为
,I-I键的键能为
 ,一定条件下
,一定条件下
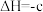
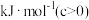 。下列说法正确的是
。下列说法正确的是

 ,I-I键的键能为
,I-I键的键能为
 ,一定条件下
,一定条件下
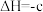
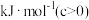 。下列说法正确的是
。下列说法正确的是A.断开1mol Br-Br键所需的能量小于 kJ kJ |
| B.上述反应中,反应物的总能量低于生成物的总能量 |
C.向密闭容器中加入2mol  和2mol 和2mol 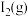 ,充分反应后放出 ,充分反应后放出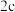 kJ热量 kJ热量 |
D.断开2mol H-I键所需的能量为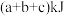 |
您最近一年使用:0次
2021-10-19更新
|
79次组卷
|
2卷引用:云南省部分名校2021-2022学年高二上学期第一次月考联考化学试卷
名校
8 . 下表所列数据是在相同条件下,不同物质中氧氧键的键长和键能的实测数据,下列有关说法中正确的是
| 微粒 | O | O | O2 | O |
| 键长/pm | 149 | 128 | 121 | 112 |
| 键能/ kJ·mol-1 | a | b | 496 | 628 |
| A.a<b | B.O-O键的键能为496 kJ·mol-1 |
C.O 中存在π键 中存在π键 | D.键长越长,键能越大 |
您最近一年使用:0次
2021-07-12更新
|
413次组卷
|
3卷引用:云南省永胜县第一中学2020-2021学年高二下学期6月份考试化学试题
9 . 等电子体指原子总数相同、价电子总数也相同的微粒。下列各选项中的两种微粒不互为等电子体的是
| A.N2O和CO2 | B.O3和NO | C.CH4和NH | D.OH-和NH |
您最近一年使用:0次
名校
10 . 下列有关化学键类型的判断不正确的是
| A.s-s σ键与s-p σ键的对称性不同 |
| B.分子中含有共价键,则至少含有一个σ键 |
| C.已知乙炔的结构式为H—C≡C—H,则乙炔分子中存在2个σ键(C—H)和3个π键(C≡C) |
| D.乙烷分子中只存在σ键,即6个C—H键和1个C—C键都为σ键,不存在π键 |
您最近一年使用:0次
2021-07-12更新
|
581次组卷
|
4卷引用:云南省马关县一中2020-2021学年高二下学期6月月考化学试题
云南省马关县一中2020-2021学年高二下学期6月月考化学试题(已下线)2.1.1 共价键的类型-σ键和π键-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)(已下线)第2.1.1讲 共价键-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)2.1共价键模型(课中)-鲁科版选择性必修2



