名校
解题方法
1 . HCHO(g)与O2(g)在催化剂Ca5(PO4)₃(OH) (简写为HAP)表面催化生成CO2(g)和H2O(g)的历程示意图如下。已知该反应在较高温度下不能自发进行。

下列说法正确的是

下列说法正确的是
| A.基态Ca原子的内层电子为全充满 | B.原子半径:r(P)>r(Ca) |
| C.HCHO与H2O分子中的键角相同 | D.PO 的空间结构为正四面体形 的空间结构为正四面体形 |
您最近一年使用:0次
解题方法
2 . 材料的发展水平始终是时代进步和人类文明的标志。当前含铁的磁性材料在国防、电子信息等领域中具有广泛应用。请回答下列问题:
(1)基态铁原子的价电子排布图为_______ ,基态铁原子核外电子的空间运动状态有_______ 种, 其处在最高能层的电子的电子云形状为_______ 。
(2)一种新研发出的铁磁性材料M的分子结构如图1所示。
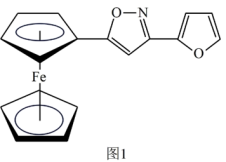
①M分子中C、N、O三种元素的电负性由大到小的顺序为_______ 。
②M分子中的Fe2+与上下两个五元碳环通过配位键相连且Fe2+共提供了6个杂化轨道,则铁原子最可能的杂化方式为_______ (填序号)。
A.sp2 B.sp3 C.dsp2 D.d2sp3
③分子中的大π键可用符号π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π ), 则M分子中由碳、氧组成的五元环中的大π键应表示为
), 则M分子中由碳、氧组成的五元环中的大π键应表示为_______ 。
(3)铁氮化合物因其特殊的组成和结构而具有优异的铁磁性能,某铁氮化合物的立方晶胞结构如图2所示。
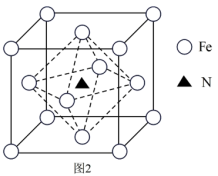
①若以氮原子为晶胞顶点,则铁原子在晶胞中的位置为_______ 。
②该化合物的化学式为_______
(1)基态铁原子的价电子排布图为
(2)一种新研发出的铁磁性材料M的分子结构如图1所示。

①M分子中C、N、O三种元素的电负性由大到小的顺序为
②M分子中的Fe2+与上下两个五元碳环通过配位键相连且Fe2+共提供了6个杂化轨道,则铁原子最可能的杂化方式为
A.sp2 B.sp3 C.dsp2 D.d2sp3
③分子中的大π键可用符号π
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π ), 则M分子中由碳、氧组成的五元环中的大π键应表示为
), 则M分子中由碳、氧组成的五元环中的大π键应表示为(3)铁氮化合物因其特殊的组成和结构而具有优异的铁磁性能,某铁氮化合物的立方晶胞结构如图2所示。

①若以氮原子为晶胞顶点,则铁原子在晶胞中的位置为
②该化合物的化学式为
您最近一年使用:0次
3 . 卤族元素包括F、Cl、Br、I等元素。下列说法正确的是
| A.电负性:F<Cl<Br<I | B.键能:HF<HBr |
| C.失电子能力:Cl—<Br—<I— | D.键的极性:Cl—I<Br—I |
您最近一年使用:0次
2022-05-31更新
|
306次组卷
|
2卷引用:江苏省徐州市第七中学2022-2023学年高三上学期10月学情调研化学试题
名校
4 . 反应HCHO + O2 H2O + CO2可用于消除甲醛污染。下列说法正确的是
H2O + CO2可用于消除甲醛污染。下列说法正确的是
 H2O + CO2可用于消除甲醛污染。下列说法正确的是
H2O + CO2可用于消除甲醛污染。下列说法正确的是A.CO2的电子式为: |
| B.O的第一电离能比同周期相邻元素小 |
| C.H2O为非极性分子 |
| D.HCHO中σ键和π键的数目比为2∶1 |
您最近一年使用:0次
2022-04-18更新
|
272次组卷
|
2卷引用:江苏省徐州市第七中学2021-2022学年高三下学期考前模拟化学试题
名校
5 . [Cu(OH)(NH3)]+是汽车尾气脱硝的催化剂,其催化机理如图所示,下列说法错误的是
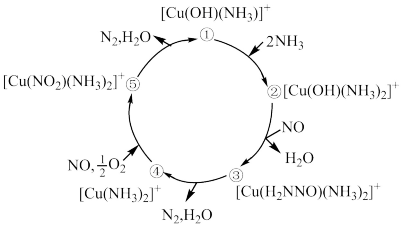
| A.[Cu(OH)(NH3)]+中O和N原子是配位原子 |
| B.该催化循环中Cu的成键数目发生了变化 |
| C.反应过程中存在非极性键的断裂和形成 |
D.总反应的化学方程式为:4NH3+2NO+2O2 3N2+6H2O 3N2+6H2O |
您最近一年使用:0次
2021-12-22更新
|
553次组卷
|
5卷引用:江苏省徐州市第七中学2021-2022学年高三下学期2月检测化学试题



