名校
解题方法
1 . 含磷物质之间可发生如图所示转化, 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是

 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
A. 白磷分子中含有 白磷分子中含有 键的数目为 键的数目为 |
B.标准状况下, 含有的分子数为 含有的分子数为 |
C.反应Ⅰ生成 转移的电子数为 转移的电子数为 |
D. 溶液中 溶液中 数目之和为 数目之和为 |
您最近一年使用:0次
解题方法
2 . 现有前四周期A、B、C、D、E、F、G七种元素,它们的原子序数依次增大。其中:A元素原子的核外电子数与其能层数相等,B元素原子的价层电子数为4,C元素基态原子的p能级电子数比s能级电子数少1,D与F在同一主族,且元素F的最高正价与其最低负价的绝对值的差值为4,E元素原子的第一至第三电离能分别是 =496kJ/mol,
=496kJ/mol, =4562kJ/mol,
=4562kJ/mol, =6912kJ/mol,G元素位于元素周期表中的第7列(从左至右)。请根据以上有关信息,回答有关问题:
=6912kJ/mol,G元素位于元素周期表中的第7列(从左至右)。请根据以上有关信息,回答有关问题:
(1)C的元素符号为_______ ,其基态原子的电子排布式为_______ ;
(2)G在元素周期表中的位置是_______ ,其正二价阳离子的价层电子排布图为_______ ;
(3)D、E、F三种元素的简单离子半径由大到小的顺序是_______ (用离子符号表示),D、F可分别与A形成 、
、 两种分子,前者的稳定性强于后者,原因是
两种分子,前者的稳定性强于后者,原因是_______ ;D与E可形成原子个数比为1:1的离子化合物,该化合物中所含有的化学键类型是_______ ;
(4)已知共价分子ABC,分子中各原子均达到稳定结构,则该分子的结构式为_______ ,0.2mol该分子所含有的π键数目是_______  。
。
 =496kJ/mol,
=496kJ/mol, =4562kJ/mol,
=4562kJ/mol, =6912kJ/mol,G元素位于元素周期表中的第7列(从左至右)。请根据以上有关信息,回答有关问题:
=6912kJ/mol,G元素位于元素周期表中的第7列(从左至右)。请根据以上有关信息,回答有关问题:(1)C的元素符号为
(2)G在元素周期表中的位置是
(3)D、E、F三种元素的简单离子半径由大到小的顺序是
 、
、 两种分子,前者的稳定性强于后者,原因是
两种分子,前者的稳定性强于后者,原因是(4)已知共价分子ABC,分子中各原子均达到稳定结构,则该分子的结构式为
 。
。
您最近一年使用:0次
名校
解题方法
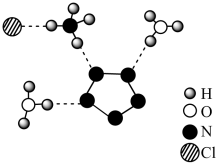
3 . 我国科学家成功合成了世界上首个五氮阴离子盐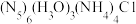 ,其局部结构如下图所示,下列说法中错误的是
,其局部结构如下图所示,下列说法中错误的是
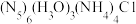 ,其局部结构如下图所示,下列说法中错误的是
,其局部结构如下图所示,下列说法中错误的是
A.该化合物中两种阳离子的中心原子均采取 杂化 杂化 |
| B.该化合物中两种阳离子的空间构型分别为正四面体形和三角锥形 |
C.阴离子 中的 中的 键总数为5个 键总数为5个 |
| D.该化合物中只存在共价键、氢键和配位键三种作用力 |
您最近一年使用:0次
2023-02-27更新
|
256次组卷
|
2卷引用:重庆市渝东九校联盟2021-2022学年高二下学期期中考试化学试题
名校
解题方法
4 . 治疗新冠肺炎药物瑞德西韦可显著降低新冠高危患者的住院风险,主要成分结构如下图,下列说法正确的是


| A.该分子不含手性碳原子 |
| B.分子中N、O、P原子的原子半径由大到小的关系为P>N>O |
| C.分子中的N-H键的键长小于O-H键的键长 |
| D.分子中只存在σ键 |
您最近一年使用:0次
2023-02-27更新
|
305次组卷
|
4卷引用:重庆市渝东九校联盟2021-2022学年高二下学期期中考试化学试题
名校
解题方法
5 . 下列选项中排序不正确的是
| A.热稳定性:HF>HCl>HBr>HI | B.硬度由大到小:金刚石>碳化硅>晶体硅 |
| C.第一电离能:F>N>O>C | D.分子中键角: |
您最近一年使用:0次
2023-02-27更新
|
434次组卷
|
2卷引用:重庆市渝东九校联盟2021-2022学年高二下学期期中考试化学试题
名校
解题方法
6 . 化合物A是含有草酸根( )的铜配合物(结构如下图),可加热分解制备Cu纳米颗粒。请回答以下相关问题:
)的铜配合物(结构如下图),可加热分解制备Cu纳米颗粒。请回答以下相关问题:
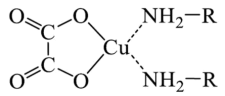
(1)草酸根中C原子的杂化方式为_______ 。
(2)上述的C、H、O、N四种元素中,第一电离能由小到大的顺序为_______ (用元素符号回答,下同),其中,第一电离能最大的元素的原子的价层电子的轨道表达式(电子排布图)为_______ ,该元素第一电离能较大的原因是_______ 。
(3)该配合物加热会生成一种气体,该气体与N2O是等电子体,其分子构型为_______ 。
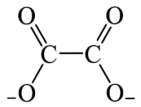
(4)草酸根( )的结构如下图所示,其中σ键和π键的比例为
)的结构如下图所示,其中σ键和π键的比例为_______ 。
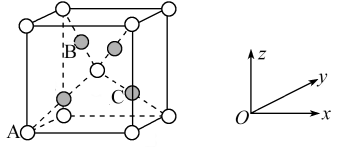
(5)在一定温度加热配合物会生成Cu2O,其中基态Cu+的价层电子排布式为_______ 。Cu2O的晶胞如下图所示,若A原子的坐标参数为(0,0,0),C原子的坐标参数为( ,
, ,
, ),则B原子的坐标参数为
),则B原子的坐标参数为_______ 。若最近的两个O2-的距离为anm,阿伏加德罗常数为NA,则该晶体的密度为_______ g·cm-3。
 )的铜配合物(结构如下图),可加热分解制备Cu纳米颗粒。请回答以下相关问题:
)的铜配合物(结构如下图),可加热分解制备Cu纳米颗粒。请回答以下相关问题:
(1)草酸根中C原子的杂化方式为
(2)上述的C、H、O、N四种元素中,第一电离能由小到大的顺序为
(3)该配合物加热会生成一种气体,该气体与N2O是等电子体,其分子构型为
(4)草酸根(
 )的结构如下图所示,其中σ键和π键的比例为
)的结构如下图所示,其中σ键和π键的比例为
(5)在一定温度加热配合物会生成Cu2O,其中基态Cu+的价层电子排布式为
 ,
, ,
, ),则B原子的坐标参数为
),则B原子的坐标参数为
您最近一年使用:0次
名校
解题方法
7 . AlN、SiC的成键结构与金刚石相似,晶体中只存在Al-N键、Si-C键。下列说法错误的是
| A.AlN中存在配位键 | B.晶体中所有原子均采取sp3杂化 |
| C.SiC中原子数与共价键数之比为1:1 | D.SiC的熔点比金刚石低 |
您最近一年使用:0次
2023-01-01更新
|
423次组卷
|
4卷引用:重庆南开中学2022-2023学年高三第五次质量检测化学试题
重庆南开中学2022-2023学年高三第五次质量检测化学试题(已下线)北京市海淀区2023届高三上学期期末考试变式汇编(1-7)福建省莆田第一中学2022-2023学年高二下学期第二学段(期中)考试化学试题黑龙江省哈尔滨市宾县第二中学2022-2023学年高二下学期第二次月考化学试题
解题方法
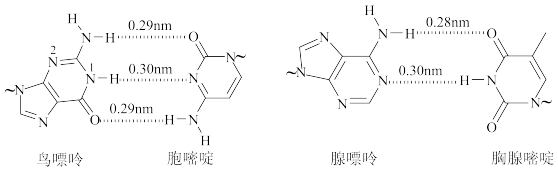
8 . DNA中四种碱基间的配对方式如图(~代表糖苷键,“ ”代表氢键),下列说法错误的是
”代表氢键),下列说法错误的是
 ”代表氢键),下列说法错误的是
”代表氢键),下列说法错误的是
| A.基态原子的第一电离能:N>O | B. 与 与 通过配位键形成 通过配位键形成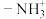 |
C.鸟嘌吟中1号N的杂化类型为 | D.鸟嘌吟中N—H键的平均键长大于0.29nm |
您最近一年使用:0次
名校
9 . A、B、C、D、E五种短周期元素。基态A原子核外电子的L层电子数是K层的2倍;B原子基态时的2p轨道上有3个未成对的电子;C元素在地壳中含量最高;D元素核外有3个电子层,最外层电子数是核外电子总数的 ;E的最外层电子数与其核外电子总数之比为3:8。
;E的最外层电子数与其核外电子总数之比为3:8。
(1)B的元素符号为_______ ,D元素在周期表中位置为_______ 。
(2)A、C形成的简单氢化物的键角顺序_______ (填化学式),并分析原因:_______ 。
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是_______ (填化学式),理由是_______ 。
(4)元素的非金属性C_______ (填“>”或“<”)E,并用化学原理证明(用化学方程式表示)_______ 。
 ;E的最外层电子数与其核外电子总数之比为3:8。
;E的最外层电子数与其核外电子总数之比为3:8。(1)B的元素符号为
(2)A、C形成的简单氢化物的键角顺序
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是
(4)元素的非金属性C
您最近一年使用:0次
名校
10 . 钒(V)固氮酶种类众多,其中一种结构如图所示。说法错误的是
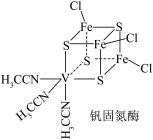

A. 中所含σ键与π键数目之比为5∶1 中所含σ键与π键数目之比为5∶1 |
B. 中碳的杂化类型为 中碳的杂化类型为 和sp 和sp |
| C.根据价电子排布可推测V的化合价可能有+5 |
| D.可通过向硫化钠溶液中通入少量氯气来证明非金属性Cl>S |
您最近一年使用:0次
2022-12-15更新
|
271次组卷
|
2卷引用:重庆市第八中学校2022-2023学年高二上学期第二次月考化学试题



