名校
解题方法
1 . 类比是一种重要的学习方法,下列“类比”正确的是
A.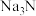 与盐酸反应生成 与盐酸反应生成 和 和 ,则 ,则 与盐酸反应生成 与盐酸反应生成 和 和 |
B. 与 与 反应生成 反应生成 和 和 ,则 ,则 与 与 反应生成 反应生成 和 和 |
C.可用 固体与浓硫酸加热制 固体与浓硫酸加热制 气体,则可用 气体,则可用 固体与浓硫酸加热制 固体与浓硫酸加热制 气体 气体 |
D. 中C为 中C为 杂化,则 杂化,则 中 中 也为 也为 杂化 杂化 |
您最近一年使用:0次
名校
2 . TiCl4是制备金属钛的重要中间体。某小组同学利用如图装置在实验室制备(夹持装置略去)。
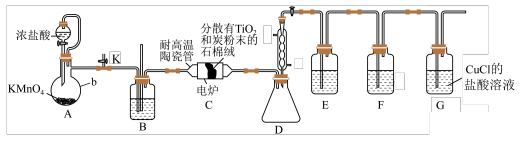
已知:TiCl4易挥发,高温时能与O2反应,不与HCl反应,其他相关信息如表所示:
回答下列问题:
(1)装置B中的试剂是___________ (填试剂名称)。
(2)装置D的作用是___________ ,装置C中除生成 外,还生成CO,该反应的化学方程式为
外,还生成CO,该反应的化学方程式为___________ 。
(3)利用G装置可以将CO吸收得到氯化羰基亚铜[Cu2Cl2(CO)2•2H2O],其结构如图所示。试从结构角度分析,CuCl的盐酸溶液可以吸收CO的原因是___________ 。
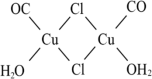
(4)可以选用下面的一套装置___________(填标号)替换掉装置E和F。
(5)利用如图装置测定所得TiCl4的纯度:取2.0g产品加入烧瓶中,向安全漏斗中加入适量蒸馏水,待TiCl4充分反应后,将烧瓶和漏斗中的液体一并转入锥形瓶中,滴加几滴0.1mol•L-1K2CrO4溶液作指示剂,用1.00mol•L-1AgNO3标准溶液滴定至终点,消耗标准溶液40.00mL。已知:常温下Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.1×10-12,Ag2CrO4呈砖红色,TiCl4+(2+n)H2O=TiO2•nH2O↓+4HCl。
①安全漏斗中的水在本实验中的作用除与TiCl4反应外,还有________ 。
②滴定终点的判断方法是_________ 。
③已知TiCl4的摩尔质量是190g/mol,则产品的纯度为______ (保留两位有效数字)。

已知:TiCl4易挥发,高温时能与O2反应,不与HCl反应,其他相关信息如表所示:
| 熔点/℃ | 沸点/℃ | 密度/(g•cm-3) | 水溶性 | |
| TiCl4 | -24 | 136.4 | 1.7 | 易水解生成白色沉淀,能溶于有机溶剂 |
(1)装置B中的试剂是
(2)装置D的作用是
 外,还生成CO,该反应的化学方程式为
外,还生成CO,该反应的化学方程式为(3)利用G装置可以将CO吸收得到氯化羰基亚铜[Cu2Cl2(CO)2•2H2O],其结构如图所示。试从结构角度分析,CuCl的盐酸溶液可以吸收CO的原因是

(4)可以选用下面的一套装置___________(填标号)替换掉装置E和F。
A. | B. | C. | D. |

①安全漏斗中的水在本实验中的作用除与TiCl4反应外,还有
②滴定终点的判断方法是
③已知TiCl4的摩尔质量是190g/mol,则产品的纯度为
您最近一年使用:0次
名校
3 . 七叶亭是一种植物抗菌素,适用于细菌性痢疾,其结构如图,下列说法,正确的是
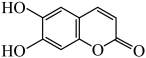

A.分子中存在 种官能团,无手性碳原子 种官能团,无手性碳原子 |
| B.分子中所有碳原子共平面,且碳原子的杂化方式只有一种 |
C. 该物质与足量溴水反应,最多可消耗 该物质与足量溴水反应,最多可消耗 Br2 Br2 |
D. 该物质与足量 该物质与足量 溶液反应,最多可消耗 溶液反应,最多可消耗 |
您最近一年使用:0次
名校
解题方法
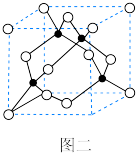
4 . 氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如图一所示。下列叙述错误的是
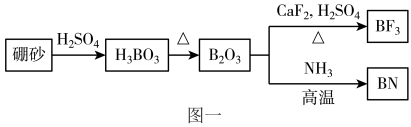


A.H3BO3在水溶液中发生反应: ,可知H3BO3是一元弱酸 ,可知H3BO3是一元弱酸 |
| B.六方氮化硼在高温高压下,可以转化为立方氮化硼,其晶胞结构如图二,立方氮化硼晶胞中含有4个氮原子、4个硼原子 |
| C.由B2O3可制备晶体硼,晶体硼的熔点2573K,沸点2823K,硬度大,属于共价晶体 |
| D.NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一,1 mol NH4BF4含有配位键的数目为NA |
您最近一年使用:0次
名校
解题方法
5 . 一种含Pt催化剂活化甲烷中碳氢键的反应机理如图所示。下列说法错误的是
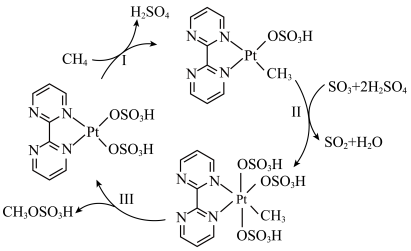

| A.反应II、III一定存在电子转移 |
| B.该过程涉及的氧化物均为含极性键的极性分子 |
| C.催化循环中含S的分子或离子VSEPR模型不完全相同 |
D.上述过程的总反应: |
您最近一年使用:0次
名校
解题方法
6 . 下列化学或离子方程式书写正确的是
A.硫酸铜溶液中滴入几滴氨水: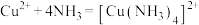 |
B.MgO溶于 溶液: 溶液: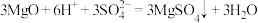 |
C.将稀硫酸加入硫代硫酸钠溶液中: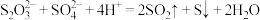 |
D. 加入大量水中: 加入大量水中: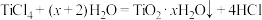 |
您最近一年使用:0次
名校
解题方法
7 . 氨基酸是构成人体必备蛋白质的基础,某氨基酸的结构简式如图所示。下列说法正确的是
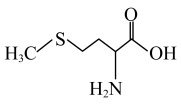
| A.第一电离能:O>N>C>H |
| B.该分子中碳原子的杂化类型有sp、sp2和sp3 |
| C.基态氧原子的电子有8种运动状态 |
| D.该物质所含元素中,电负性最大的是N |
您最近一年使用:0次
2024-03-09更新
|
251次组卷
|
2卷引用:重庆市大足中学2023-2024学年高三下学期3月适应性考试化学试题
名校
解题方法
8 . 三氯化硼( )是一种重要的化工原料,可用来制造氮化硼及硼烷化合物等。查阅资料可知:
)是一种重要的化工原料,可用来制造氮化硼及硼烷化合物等。查阅资料可知:
① 的熔点为
的熔点为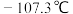 ,沸点为12.5℃,与水(包括水蒸气)能剧烈反应生成硼酸(
,沸点为12.5℃,与水(包括水蒸气)能剧烈反应生成硼酸( ),同时有白雾出现。
),同时有白雾出现。
②硼与铝的性质相似。硼与强酸或强碱溶液均能反应,与HCl气体反应生成 。
。
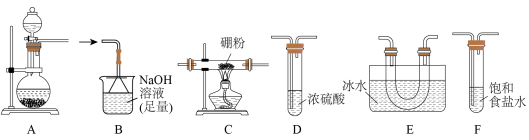
据此,某实验小组利用下列装置制备 (原理为
(原理为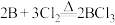 )。
)。
(1) 分子的空间结构为
分子的空间结构为__________ 。
(2)装置F的作用为__________ ,装置E的作用为____________________ 。
(3)实验装置合理的连接顺序为_______ →D→B。(装置可重复使用)
(4)连接好仪器,装入药品前,应进行的操作是_________ 。
(5)写出装置A中发生反应的化学方程式:____________________________ 。
(6)测定 产品中氯元素的含量。
产品中氯元素的含量。
称取a g样品置于蒸馏水中完全水解,并配制成100mL溶液,取出25mL于锥形瓶中,再加入
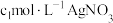 溶液使
溶液使 充分沉淀,然后加入3mL硝基苯(常温常压下,密度为
充分沉淀,然后加入3mL硝基苯(常温常压下,密度为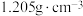 ),振荡、静置,再向锥形瓶中滴加3滴
),振荡、静置,再向锥形瓶中滴加3滴 溶液作指示剂,用
溶液作指示剂,用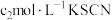 标准溶液滴定
标准溶液滴定 (发生反应
(发生反应 ),达到滴定终点时,消耗标准溶液
),达到滴定终点时,消耗标准溶液 。已知:
。已知: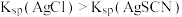 ;该实验条件下,硼酸不与
;该实验条件下,硼酸不与 反应。
反应。
①达到滴定终点时的现象为_________ 。
②样品中氯元素的质量分数为_______ %。若其他操作都正确,仅滴定管没有用KSCN标准溶液润洗,则测得产品中 的质量分数
的质量分数_______ (填“偏高”“偏低”或“无影响”)。
 )是一种重要的化工原料,可用来制造氮化硼及硼烷化合物等。查阅资料可知:
)是一种重要的化工原料,可用来制造氮化硼及硼烷化合物等。查阅资料可知:①
 的熔点为
的熔点为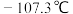 ,沸点为12.5℃,与水(包括水蒸气)能剧烈反应生成硼酸(
,沸点为12.5℃,与水(包括水蒸气)能剧烈反应生成硼酸( ),同时有白雾出现。
),同时有白雾出现。②硼与铝的性质相似。硼与强酸或强碱溶液均能反应,与HCl气体反应生成
 。
。据此,某实验小组利用下列装置制备
 (原理为
(原理为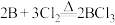 )。
)。
(1)
 分子的空间结构为
分子的空间结构为(2)装置F的作用为
(3)实验装置合理的连接顺序为
(4)连接好仪器,装入药品前,应进行的操作是
(5)写出装置A中发生反应的化学方程式:
(6)测定
 产品中氯元素的含量。
产品中氯元素的含量。称取a g样品置于蒸馏水中完全水解,并配制成100mL溶液,取出25mL于锥形瓶中,再加入

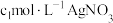 溶液使
溶液使 充分沉淀,然后加入3mL硝基苯(常温常压下,密度为
充分沉淀,然后加入3mL硝基苯(常温常压下,密度为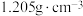 ),振荡、静置,再向锥形瓶中滴加3滴
),振荡、静置,再向锥形瓶中滴加3滴 溶液作指示剂,用
溶液作指示剂,用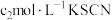 标准溶液滴定
标准溶液滴定 (发生反应
(发生反应 ),达到滴定终点时,消耗标准溶液
),达到滴定终点时,消耗标准溶液 。已知:
。已知: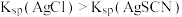 ;该实验条件下,硼酸不与
;该实验条件下,硼酸不与 反应。
反应。①达到滴定终点时的现象为
②样品中氯元素的质量分数为
 的质量分数
的质量分数
您最近一年使用:0次
2024-03-08更新
|
277次组卷
|
3卷引用:重庆市璧山来凤中学等多校联考2023-2024学年高三下学期3月月考化学试题
名校
解题方法
9 . 用于治疗糖尿病的某药物W可以用3−氨基−1−金刚烷醇(结构如图)为原料合成。下列有关3−氨基−1−金刚烷醇的说法正确的是
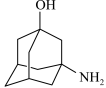
| A.分子中含有手性碳原子 | B.分子中N原子采取 杂化 杂化 |
C.分子中键长: | D.分子式为 |
您最近一年使用:0次
2024-03-08更新
|
142次组卷
|
2卷引用:重庆市璧山来凤中学等多校联考2023-2024学年高三下学期3月月考化学试题
名校
10 . 氟利昂 破坏臭氧层的反应过程如图所示。设
破坏臭氧层的反应过程如图所示。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 破坏臭氧层的反应过程如图所示。设
破坏臭氧层的反应过程如图所示。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
A.0.5mol由 、 、 组成的混合物中共价键的数目为 组成的混合物中共价键的数目为 |
B.1.6g由 和 和 组成的混合气体中含有的原子总数为 组成的混合气体中含有的原子总数为 |
C.标准状况下,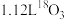 中含有的中子总数为 中含有的中子总数为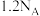 |
D.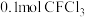 的中心原子的孤电子对数为 的中心原子的孤电子对数为 |
您最近一年使用:0次
2024-03-08更新
|
85次组卷
|
2卷引用:重庆市璧山来凤中学等多校联考2023-2024学年高三下学期3月月考化学试题



