解题方法
1 . 微颗粒的氧化锌作为一种纳米材料开始在相关领域发挥作用,利用锌焙砂 主要成分为
主要成分为 ,含
,含 及铅、铜、镉的氧化物
及铅、铜、镉的氧化物 生产高纯氧化锌的工业流程如图所示,回答下列问题:
生产高纯氧化锌的工业流程如图所示,回答下列问题:

已知: 微溶于水而生成亚砷酸
微溶于水而生成亚砷酸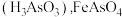 和
和 难溶于水。
难溶于水。
(1)基态 原子核外价层电子轨道表达式为
原子核外价层电子轨道表达式为______ , 中
中 的化合价为
的化合价为______ 。
(2)“浸出”过程中 足量,则生成的主要配离子的化学式为
足量,则生成的主要配离子的化学式为______ ;增大浸出率可采取的措施是______  写出两条
写出两条 。
。
(3)“除砷”过程中, 作氧化剂
作氧化剂 溶液呈酸性
溶液呈酸性 ,发生反应的离子方程式为
,发生反应的离子方程式为______ 。
(4)“除重金属”过程中加入 后
后 在溶液中的残留浓度为
在溶液中的残留浓度为 ,此时
,此时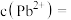
______ 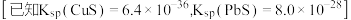 。
。
(5)“沉锌”前锌元素以 存在,写出“沉锌”的化学方程式
存在,写出“沉锌”的化学方程式______ 。
(6)流程中可循环利用的物质有 、
、______ 、______  填化学式
填化学式 。
。
 主要成分为
主要成分为 ,含
,含 及铅、铜、镉的氧化物
及铅、铜、镉的氧化物 生产高纯氧化锌的工业流程如图所示,回答下列问题:
生产高纯氧化锌的工业流程如图所示,回答下列问题:
已知:
 微溶于水而生成亚砷酸
微溶于水而生成亚砷酸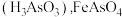 和
和 难溶于水。
难溶于水。(1)基态
 原子核外价层电子轨道表达式为
原子核外价层电子轨道表达式为 中
中 的化合价为
的化合价为(2)“浸出”过程中
 足量,则生成的主要配离子的化学式为
足量,则生成的主要配离子的化学式为 写出两条
写出两条 。
。(3)“除砷”过程中,
 作氧化剂
作氧化剂 溶液呈酸性
溶液呈酸性 ,发生反应的离子方程式为
,发生反应的离子方程式为(4)“除重金属”过程中加入
 后
后 在溶液中的残留浓度为
在溶液中的残留浓度为 ,此时
,此时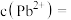
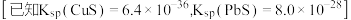 。
。(5)“沉锌”前锌元素以
 存在,写出“沉锌”的化学方程式
存在,写出“沉锌”的化学方程式(6)流程中可循环利用的物质有
 、
、 填化学式
填化学式 。
。
您最近一年使用:0次
2 . 下列实验操作、现象和所得结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向盛有2mL0.1mol。L-1AgNO3溶液的试管中滴加4滴0.1mol。L-1NaCl溶液;振荡试管,然后再向其中滴加4滴0.1mol·L-1KI溶液 | 先生成白色沉淀,后沉淀由白色变为黄色 | Ksp(AgCl)>Ksp(AgI) |
| B | 在稀硫酸中加入少量Cu2O(s) | 溶液由无色变为蓝色,并有红色固体生成 | 反应中Cu2O既作氧化剂又作还原剂 |
| C | 在灼热木炭中加入浓硫酸,将生成的气体依次通过品红溶液、饱和NaHCO3溶液、澄清石灰水 | 品红溶液视色,澄清石灰水变浑浊 | 浓硫酸和木炭反应产生SO2和CO2气体 |
| D | 向CuSO4溶液中滴加浓氨水至过量 | 先生成蓝色沉淀,后逐渐溶解 | Cu(OH)2是两性氢氧化物 |
A. | B. | C. | D. |
您最近一年使用:0次
解题方法
3 . 氨硼烷 是一种新型储氢材料,分子中与
是一种新型储氢材料,分子中与 原子相连的
原子相连的 原子呈正电性,与
原子呈正电性,与 原子相连的
原子相连的 原子呈负催化剂电性。氨硼烷与水发生如下反应:
原子呈负催化剂电性。氨硼烷与水发生如下反应: 。下列说法正确的是
。下列说法正确的是
 是一种新型储氢材料,分子中与
是一种新型储氢材料,分子中与 原子相连的
原子相连的 原子呈正电性,与
原子呈正电性,与 原子相连的
原子相连的 原子呈负催化剂电性。氨硼烷与水发生如下反应:
原子呈负催化剂电性。氨硼烷与水发生如下反应: 。下列说法正确的是
。下列说法正确的是A.中子数为 的 的 原子: 原子: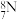 |
B.基态原子第一电离能由大到小: |
C.反应前后 原子均采用 原子均采用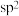 杂化 杂化 |
| D.氨硼烷中两种氢原子之间存在相互吸引作用 |
您最近一年使用:0次
名校
4 . 下列反应的离子方程式正确的是
| A.硝酸钡溶液中通入SO2:Ba2++SO2+H2O=BaSO3↓+2H+ |
B.Ca(HCO3)2溶液中加少量NaOH溶液:Ca2++ +OH-=CaCO3↓+H2O +OH-=CaCO3↓+H2O |
C.饱和Na2CO3溶液中通入过量CO2: +CO2+H2O=2 +CO2+H2O=2 |
D.硫酸铜溶液中加过量浓氨水:Cu2++2NH3⋅H2O=Cu(OH)2↓+2 |
您最近一年使用:0次
名校
5 . 用氨水吸收硫酸工厂尾气中的SO2,发生的反应为:2NH3·H2O+SO2=(NH4)2SO3+H2O。下列说法不正确的是
| A.SO2是极性分子 |
| B.NH3中氮原子的杂化方式为sp3杂化 |
| C.(NH4)2SO3晶体中含离子键、共价键、配位键 |
| D.H2O分子间存在氢键所以较稳定 |
您最近一年使用:0次
名校
6 . 二氯化二硫(S2Cl2)可用作橡胶工业的硫化剂,它的分子结构与H2O2相似,下列说法错误的是
| A.S2Cl2是含有极性键的非极性分子 |
| B.SO2中S的VSEPR模型为平面三角形 |
| C.键角:H2O<SO2 |
| D.沸点:H2O>HCl |
您最近一年使用:0次
名校
7 . 硫代硫酸钠(Na2S2O3)是硫酸钠中一个氧原子被硫原子取代的产物。硫代硫酸钠晶体(Na2S2O3·5H2O,M=248g⋅mol−1)易溶于水,难溶于乙醇,在酸性环境中易分解。
Ⅰ.制备a2S2O3·5H2O
方法一:亚硫酸钠法。反应原理:S+Na2SO3=Na2S2O3
实验步骤:称取一定量的Na2SO3固体于烧杯中,溶于煮沸过的蒸馏水。另取过量的硫粉,加入少量乙醇充分搅拌后,加到上述Na2SO3溶液中。水浴加热,微沸,反应后趁热过滤。滤液蒸发浓缩、冷却结晶析出Na2S2O3·5H2O晶体。
(1) 中心硫原子的杂化方式为
中心硫原子的杂化方式为___________ 。
(2)使用煮沸过的蒸馏水配制Na2SO3溶液的目的是___________ 。
方法二:硫化碱法。装置如图所示。
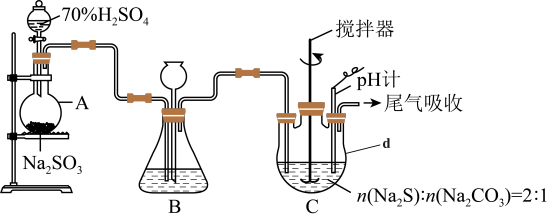
(3)①仪器d的名称为___________ 。
②装置A中发生反应的化学方程式为___________ 。
③装置C中,将Na2S和Na2CO3以2:1的物质的量之比配成溶液再通入SO2,便可制得Na2S2O3和CO2.该反应的化学方程式为___________ 。
④实验过程中,为了保证Na2S2O3·5H2O的产量,实验中通入的SO2不能过量,原因是_________ 。
Ⅱ.Na2S2O3的应用
(4)设计以下实验测定粗产品中Na2S2O3·5H2O的含量:
步骤1:准确称取8.0000g样品溶于水,配成100mL溶液。
步骤2:准确称取0.294gK2Cr2O7固体于碘量瓶中,加入20mL蒸馏水溶解,再加入10mL2mol⋅L−1H2SO4和20mL10%KI溶液使铬元素完全转化为Cr3+,加水稀释至100mL。
步骤3:向碘量瓶中加入1mL某溶液作指示剂,用待测Na2S2O3溶液滴定碘量瓶中溶液至滴定终点,消耗Na2S2O3溶液20.00mL。(已知:I2+2 =2I−+
=2I−+ )
)
①步骤3中向碘量瓶中加入的指示剂是___________ 。
②由计算可得Na2S2O3·5H2O的纯度为___________ 。
Ⅰ.制备a2S2O3·5H2O
方法一:亚硫酸钠法。反应原理:S+Na2SO3=Na2S2O3
实验步骤:称取一定量的Na2SO3固体于烧杯中,溶于煮沸过的蒸馏水。另取过量的硫粉,加入少量乙醇充分搅拌后,加到上述Na2SO3溶液中。水浴加热,微沸,反应后趁热过滤。滤液蒸发浓缩、冷却结晶析出Na2S2O3·5H2O晶体。
(1)
 中心硫原子的杂化方式为
中心硫原子的杂化方式为(2)使用煮沸过的蒸馏水配制Na2SO3溶液的目的是
方法二:硫化碱法。装置如图所示。

(3)①仪器d的名称为
②装置A中发生反应的化学方程式为
③装置C中,将Na2S和Na2CO3以2:1的物质的量之比配成溶液再通入SO2,便可制得Na2S2O3和CO2.该反应的化学方程式为
④实验过程中,为了保证Na2S2O3·5H2O的产量,实验中通入的SO2不能过量,原因是
Ⅱ.Na2S2O3的应用
(4)设计以下实验测定粗产品中Na2S2O3·5H2O的含量:
步骤1:准确称取8.0000g样品溶于水,配成100mL溶液。
步骤2:准确称取0.294gK2Cr2O7固体于碘量瓶中,加入20mL蒸馏水溶解,再加入10mL2mol⋅L−1H2SO4和20mL10%KI溶液使铬元素完全转化为Cr3+,加水稀释至100mL。
步骤3:向碘量瓶中加入1mL某溶液作指示剂,用待测Na2S2O3溶液滴定碘量瓶中溶液至滴定终点,消耗Na2S2O3溶液20.00mL。(已知:I2+2
 =2I−+
=2I−+ )
)①步骤3中向碘量瓶中加入的指示剂是
②由计算可得Na2S2O3·5H2O的纯度为
您最近一年使用:0次
名校
解题方法
8 . 下列方程式与所给事实不相符的是
A.硫酸铜溶液中加少量氨水:Cu2++2NH3·H2O=Cu(OH)2↓+2 |
B.氢气燃烧热为285.8kJ/mol:H2(g)+ O2(g)=H2O(l) ΔH=−285.8kJ/mol O2(g)=H2O(l) ΔH=−285.8kJ/mol |
| C.用KSCN溶液检验Fe3+:Fe3++3SCN−=Fe(SCN)3↓ |
| D.加热CuCl2溶液,溶液变成黄绿色:[Cu(H2O)4]2++4Cl−⇌[CuCl4]2−+4H2O ΔH>0 |
您最近一年使用:0次
名校
解题方法
9 . 关于第Ⅳ 族的元素——碳(
族的元素——碳( )、硅(
)、硅( )、锗(
)、锗( )、锡(
)、锡( )和铅(
)和铅( ),它们可形成许多结构各异的物质。回答下列问题:
),它们可形成许多结构各异的物质。回答下列问题:
(1)基态 原子的价电子轨道表示式为
原子的价电子轨道表示式为______ ,有______ 种不同运动状态的电子。
(2) 中
中 原子的杂化类型是
原子的杂化类型是______ , 的空间结构是
的空间结构是______ 。
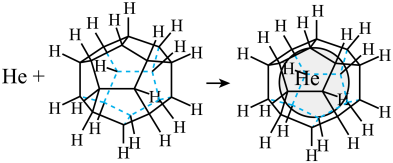
(3)1999年,科学家成功地将一个 原子“装入”了一个
原子“装入”了一个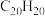 的空腔内,得到了“世界上最小的氦气球”(如图所示,产物记为
的空腔内,得到了“世界上最小的氦气球”(如图所示,产物记为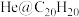 )。则
)。则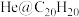 中,
中, 与
与 之间的作用力为
之间的作用力为______ 。
(4)第Ⅳ 族的金属元素可形成
族的金属元素可形成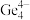 、
、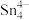 和
和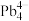 等阴离子,根据等电子体原理判断,
等阴离子,根据等电子体原理判断,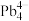 中的键角为
中的键角为______ 。
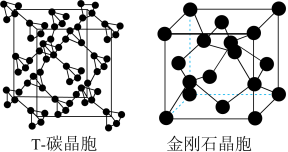
(5)科研团队通过皮秒激光照射悬浮在甲醇溶液中的多臂碳纳米管合成 碳,
碳, 碳的晶体结构可以看成金刚石晶体中每个碳原子被一个由四个碳原子组成的正四面体结构单元取代,
碳的晶体结构可以看成金刚石晶体中每个碳原子被一个由四个碳原子组成的正四面体结构单元取代,
碳的密度约为金刚石的一半 , 碳晶体的晶胞、金刚石的晶胞如图所示。则
碳晶体的晶胞、金刚石的晶胞如图所示。则 碳晶胞的棱长是金刚石晶胞棱长的
碳晶胞的棱长是金刚石晶胞棱长的______ 倍。
(6) 与碱金属形成的盐具有特别的意义,他们能在低温时转变为超导材料。
与碱金属形成的盐具有特别的意义,他们能在低温时转变为超导材料。 与
与 形成的一种超导材料的晶胞如图所示,图中白球表示
形成的一种超导材料的晶胞如图所示,图中白球表示 ,黑球表示钾原子。
,黑球表示钾原子。
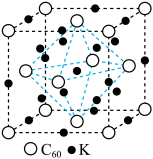
①该材料的化学式是____________ 。
②已知晶胞边长为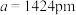 ,则该超导材料的理论密度为
,则该超导材料的理论密度为
____________  (写出表达式)。
(写出表达式)。
 族的元素——碳(
族的元素——碳( )、硅(
)、硅( )、锗(
)、锗( )、锡(
)、锡( )和铅(
)和铅( ),它们可形成许多结构各异的物质。回答下列问题:
),它们可形成许多结构各异的物质。回答下列问题:(1)基态
 原子的价电子轨道表示式为
原子的价电子轨道表示式为(2)
 中
中 原子的杂化类型是
原子的杂化类型是 的空间结构是
的空间结构是(3)1999年,科学家成功地将一个
 原子“装入”了一个
原子“装入”了一个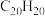 的空腔内,得到了“世界上最小的氦气球”(如图所示,产物记为
的空腔内,得到了“世界上最小的氦气球”(如图所示,产物记为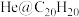 )。则
)。则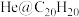 中,
中, 与
与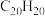 之间的作用力为
之间的作用力为
(4)第Ⅳ
 族的金属元素可形成
族的金属元素可形成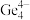 、
、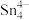 和
和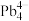 等阴离子,根据等电子体原理判断,
等阴离子,根据等电子体原理判断,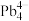 中的键角为
中的键角为(5)科研团队通过皮秒激光照射悬浮在甲醇溶液中的多臂碳纳米管合成
 碳,
碳, 碳的晶体结构可以看成金刚石晶体中每个碳原子被一个由四个碳原子组成的正四面体结构单元取代,
碳的晶体结构可以看成金刚石晶体中每个碳原子被一个由四个碳原子组成的正四面体结构单元取代,
 碳晶体的晶胞、金刚石的晶胞如图所示。则
碳晶体的晶胞、金刚石的晶胞如图所示。则 碳晶胞的棱长是金刚石晶胞棱长的
碳晶胞的棱长是金刚石晶胞棱长的
(6)
 与碱金属形成的盐具有特别的意义,他们能在低温时转变为超导材料。
与碱金属形成的盐具有特别的意义,他们能在低温时转变为超导材料。 与
与 形成的一种超导材料的晶胞如图所示,图中白球表示
形成的一种超导材料的晶胞如图所示,图中白球表示 ,黑球表示钾原子。
,黑球表示钾原子。
①该材料的化学式是
②已知晶胞边长为
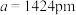 ,则该超导材料的理论密度为
,则该超导材料的理论密度为
 (写出表达式)。
(写出表达式)。
您最近一年使用:0次
2024-02-14更新
|
229次组卷
|
2卷引用:重庆市西南大学附中2023-2024学年高二上学期期末考试化学试题
名校
解题方法
10 . 下列有关化学用语表示正确的是
A.HClO的电子式: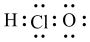 |
| B.基态As原子的电子排布式:[Ar]4s24p3 |
C.O3分子结构的空间模型: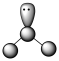 |
D.顺聚异戊二烯的结构简式: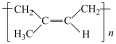 |
您最近一年使用:0次



