名校
1 . 下列说法错误的是
| A.CO2与SiO2的键角相等 |
| B.SiH4、CO2均是由极性键构成的非极性分子 |
| C.HCNO中元素的电负性:O>N>C>H |
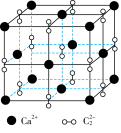
| D.CaC2晶胞如图所示,Ca2+的配位数为6 |
您最近一年使用:0次
名校
2 . 下列说法中不正确的是
| A.同一基态原子中,4px、4py、4pz轨道上电子的能量相同 |
| B.s-s轨道可以形成的σ键,s-p轨道也可以形成的σ键, |
| C.某原子价电子排布式是6s26p2,则该元素位于元素周期表的p区 |
| D.CH4中4个C-H键的键长、键能不完全相同 |
您最近一年使用:0次
名校
3 . 以下性质的比较中,正确的是
| A.沸点高低:HCl<HBr<HI<HF | B.晶格能大小:NaI>NaBr>NaCl>NaF |
| C.共价键的键长:C-C>C-Si>Si-Si | D.单质的熔点:Li<Na<K<Rb |
您最近一年使用:0次
名校
4 . 下列说法正确的是
A.键角: |
B.三氧化硫有单分子气体 和三聚分子固体 和三聚分子固体 ( ( )两种存在形式,两种形式中S原子的杂化轨道类型相同 )两种存在形式,两种形式中S原子的杂化轨道类型相同 |
C. 与 与 互为等电子体,1mol 互为等电子体,1mol  中含有的 中含有的 键数目为2 键数目为2 |
D. 、 、 、 、 分子的空间构型为正四面体形,键角都相同 分子的空间构型为正四面体形,键角都相同 |
您最近一年使用:0次
名校
解题方法
5 . 分子人工光合作用的光捕获原理如图所示,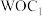 是水氧化催化剂WOC在水氧化过程中产生的中间体,
是水氧化催化剂WOC在水氧化过程中产生的中间体,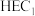 是析氢催化剂HEC在析氢过程中产生的中间体。
是析氢催化剂HEC在析氢过程中产生的中间体。
(1)与Fe元素同周期,基态原子有2个未成对电子的金属元素有___________ 种,下列状态的铁中,电离最外层一个电子所需能量最大的是___________ (填选项)。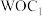 中通过螯合作用形成的配位键有
中通过螯合作用形成的配位键有___________ mol。
(3)在多原子分子中有相互平行的p轨道,它们连贯、重叠在一起,构成一个整体,p电子在多个原子间运动,像这样不局限在两个原子之间的 键称为离域
键称为离域 键,如苯分子中的离域
键,如苯分子中的离域 键可表示为
键可表示为 。N元素形成的两种微粒
。N元素形成的两种微粒 、
、 中,
中, 中的离域
中的离域 键可表示为
键可表示为___________ , 、
、 的键角由大到小的顺序为
的键角由大到小的顺序为_________________________________ 。
(4)水催化氧化是“分子人工光合作用”的关键步骤。水的晶体有普通冰和重冰等不同类型。普通冰的晶胞结构与水分子间的氢键如图甲、乙所示。晶胞参数分别为a pm、c pm,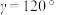 ;标注为1、2、3的氧原子在Z轴的分数坐标分别为:0.375c、0.5c、0.875c。
;标注为1、2、3的氧原子在Z轴的分数坐标分别为:0.375c、0.5c、0.875c。___________ pm。
②普通冰晶体的密度为______________________  (列出数学表达式,不必计算出结果)。
(列出数学表达式,不必计算出结果)。
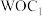 是水氧化催化剂WOC在水氧化过程中产生的中间体,
是水氧化催化剂WOC在水氧化过程中产生的中间体,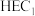 是析氢催化剂HEC在析氢过程中产生的中间体。
是析氢催化剂HEC在析氢过程中产生的中间体。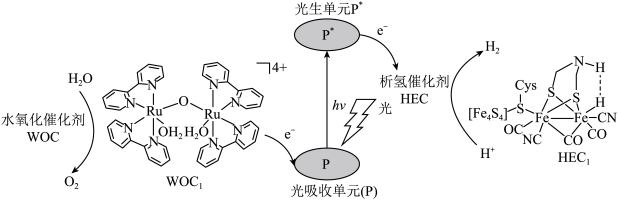
(1)与Fe元素同周期,基态原子有2个未成对电子的金属元素有
A. 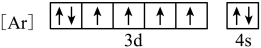
B.
C. 
D.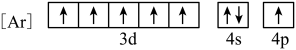
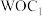 中通过螯合作用形成的配位键有
中通过螯合作用形成的配位键有(3)在多原子分子中有相互平行的p轨道,它们连贯、重叠在一起,构成一个整体,p电子在多个原子间运动,像这样不局限在两个原子之间的
 键称为离域
键称为离域 键,如苯分子中的离域
键,如苯分子中的离域 键可表示为
键可表示为 。N元素形成的两种微粒
。N元素形成的两种微粒 、
、 中,
中, 中的离域
中的离域 键可表示为
键可表示为 、
、 的键角由大到小的顺序为
的键角由大到小的顺序为(4)水催化氧化是“分子人工光合作用”的关键步骤。水的晶体有普通冰和重冰等不同类型。普通冰的晶胞结构与水分子间的氢键如图甲、乙所示。晶胞参数分别为a pm、c pm,
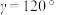 ;标注为1、2、3的氧原子在Z轴的分数坐标分别为:0.375c、0.5c、0.875c。
;标注为1、2、3的氧原子在Z轴的分数坐标分别为:0.375c、0.5c、0.875c。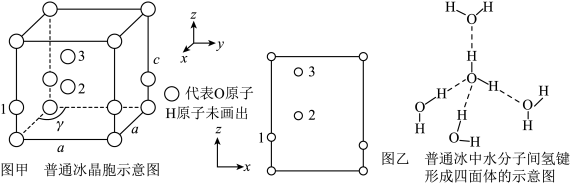
②普通冰晶体的密度为
 (列出数学表达式,不必计算出结果)。
(列出数学表达式,不必计算出结果)。
您最近一年使用:0次
名校
6 . 下列事实不能用键能的大小来解释的是
| A.N元素的电负性较大,但N2的化学性质很稳定 |
| B.F2比O2更容易与H₂反应 |
| C.HF、HCl、HBr、HI的稳定性逐渐减弱 |
| D.稀有气体一般难发生反应 |
您最近一年使用:0次
2024-04-26更新
|
57次组卷
|
2卷引用:福建省福州第二中学2023-2024学年高二下学期4月期中考试化学试题
名校
7 . 亚硝酰硫酸( )是一种浅黄色液体,遇水易分解,溶于浓硫酸,主要用于染料、医药领域的重氮化反应。实验室用如图装置(夹持装置略)制备少量
)是一种浅黄色液体,遇水易分解,溶于浓硫酸,主要用于染料、医药领域的重氮化反应。实验室用如图装置(夹持装置略)制备少量 。
。

已知:亚硝酸在溶液中很不稳定,很快分解为 和NO
和NO
(1)装置A中盛装浓硫酸的仪器名称是_____ ,装置D最好选用_____ (填序号)。
a.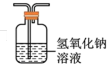 b.
b.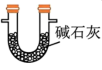 c.
c.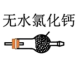 d.
d.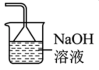
(2)装置C中浓 与
与 在浓
在浓 作用下反应制得
作用下反应制得 。
。
①C中“冷水”的温度一般控制在20℃,装置C中温度过高产率降低的原因是_____ 。
②开始通 时,反应缓慢,待生成少量
时,反应缓慢,待生成少量 后,温度变化不大,但反应速率明显加快,其原因是
后,温度变化不大,但反应速率明显加快,其原因是_____ 。
③请写出亚硝酰硫酸( )遇水分解时发生反应的化学方程式
)遇水分解时发生反应的化学方程式_____ 。
(3)测定亚硝酰硫酸 的纯度:准确称取1.500g产品放入250mL的碘量瓶中,加入
的纯度:准确称取1.500g产品放入250mL的碘量瓶中,加入 、60.00mL的
、60.00mL的 标准溶液和
标准溶液和 溶液,然后摇匀。用
溶液,然后摇匀。用 草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.0mL。
草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.0mL。
已知: ;
;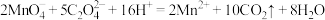 。
。
达到滴定终点时的颜色变化为_____ 变为_____ ,亚硝酰硫酸的纯度为_____ (精确到0.1%)。
(4)亚硝酰硫酸组成元素中,N、O、S第一电离能由大到小的顺序是_____ ,比较亚硝酰正离子 与亚硝酸根
与亚硝酸根 的键角大小:
的键角大小:
_____  (选填“>”、“<”或“=”),从物质结构的角度简要解释原因
(选填“>”、“<”或“=”),从物质结构的角度简要解释原因_____ 。
 )是一种浅黄色液体,遇水易分解,溶于浓硫酸,主要用于染料、医药领域的重氮化反应。实验室用如图装置(夹持装置略)制备少量
)是一种浅黄色液体,遇水易分解,溶于浓硫酸,主要用于染料、医药领域的重氮化反应。实验室用如图装置(夹持装置略)制备少量 。
。
已知:亚硝酸在溶液中很不稳定,很快分解为
 和NO
和NO(1)装置A中盛装浓硫酸的仪器名称是
a.
 b.
b. c.
c. d.
d.
(2)装置C中浓
 与
与 在浓
在浓 作用下反应制得
作用下反应制得 。
。①C中“冷水”的温度一般控制在20℃,装置C中温度过高产率降低的原因是
②开始通
 时,反应缓慢,待生成少量
时,反应缓慢,待生成少量 后,温度变化不大,但反应速率明显加快,其原因是
后,温度变化不大,但反应速率明显加快,其原因是③请写出亚硝酰硫酸(
 )遇水分解时发生反应的化学方程式
)遇水分解时发生反应的化学方程式(3)测定亚硝酰硫酸
 的纯度:准确称取1.500g产品放入250mL的碘量瓶中,加入
的纯度:准确称取1.500g产品放入250mL的碘量瓶中,加入 、60.00mL的
、60.00mL的 标准溶液和
标准溶液和 溶液,然后摇匀。用
溶液,然后摇匀。用 草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.0mL。
草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.0mL。已知:
 ;
;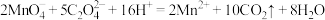 。
。达到滴定终点时的颜色变化为
(4)亚硝酰硫酸组成元素中,N、O、S第一电离能由大到小的顺序是
 与亚硝酸根
与亚硝酸根 的键角大小:
的键角大小:
 (选填“>”、“<”或“=”),从物质结构的角度简要解释原因
(选填“>”、“<”或“=”),从物质结构的角度简要解释原因
您最近一年使用:0次
名校
8 . 下列关于物质的结构或性质及解释均正确的是
| 选项 | 物质的结构或性质 | 解释 |
| A | 键角: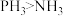 | N的电负性大于P |
| B | 稳定性: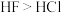 |  分子间氢键强于 分子间氢键强于 分子间作用力 分子间作用力 |
| C | 熔点:碳化硅>金刚石 |  键的键能大于 键的键能大于 键的键能 键的键能 |
| D |  在 在 中的溶解度比在水中的大 中的溶解度比在水中的大 |  和 和 都是非极性分子, 都是非极性分子, 是极性分子 是极性分子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-01更新
|
216次组卷
|
3卷引用:福建省厦门市松柏中学2023-2024学年高三上学期期中考试化学试题
解题方法
9 . 门捷列夫最早预言了具有半导体特性类硅元素锗(32Ge),工业上用精硫锗矿(主要成分为GeS2)制取高纯度锗,其工艺流程如图所示:
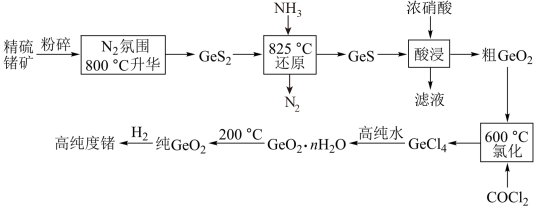
已知:①硅和锗是同主族相邻元素,结构和性质类似;
②GeO2∙nH2O在5.3mol∙L-1的盐酸中溶解度最小。
(1)基态锗原子的价层电子排布式为___________ ,晶体锗的晶体类型是___________ 。
(2)800℃,使精硫锗矿在N2氛围中升华的原因:___________ 。
(3)还原时发生反应: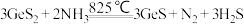 ,比较键角:NH3
,比较键角:NH3___________ H2S(填“>”“<”或“=”)。
(4)酸浸时温度不能过高的原因:___________ 。
(5)氯化除生成GeCl4外,反应还生成一种酸性气体,写出相应的化学方程式:___________ 。
(6) GeCl4水解得到GeO2∙nH2O,该步骤高纯水不能过量,原因是___________ 。

已知:①硅和锗是同主族相邻元素,结构和性质类似;
②GeO2∙nH2O在5.3mol∙L-1的盐酸中溶解度最小。
(1)基态锗原子的价层电子排布式为
(2)800℃,使精硫锗矿在N2氛围中升华的原因:
(3)还原时发生反应:
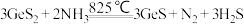 ,比较键角:NH3
,比较键角:NH3(4)酸浸时温度不能过高的原因:
(5)氯化除生成GeCl4外,反应还生成一种酸性气体,写出相应的化学方程式:
(6) GeCl4水解得到GeO2∙nH2O,该步骤高纯水不能过量,原因是
您最近一年使用:0次
真题
名校
10 . W、X、Y、Z为原子序数依次增加的同一短周期元素,其中X、Y、Z相邻,W的核外电子数与X的价层电子数相等, 是氧化性最强的单质,4种元素可形成离子化合物
是氧化性最强的单质,4种元素可形成离子化合物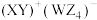 。下列说法正确的是
。下列说法正确的是
 是氧化性最强的单质,4种元素可形成离子化合物
是氧化性最强的单质,4种元素可形成离子化合物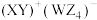 。下列说法正确的是
。下列说法正确的是A.分子的极性: | B.第一电离能:X<Y<Z |
C.氧化性: | D.键能: |
您最近一年使用:0次
2023-06-14更新
|
9033次组卷
|
13卷引用:福建省漳州市 十校联盟2023-2024 学年高三上学期期中质量检测联考化学试卷
福建省漳州市 十校联盟2023-2024 学年高三上学期期中质量检测联考化学试卷福建省福州第三中学2023-2024学年高三下学期第十六次检测(三模)化学试题2023年高考湖北卷化学真题(已下线)专题07 元素周期表与元素周期律(已下线)T6-元素周期表及周期律(已下线)专题07 元素周期表与元素周期律(已下线)专题07 元素周期表与元素周期律江西省龙南中学2022-2023学年高二下学期6月期末考试化学试题(已下线)考点07 元素周期律和元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题12 物质结构与性质(选择题)-2023年高考化学真题题源解密(新高考专用)(已下线)专题08 物质结构与性质 元素推断-2023年高考化学真题题源解密(全国通用)新疆生产建设兵团第二中学2023-2024学年高三上学期12月月考化学题湖南省邵阳市第二中学2023-2024学年高二下学期入学考试化学试题



