1 . 超纯 是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯
是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯 方面取得了显著成果,工业上以粗镓为原料,制备超纯
方面取得了显著成果,工业上以粗镓为原料,制备超纯 的工艺流程如下:
的工艺流程如下: 的化学性质和
的化学性质和 相似,
相似, 的熔点为
的熔点为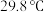 ;
;
② (乙醚)和
(乙醚)和 (三正辛胺)在上述流程中可作为配体;
(三正辛胺)在上述流程中可作为配体;
③相关物质的沸点:
回答下列问题:
(1)晶体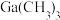 的晶体类型是
的晶体类型是_______ ;
(2)“电解精炼”装置如图所示,电解池温度控制在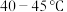 的原因是
的原因是_______ ,阴极的电极反应式为_______ ;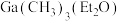 ”工序中的产物还包括
”工序中的产物还包括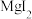 和
和 ,写出该反应的化学方程式:
,写出该反应的化学方程式:_______ ;
(4)“残渣”经纯水处理,能产生可燃性气体,该气体主要成分是_______ ;
(5)下列说法错误的是_______;
(6)直接分解 不能制备超纯
不能制备超纯 ,而本流程采用“配体交换”工艺制备超纯
,而本流程采用“配体交换”工艺制备超纯 的理由是
的理由是_______ ;
(7)比较分子中的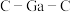 键角大小:
键角大小:
_______  (填“>”“<”或“=”),其原因是
(填“>”“<”或“=”),其原因是_______ 。
 是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯
是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯 方面取得了显著成果,工业上以粗镓为原料,制备超纯
方面取得了显著成果,工业上以粗镓为原料,制备超纯 的工艺流程如下:
的工艺流程如下: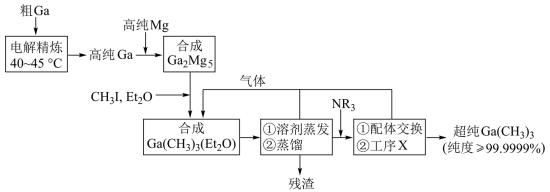
 的化学性质和
的化学性质和 相似,
相似, 的熔点为
的熔点为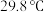 ;
;②
 (乙醚)和
(乙醚)和 (三正辛胺)在上述流程中可作为配体;
(三正辛胺)在上述流程中可作为配体;③相关物质的沸点:
| 物质 | 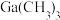 |  | 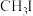 | 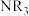 |
沸点/ | 55.7 | 34.6 | 42.4 | 365.8 |
(1)晶体
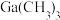 的晶体类型是
的晶体类型是(2)“电解精炼”装置如图所示,电解池温度控制在
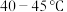 的原因是
的原因是
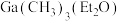 ”工序中的产物还包括
”工序中的产物还包括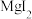 和
和 ,写出该反应的化学方程式:
,写出该反应的化学方程式:(4)“残渣”经纯水处理,能产生可燃性气体,该气体主要成分是
(5)下列说法错误的是_______;
A.流程中 得到了循环利用 得到了循环利用 |
B.流程中,“合成 ”至“工序X”需在无水无氧的条件下进行 ”至“工序X”需在无水无氧的条件下进行 |
C.“工序X”的作用是解配 ,并蒸出 ,并蒸出 |
D.用核磁共振氢谱不能区分 和 和 |
 不能制备超纯
不能制备超纯 ,而本流程采用“配体交换”工艺制备超纯
,而本流程采用“配体交换”工艺制备超纯 的理由是
的理由是(7)比较分子中的
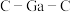 键角大小:
键角大小:
 (填“>”“<”或“=”),其原因是
(填“>”“<”或“=”),其原因是
您最近一年使用:0次
2023-06-16更新
|
10014次组卷
|
11卷引用:2023年高考湖南卷化学真题
2023年高考湖南卷化学真题(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题(已下线)2023年湖南卷高考真题变式题(工业流程题)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)福建省厦门市 第一中学2023-2024上学期高三上学期12月考化学试题福建省漳州市华安县第一中学2023-2024学年高三上学期12月月考化学试题(已下线)题型四 无机化工流程题解题策略-备战2024年高考化学答题技巧与模板构建
2 . 卤素可形成许多结构和性质特殊的化合物。回答下列问题:
(1)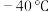 时,
时, 与冰反应生成
与冰反应生成 和
和 。常温常压下,
。常温常压下, 为无色气体,固态
为无色气体,固态 的晶体类型为
的晶体类型为_____ , 水解反应的产物为
水解反应的产物为_____ (填化学式)。
(2) 中心原子为
中心原子为 ,
, 中心原子为
中心原子为 ,二者均为
,二者均为 形结构,但
形结构,但 中存在大
中存在大 键
键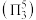 。
。 中
中 原子的轨道杂化方式
原子的轨道杂化方式_____ ;为 键角
键角_____  键角(填“>”“ <”或“=”)。比较
键角(填“>”“ <”或“=”)。比较 与
与 中
中 键的键长并说明原因
键的键长并说明原因_____ 。
(3)一定条件下, 和
和 反应生成
反应生成 和化合物
和化合物 。已知
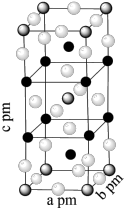
。已知 属于四方晶系,晶胞结构如图所示(晶胞参数
属于四方晶系,晶胞结构如图所示(晶胞参数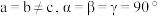 ),其中
),其中 化合价为
化合价为 。上述反应的化学方程式为
。上述反应的化学方程式为_____ 。若阿伏伽德罗常数的值为 ,化合物
,化合物 的密度
的密度
_____  (用含
(用含 的代数式表示)。
的代数式表示)。
(1)
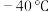 时,
时, 与冰反应生成
与冰反应生成 和
和 。常温常压下,
。常温常压下, 为无色气体,固态
为无色气体,固态 的晶体类型为
的晶体类型为 水解反应的产物为
水解反应的产物为(2)
 中心原子为
中心原子为 ,
, 中心原子为
中心原子为 ,二者均为
,二者均为 形结构,但
形结构,但 中存在大
中存在大 键
键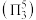 。
。 中
中 原子的轨道杂化方式
原子的轨道杂化方式 键角
键角 键角(填“>”“ <”或“=”)。比较
键角(填“>”“ <”或“=”)。比较 与
与 中
中 键的键长并说明原因
键的键长并说明原因(3)一定条件下,
 和
和 反应生成
反应生成 和化合物
和化合物 。已知
。已知 属于四方晶系,晶胞结构如图所示(晶胞参数
属于四方晶系,晶胞结构如图所示(晶胞参数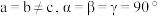 ),其中
),其中 化合价为
化合价为 。上述反应的化学方程式为
。上述反应的化学方程式为 ,化合物
,化合物 的密度
的密度
 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2023-06-19更新
|
10414次组卷
|
10卷引用:2023年高考山东卷化学真题
2023年高考山东卷化学真题(已下线)2023年高考山东卷化学真题变式题(结构与性质)(已下线)专题20 结构与性质(已下线)专题20 结构与性质(已下线)第11讲 氯气和卤族元素(已下线)专题17 物质结构与性质综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题16 物质结构与性质综合题-2023年高考化学真题题源解密(全国通用)(已下线)第20讲化学键(已下线)考点14 氯及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用) 河南省南阳市第一中学校2024届高三上学期阶段检测化学试题(12月)
3 . 聚苯乙烯是一类重要的高分子材料,可通过苯乙烯聚合制得。
Ⅰ.苯乙烯的制备
(1)已知下列反应的热化学方程式:
①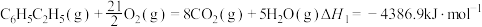
②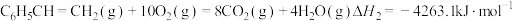
③
计算反应④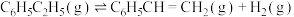 的
的
_______  ;
;
(2)在某温度、 下,向反应器中充入
下,向反应器中充入 气态乙苯发生反应④,其平衡转化率为50%,欲将平衡转化率提高至75%,需要向反应器中充入
气态乙苯发生反应④,其平衡转化率为50%,欲将平衡转化率提高至75%,需要向反应器中充入_______  水蒸气作为稀释气(计算时忽略副反应);
水蒸气作为稀释气(计算时忽略副反应);
(3)在 、
、 下,以水蒸气作稀释气。
下,以水蒸气作稀释气。 作催化剂,乙苯除脱氢生成苯乙烯外,还会发生如下两个副反应:
作催化剂,乙苯除脱氢生成苯乙烯外,还会发生如下两个副反应:
⑤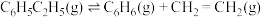
⑥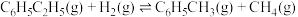
以上反应体系中,芳香烃产物苯乙烯、苯和甲苯的选择性S( )随乙苯转化率的变化曲线如图所示,其中曲线b代表的产物是
)随乙苯转化率的变化曲线如图所示,其中曲线b代表的产物是_______ ,理由是_______ ; 的描述错误的是_______;
的描述错误的是_______;
Ⅱ.苯乙烯的聚合
苯乙烯聚合有多种方法,其中一种方法的关键步骤是某 (Ⅰ)的配合物促进
(Ⅰ)的配合物促进 (引发剂,X表示卤素)生成自由基
(引发剂,X表示卤素)生成自由基 ,实现苯乙烯可控聚合。
,实现苯乙烯可控聚合。
(5)引发剂 中活性最高的是
中活性最高的是_______ ;
(6)室温下,① 在配体L的水溶液中形成
在配体L的水溶液中形成 ,其反应平衡常数为K;②
,其反应平衡常数为K;② 在水中的溶度积常数为
在水中的溶度积常数为 。由此可知,
。由此可知, 在配体L的水溶液中溶解反应的平衡常数为
在配体L的水溶液中溶解反应的平衡常数为_______ (所有方程式中计量系数关系均为最简整数比)。
Ⅰ.苯乙烯的制备
(1)已知下列反应的热化学方程式:
①
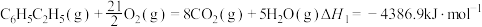
②
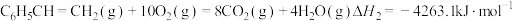
③

计算反应④
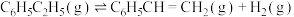 的
的
 ;
;(2)在某温度、
 下,向反应器中充入
下,向反应器中充入 气态乙苯发生反应④,其平衡转化率为50%,欲将平衡转化率提高至75%,需要向反应器中充入
气态乙苯发生反应④,其平衡转化率为50%,欲将平衡转化率提高至75%,需要向反应器中充入 水蒸气作为稀释气(计算时忽略副反应);
水蒸气作为稀释气(计算时忽略副反应);(3)在
 、
、 下,以水蒸气作稀释气。
下,以水蒸气作稀释气。 作催化剂,乙苯除脱氢生成苯乙烯外,还会发生如下两个副反应:
作催化剂,乙苯除脱氢生成苯乙烯外,还会发生如下两个副反应:⑤
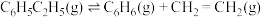
⑥
以上反应体系中,芳香烃产物苯乙烯、苯和甲苯的选择性S(
 )随乙苯转化率的变化曲线如图所示,其中曲线b代表的产物是
)随乙苯转化率的变化曲线如图所示,其中曲线b代表的产物是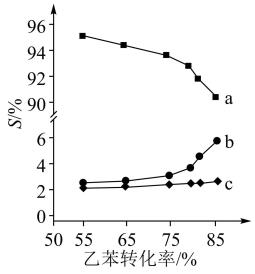
 的描述错误的是_______;
的描述错误的是_______;A.X射线衍射技术可测定 晶体结构 晶体结构 |
B. 可改变乙苯平衡转化率 可改变乙苯平衡转化率 |
C. 降低了乙苯脱氢反应的活化能 降低了乙苯脱氢反应的活化能 |
D.改变 颗粒大小不影响反应速率 颗粒大小不影响反应速率 |
Ⅱ.苯乙烯的聚合
苯乙烯聚合有多种方法,其中一种方法的关键步骤是某
 (Ⅰ)的配合物促进
(Ⅰ)的配合物促进 (引发剂,X表示卤素)生成自由基
(引发剂,X表示卤素)生成自由基 ,实现苯乙烯可控聚合。
,实现苯乙烯可控聚合。(5)引发剂
 中活性最高的是
中活性最高的是(6)室温下,①
 在配体L的水溶液中形成
在配体L的水溶液中形成 ,其反应平衡常数为K;②
,其反应平衡常数为K;② 在水中的溶度积常数为
在水中的溶度积常数为 。由此可知,
。由此可知, 在配体L的水溶液中溶解反应的平衡常数为
在配体L的水溶液中溶解反应的平衡常数为
您最近一年使用:0次
2023-06-16更新
|
7564次组卷
|
9卷引用:2023年高考湖南卷化学真题
2023年高考湖南卷化学真题(已下线)专题17 原理综合题(已下线)2023年湖南卷高考真题变式题(原理综合题)(已下线)专题14 化学反应原理综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题15 化学反应原理综合题-2023年高考化学真题题源解密(全国通用)湖南省长沙市麓山国际实验学校2023-2024学年高三上学期第一次月考化学试题 浙江省义乌中学2024届高三上学期首考适应性考试化学试题湖北省沙市中学2023-2024学年高三下学期3月月考化学试题(已下线)压轴题13 化学反应原理综合题(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
解题方法
4 . 硅及其化合物在生产生活中有广泛应用。根据所学知识,回答下列问题:
(1)三甲基卤硅烷【(CH3)3SiX,X为Cl、Br、I】是重要的化工原料。
①氯元素基态原子的价电子排布式为___ ;按照核外电子排布对元素周期表分区,溴元素位于___ 区;基态硅原子中有____ 种运动状态不同的电子。
②Br、I的第一电离能的大小关系:I1(Br)____ I1(I)(填“大于”“小于”或“等于”)。
③常温下,(CH3)3SiI中Si—I键比(CH3)3SiCl中Si—Cl键易断裂的原因是____ 。
(2)(CH3)3SiCl可作为下列有机合成反应的催化剂。
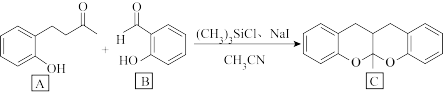
①1个有机物A分子中采取sp2杂化的碳原子有____ 个。
②有机物B的沸点低于对羟基苯甲醛(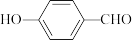 )的沸点,其原因是
)的沸点,其原因是____ 。
③CH3CN中σ键与π键的个数比为____ 。
(3)一种钛硅碳新型材料可用作高铁车体与供电网的连接材料。该材料的晶胞属于六方晶系(a、b方向的夹角为120°,c方向垂直于a、b方向,棱长a+b≠c),如图甲所示;晶胞中碳原子的投影位置如图乙所示。
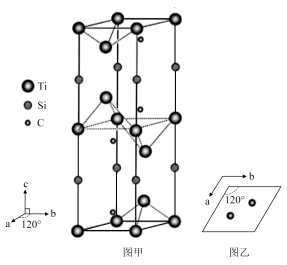
①该钛硅碳新型材料的化学式为____ 。
②已知该新型材料的密度为4.51g•cm-3,且a、b的长度均为307pm,阿伏加德罗常数的值用NA表示,则c的长度为____ pm (列出计算式)。
(1)三甲基卤硅烷【(CH3)3SiX,X为Cl、Br、I】是重要的化工原料。
①氯元素基态原子的价电子排布式为
②Br、I的第一电离能的大小关系:I1(Br)
③常温下,(CH3)3SiI中Si—I键比(CH3)3SiCl中Si—Cl键易断裂的原因是
(2)(CH3)3SiCl可作为下列有机合成反应的催化剂。
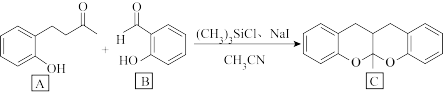
①1个有机物A分子中采取sp2杂化的碳原子有
②有机物B的沸点低于对羟基苯甲醛(
 )的沸点,其原因是
)的沸点,其原因是③CH3CN中σ键与π键的个数比为
(3)一种钛硅碳新型材料可用作高铁车体与供电网的连接材料。该材料的晶胞属于六方晶系(a、b方向的夹角为120°,c方向垂直于a、b方向,棱长a+b≠c),如图甲所示;晶胞中碳原子的投影位置如图乙所示。

①该钛硅碳新型材料的化学式为
②已知该新型材料的密度为4.51g•cm-3,且a、b的长度均为307pm,阿伏加德罗常数的值用NA表示,则c的长度为
您最近一年使用:0次
5 . 铁及其化合物在生产、生活中有重要应用。回答下列问题:
(1)基态Fe3+的价电子排布式为______ 。
(2)某铁的配合物结构如图1所示,可由(CH3)3SiCl与K[Fe(C5H5)(CO)2CO2]混合加热制得。

①在(CH3)3SiCl、(CH3)3SiF、(CH3)4Si中,C-Si-C键角最大的是_______ ,原因是______ 。
②C5H 表示环戊二烯负离子,已知分子中的大π键可用符号π
表示环戊二烯负离子,已知分子中的大π键可用符号π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π ),则C5H
),则C5H 中的大π键应表示为
中的大π键应表示为______ 。
③该铁的配合物中碳原子的杂化方式共有_____ 种。
(3)普鲁士蓝晶体属立方晶系,晶胞棱长为apm。铁-氰骨架组成小立方体,Fe粒子在顶点,CN-在棱上,两端均与Fe相连,立方体中心空隙可容纳K+,如图2所示(CN-在图中省略)。

①普鲁士蓝中Fe2+与Fe3+个数之比为_____ ;该晶胞的化学式为______ 。
②若所有铁粒子为等径小球,则K+与Fe2+之间最近距离为_____ pm;该晶体的密度为_____ g•cm-3(阿伏加德罗常数为NA)。
(1)基态Fe3+的价电子排布式为
(2)某铁的配合物结构如图1所示,可由(CH3)3SiCl与K[Fe(C5H5)(CO)2CO2]混合加热制得。

①在(CH3)3SiCl、(CH3)3SiF、(CH3)4Si中,C-Si-C键角最大的是
②C5H
 表示环戊二烯负离子,已知分子中的大π键可用符号π
表示环戊二烯负离子,已知分子中的大π键可用符号π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π ),则C5H
),则C5H 中的大π键应表示为
中的大π键应表示为③该铁的配合物中碳原子的杂化方式共有
(3)普鲁士蓝晶体属立方晶系,晶胞棱长为apm。铁-氰骨架组成小立方体,Fe粒子在顶点,CN-在棱上,两端均与Fe相连,立方体中心空隙可容纳K+,如图2所示(CN-在图中省略)。

①普鲁士蓝中Fe2+与Fe3+个数之比为
②若所有铁粒子为等径小球,则K+与Fe2+之间最近距离为
您最近一年使用:0次
6 . 铜及其化合物在能源、信息等领域应用广泛。回答下列问题:
(1)铜和锌同周期且相邻,现有几种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10,失去1个电子需要的能量由大到小排序是 (填字母)。
(2)铜的熔点比同周期钾的熔点高,这是由于________ 。
(3)用超临界CO2/CH3CN及水作电解质,使用碳作载体的铜基催化剂可高效将CO2还原为HCOOH。CO2的空间结构为_____ ,CH3CN 中C原子的杂化方式为 _________ 。
(4)[Cu(NH3)4]2+是Cu2+常见的配离子,1 mol [Cu(NH3)4]2+中所含σ键数目为_________ ;[Cu(NH3)4]2+中H-N-H的键角比NH3中H- N- H的键角_____ (填“大”“小”或“无法判断”),原因是______ 。
(5)一种热电材料的晶胞结构如图所示,底部边长为apm的正方形,高为cpm,该晶体的化学式为___ ,紧邻的 Sb与Cu间的距离为______ pm,设NA为阿伏加德罗常数的值,晶体的密度为_____ g· cm-3(列出计算表达式)。
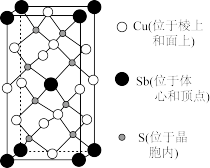
(1)铜和锌同周期且相邻,现有几种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10,失去1个电子需要的能量由大到小排序是 (填字母)。
| A.④②①③ | B.④②③① |
| C.①②④③ | D.①④③② |
(3)用超临界CO2/CH3CN及水作电解质,使用碳作载体的铜基催化剂可高效将CO2还原为HCOOH。CO2的空间结构为
(4)[Cu(NH3)4]2+是Cu2+常见的配离子,1 mol [Cu(NH3)4]2+中所含σ键数目为
(5)一种热电材料的晶胞结构如图所示,底部边长为apm的正方形,高为cpm,该晶体的化学式为

您最近一年使用:0次
2022-05-29更新
|
918次组卷
|
2卷引用:安徽省新未来联盟2022届高三下学期5月联考理科综合化学试题
解题方法
7 . 元素周期表中,第四周期元素单质及其化合物在化工生产和研究中有重要的应用。
(1)Ti能形成化合物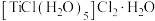 ,该化合物中
,该化合物中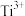 的配位数为
的配位数为______ ,在该化合物中不含______ (填标号)。
A. 键 B.
键 B. 键 C.配位键 D.离子键 E.极性键 F.非极性键
键 C.配位键 D.离子键 E.极性键 F.非极性键
(2)在ZnO催化作用下,呋喃( )可与氨反应,转化为吡咯(
)可与氨反应,转化为吡咯( ),吡咯分子中所有原子共平面,已知大π键可以用
),吡咯分子中所有原子共平面,已知大π键可以用 表示,其中m表示参与形成大
表示,其中m表示参与形成大 键的原子数,n代表大
键的原子数,n代表大 键中的电子数,则吡咯中大
键中的电子数,则吡咯中大 键可以表示为
键可以表示为______ 。呋喃的熔、沸点______ 吡咯(填“高于”或“低于”),原因是______ 。
(3)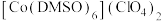 是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为
是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为 。
。 中
中 键角
键角______  中
中 键角(填“大于”“小于”或“等于”)。
键角(填“大于”“小于”或“等于”)。
(4)硒氧化铋是一类:全新二维半导体芯片材料,为四方晶系晶胞结构(如图所示),可以看成带正电的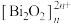 层与带负电的
层与带负电的 层交替堆叠。据此推断硒氧化铋的化学式为
层交替堆叠。据此推断硒氧化铋的化学式为______ 。晶胞棱边夹角均为90°,则晶体密度的计算式为______  (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)Ti能形成化合物
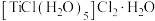 ,该化合物中
,该化合物中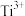 的配位数为
的配位数为A.
 键 B.
键 B. 键 C.配位键 D.离子键 E.极性键 F.非极性键
键 C.配位键 D.离子键 E.极性键 F.非极性键(2)在ZnO催化作用下,呋喃(
 )可与氨反应,转化为吡咯(
)可与氨反应,转化为吡咯( ),吡咯分子中所有原子共平面,已知大π键可以用
),吡咯分子中所有原子共平面,已知大π键可以用 表示,其中m表示参与形成大
表示,其中m表示参与形成大 键的原子数,n代表大
键的原子数,n代表大 键中的电子数,则吡咯中大
键中的电子数,则吡咯中大 键可以表示为
键可以表示为(3)
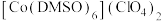 是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为
是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为 。
。 中
中 键角
键角 中
中 键角(填“大于”“小于”或“等于”)。
键角(填“大于”“小于”或“等于”)。(4)硒氧化铋是一类:全新二维半导体芯片材料,为四方晶系晶胞结构(如图所示),可以看成带正电的
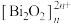 层与带负电的
层与带负电的 层交替堆叠。据此推断硒氧化铋的化学式为
层交替堆叠。据此推断硒氧化铋的化学式为 (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
名校
解题方法
8 . 富勒烯( )是一类完全由碳组成的中空分子,在催化、光电等很多领域都有重要作用。
)是一类完全由碳组成的中空分子,在催化、光电等很多领域都有重要作用。
Ⅰ. 以其完美的球烯受到科学家重视,其结构如右图所示。60个碳原子是等同的,均为近似
以其完美的球烯受到科学家重视,其结构如右图所示。60个碳原子是等同的,均为近似 杂化,但却有两种不同类型的碳碳键。其中一种为
杂化,但却有两种不同类型的碳碳键。其中一种为 ;另一种为
;另一种为 。
。

(1) 在水中溶解度
在水中溶解度______  在甲苯中溶解度(填“>”、“<”或“≈”);
在甲苯中溶解度(填“>”、“<”或“≈”);
(2)请在图中标明这2种类型的键,注明键长_________ ;
(3)石墨、 互为同素异形体,但相同条件下,石墨的熔点比
互为同素异形体,但相同条件下,石墨的熔点比 高得多,原因是
高得多,原因是____________ 。
Ⅱ. 常态下是为紫色固体,不导电,但给富勒烯掺杂金属后(用金属原子把富勒烯分子连起来或者把金属原子放进富勒烯笼子里),其在一定条件下甚至可以成为超导体。
常态下是为紫色固体,不导电,但给富勒烯掺杂金属后(用金属原子把富勒烯分子连起来或者把金属原子放进富勒烯笼子里),其在一定条件下甚至可以成为超导体。
(4)从结构角度解释为什么 不导电
不导电____________ ;
(5) 的晶胞结构如图所示.每个白球代表1个
的晶胞结构如图所示.每个白球代表1个 分子.已知一定条件下晶胞的棱长为
分子.已知一定条件下晶胞的棱长为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该条件下
,则该条件下 的摩尔体积为
的摩尔体积为_______  (用含a、
(用含a、 的代数式表示)
的代数式表示)
(6) 晶体结构中存在四面体空隙(如图中1、3、6、7围成的空隙)和八面体空隙(如图中3、6、7、8、9、12围成的空隙).所有空隙中均填充一个金属M原子,可获得某条件下的超导材料.则该超导材料中,平均一个
晶体结构中存在四面体空隙(如图中1、3、6、7围成的空隙)和八面体空隙(如图中3、6、7、8、9、12围成的空隙).所有空隙中均填充一个金属M原子,可获得某条件下的超导材料.则该超导材料中,平均一个 晶胞需掺杂
晶胞需掺杂______ 个M原子。

 )是一类完全由碳组成的中空分子,在催化、光电等很多领域都有重要作用。
)是一类完全由碳组成的中空分子,在催化、光电等很多领域都有重要作用。Ⅰ.
 以其完美的球烯受到科学家重视,其结构如右图所示。60个碳原子是等同的,均为近似
以其完美的球烯受到科学家重视,其结构如右图所示。60个碳原子是等同的,均为近似 杂化,但却有两种不同类型的碳碳键。其中一种为
杂化,但却有两种不同类型的碳碳键。其中一种为 ;另一种为
;另一种为 。
。
(1)
 在水中溶解度
在水中溶解度 在甲苯中溶解度(填“>”、“<”或“≈”);
在甲苯中溶解度(填“>”、“<”或“≈”);(2)请在图中标明这2种类型的键,注明键长
(3)石墨、
 互为同素异形体,但相同条件下,石墨的熔点比
互为同素异形体,但相同条件下,石墨的熔点比 高得多,原因是
高得多,原因是Ⅱ.
 常态下是为紫色固体,不导电,但给富勒烯掺杂金属后(用金属原子把富勒烯分子连起来或者把金属原子放进富勒烯笼子里),其在一定条件下甚至可以成为超导体。
常态下是为紫色固体,不导电,但给富勒烯掺杂金属后(用金属原子把富勒烯分子连起来或者把金属原子放进富勒烯笼子里),其在一定条件下甚至可以成为超导体。(4)从结构角度解释为什么
 不导电
不导电(5)
 的晶胞结构如图所示.每个白球代表1个
的晶胞结构如图所示.每个白球代表1个 分子.已知一定条件下晶胞的棱长为
分子.已知一定条件下晶胞的棱长为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该条件下
,则该条件下 的摩尔体积为
的摩尔体积为 (用含a、
(用含a、 的代数式表示)
的代数式表示)(6)
 晶体结构中存在四面体空隙(如图中1、3、6、7围成的空隙)和八面体空隙(如图中3、6、7、8、9、12围成的空隙).所有空隙中均填充一个金属M原子,可获得某条件下的超导材料.则该超导材料中,平均一个
晶体结构中存在四面体空隙(如图中1、3、6、7围成的空隙)和八面体空隙(如图中3、6、7、8、9、12围成的空隙).所有空隙中均填充一个金属M原子,可获得某条件下的超导材料.则该超导材料中,平均一个 晶胞需掺杂
晶胞需掺杂
您最近一年使用:0次
2023-02-14更新
|
803次组卷
|
2卷引用:北京市海淀区教师进修学校2022-2023学年高三下学期开学检测化学试题
解题方法
9 . 硫、锌分别是人体必须的常量元素和微量元素,在生产中有着广泛应用。回答下列问题。
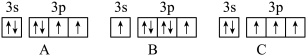
(1)基态硫原子的价电子排布式为___________ ,共有___________ 个未成对电子。下列状态的硫原子中,电离最外层1个电子所需能量最低的是___________ (填标号)。
(2)S与O同族,H2S与H2O空间构型相同,都是2对孤电子对,但H2O分子中的键角比H2S分子中的键角大,请从成键电子对之间相互排斥的角度解释其原因___________ 。
(3)二烃基锌(R-Zn-R)分子中烃基R与锌以σ键结合,C2H5-Zn-C2H5分子中原子的杂化方式有___________ ,下表是2种二烃基锌的沸点数据,则烃基R1是___________ ,推断的依据,是___________ 。
(4)闪锌矿硫化锌的晶胞结构如图所示。硫离子呈立方最密堆积,Zn2+填入S2-组成___________ 空隙中(填“正四面体”或“正八面体”);NA为阿伏加德罗常数,若晶体的密度为ρg/cm3,则S2-离子之间最短核间距离为___________ pm(用含ρ、NA的代数式表示)。
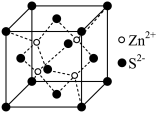
(1)基态硫原子的价电子排布式为

(2)S与O同族,H2S与H2O空间构型相同,都是2对孤电子对,但H2O分子中的键角比H2S分子中的键角大,请从成键电子对之间相互排斥的角度解释其原因
(3)二烃基锌(R-Zn-R)分子中烃基R与锌以σ键结合,C2H5-Zn-C2H5分子中原子的杂化方式有
| 物质 | R1-Zn-R1 | C2H5-Zn-C2H5 |
| 沸点(°C) | 46 | 118 |

您最近一年使用:0次
2023-03-14更新
|
772次组卷
|
3卷引用:四川省泸州市2023届高三下学期第二次教学质量诊断性考试理综化学试题
解题方法
10 . 氟在已知元素中电负性最大、非金属性最强,其单质在1886年才被首次分离出来。
(1)基态F原子的核外电子排布式为___________ 。
(2)氟氧化物 、
、 的结构已经确定。
的结构已经确定。
①依据数据推测O—O键的稳定性:
___________  (填“>”或“<”)。
(填“>”或“<”)。
② 中F—O—F键角小于
中F—O—F键角小于 中H—O—H键角,解释原因:
中H—O—H键角,解释原因:___________ 。
(3) 是一种有特殊性质的氢化物。
是一种有特殊性质的氢化物。
①已知:氢键(X—H…Y)中三原子在一条直线上时,作用力最强。测定结果表明, 固体中
固体中 分子排列为锯齿形,画出含2个
分子排列为锯齿形,画出含2个 的重复单元结构:
的重复单元结构:___________ 。
② 溶剂中加入
溶剂中加入 可以解离出
可以解离出 和具有正四面体形结构的阴离子,写出该过程的离子方程式:
和具有正四面体形结构的阴离子,写出该过程的离子方程式:___________ 。
(4)工业上用萤石(主要成分 )制备
)制备 。
。 晶体的一种立方晶胞如图所示。
晶体的一种立方晶胞如图所示。 晶体中距离
晶体中距离 最近的
最近的 有
有___________ 个。
②晶体中 与
与 的最近距离为
的最近距离为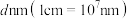 ),阿伏加德罗常数值为
),阿伏加德罗常数值为 。该晶体的密度
。该晶体的密度
___________  (列出计算式)。
(列出计算式)。
 |  | |
O—O键长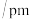 | 121 | 148 |
(2)氟氧化物
 、
、 的结构已经确定。
的结构已经确定。①依据数据推测O—O键的稳定性:

 (填“>”或“<”)。
(填“>”或“<”)。②
 中F—O—F键角小于
中F—O—F键角小于 中H—O—H键角,解释原因:
中H—O—H键角,解释原因:(3)
 是一种有特殊性质的氢化物。
是一种有特殊性质的氢化物。①已知:氢键(X—H…Y)中三原子在一条直线上时,作用力最强。测定结果表明,
 固体中
固体中 分子排列为锯齿形,画出含2个
分子排列为锯齿形,画出含2个 的重复单元结构:
的重复单元结构:②
 溶剂中加入
溶剂中加入 可以解离出
可以解离出 和具有正四面体形结构的阴离子,写出该过程的离子方程式:
和具有正四面体形结构的阴离子,写出该过程的离子方程式:(4)工业上用萤石(主要成分
 )制备
)制备 。
。 晶体的一种立方晶胞如图所示。
晶体的一种立方晶胞如图所示。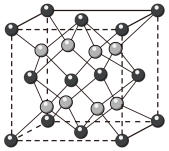
 晶体中距离
晶体中距离 最近的
最近的 有
有②晶体中
 与
与 的最近距离为
的最近距离为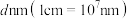 ),阿伏加德罗常数值为
),阿伏加德罗常数值为 。该晶体的密度
。该晶体的密度
 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
2023-04-06更新
|
667次组卷
|
2卷引用:北京市海淀区2022-2023学年高三下学期期中练习化学试题



