解题方法
1 . 一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成。回答下列问题:
(1)在配合物K4[Fe(CN)6]中,配位体是___________ ,配位数是___________ 。
(2)新制备的Cu(OH)2可氧化乙醛,而自身还原成Cu2O,写出该反应的化学方程式:___________ ,乙醛分子中碳原子的杂化轨道类型为___________ 。1mol乙醛分子中含有 键的数目约为
键的数目约为___________ 。乙酸的沸点明显高于乙醛,其主要原因是___________ 。Cu2O为半导体材料,在其立方晶胞内部有1个氧原子,其余氧原子均位于顶点,则该晶胞有___________ 个铜原子。
(3)Al晶体结构如图所示,晶体中每个Al周围等距且紧邻的Al有___________ 个。晶胞棱长为anm,密度为___________ gcm-3(NA表示阿伏加德罗常数的值)。

(1)在配合物K4[Fe(CN)6]中,配位体是
(2)新制备的Cu(OH)2可氧化乙醛,而自身还原成Cu2O,写出该反应的化学方程式:
 键的数目约为
键的数目约为(3)Al晶体结构如图所示,晶体中每个Al周围等距且紧邻的Al有

您最近一年使用:0次
解题方法
2 . 坐落在河北区的华为天津区域总部项目计划于2023年12月底竣工。石墨烯液冷散热技术系华为公司首创,所使用材料石墨烯是一种二维碳纳米材料。
I. 、金刚石、石墨的结构模型如图所示(石墨仅表示出其中的一层结构):
、金刚石、石墨的结构模型如图所示(石墨仅表示出其中的一层结构):

(1)金刚石、石墨和 三者互为___________(填序号)。
三者互为___________(填序号)。
(2) 晶体的晶体类型为
晶体的晶体类型为___________ 。
(3)晶体硅的结构跟金刚石相似,1mol晶体硅中所含有硅硅单键的数目是___________ 。
(4)石墨层状结构中,平均每个正六边形占有的碳原子数是___________ 。
II.石墨烯(图甲)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(图乙)。
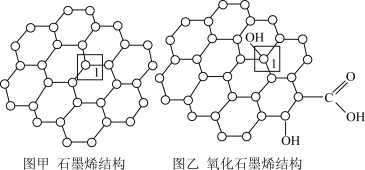

(5)图甲中,1号C与相邻C形成 键的个数为
键的个数为___________ 。
(6)图乙中,1号C的杂化方式是___________ 。
(7)若将图乙中所示的氧化石墨烯分散在 中,则氧化石墨烯中可与
中,则氧化石墨烯中可与 形成氢键的原子有
形成氢键的原子有___________ (填元素符号)。
(8)石墨烯可转化为富勒烯( ),某金属M与
),某金属M与 可制备一种低温超导材料,晶胞如图丙所示,M原子位于晶胞的棱上与内部。该材料的化学式为
可制备一种低温超导材料,晶胞如图丙所示,M原子位于晶胞的棱上与内部。该材料的化学式为___________ 。
I.
 、金刚石、石墨的结构模型如图所示(石墨仅表示出其中的一层结构):
、金刚石、石墨的结构模型如图所示(石墨仅表示出其中的一层结构):
(1)金刚石、石墨和
 三者互为___________(填序号)。
三者互为___________(填序号)。| A.同分异构体 | B.同素异形体 | C.同系物 | D.同位素 |
 晶体的晶体类型为
晶体的晶体类型为(3)晶体硅的结构跟金刚石相似,1mol晶体硅中所含有硅硅单键的数目是
(4)石墨层状结构中,平均每个正六边形占有的碳原子数是
II.石墨烯(图甲)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(图乙)。


(5)图甲中,1号C与相邻C形成
 键的个数为
键的个数为(6)图乙中,1号C的杂化方式是
(7)若将图乙中所示的氧化石墨烯分散在
 中,则氧化石墨烯中可与
中,则氧化石墨烯中可与 形成氢键的原子有
形成氢键的原子有(8)石墨烯可转化为富勒烯(
 ),某金属M与
),某金属M与 可制备一种低温超导材料,晶胞如图丙所示,M原子位于晶胞的棱上与内部。该材料的化学式为
可制备一种低温超导材料,晶胞如图丙所示,M原子位于晶胞的棱上与内部。该材料的化学式为
您最近一年使用:0次
解题方法
3 . 氮、磷、砷、锑为元素周期表中原子序数依次增大的同族元素。
(1)除 外,科学家还先后研究出了
外,科学家还先后研究出了 、
、 、
、 、高聚氮等氮的单质。
、高聚氮等氮的单质。 为正四面体结构,高聚氮具有空间网状结构,如图所示。
为正四面体结构,高聚氮具有空间网状结构,如图所示。

① 分子是一种
分子是一种_______ (填“极性”或“非极性”)分子。
② 的沸点
的沸点_______ (填“>”、“<”或“=”)高聚氮的沸点,原因是_______ 。
(2)热稳定性:
_______  (填“>”“<”),判断依据是
(填“>”“<”),判断依据是_______ 。
(3) 链状分子中所有原子都满足8电子稳定结构,则其分子中
链状分子中所有原子都满足8电子稳定结构,则其分子中 键与
键与 键之比为
键之比为_______ ,C原子的杂化类型为_______ 。
(1)除
 外,科学家还先后研究出了
外,科学家还先后研究出了 、
、 、
、 、高聚氮等氮的单质。
、高聚氮等氮的单质。 为正四面体结构,高聚氮具有空间网状结构,如图所示。
为正四面体结构,高聚氮具有空间网状结构,如图所示。
①
 分子是一种
分子是一种②
 的沸点
的沸点(2)热稳定性:

 (填“>”“<”),判断依据是
(填“>”“<”),判断依据是(3)
 链状分子中所有原子都满足8电子稳定结构,则其分子中
链状分子中所有原子都满足8电子稳定结构,则其分子中 键与
键与 键之比为
键之比为
您最近一年使用:0次
名校
解题方法
4 . 碳和硅均为元素周期表中第ⅣA族的元素,其单质和化合物有着重要应用。
(1)石墨烯是只有一个碳原子直径厚度的单层石墨,最早是由科学家用机械剥离的方法从石墨中分离出来,其部分性能优于传统的硅材料,具有广泛的应用前景。
①写出基态碳原子的电子排布式_______ ,石墨烯中C的杂化类型为_______ 。
②下图为单层石墨烯的结构示意图。12 g的石墨烯中由C原子连接成的六元环的物质的量约为_______ mol。

③石墨烯可由加热SiC晶体脱除Si的方法制得。该过程属于_______ 。
a.物理变化 b.分解反应 c.氧化还原反应
(2)SiC的晶体结构与晶体硅类似。SiC的晶体类型为_______ ,晶体中Si原子与Si-C键的数目之比为_______ 。
(3)CHCl3与SiHCl3空间构型相似,但性质不同:前者不易与水反应,但后者与水剧烈反应,生成两种酸和一种气体,写出该反应的化学方程式:______ 。
(1)石墨烯是只有一个碳原子直径厚度的单层石墨,最早是由科学家用机械剥离的方法从石墨中分离出来,其部分性能优于传统的硅材料,具有广泛的应用前景。
①写出基态碳原子的电子排布式
②下图为单层石墨烯的结构示意图。12 g的石墨烯中由C原子连接成的六元环的物质的量约为

③石墨烯可由加热SiC晶体脱除Si的方法制得。该过程属于
a.物理变化 b.分解反应 c.氧化还原反应
(2)SiC的晶体结构与晶体硅类似。SiC的晶体类型为
(3)CHCl3与SiHCl3空间构型相似,但性质不同:前者不易与水反应,但后者与水剧烈反应,生成两种酸和一种气体,写出该反应的化学方程式:
您最近一年使用:0次
名校
解题方法
5 . 请回答下列问题。
(1)钴及其化合物有重要的用途,探究其结构有重要意义。
①请写出基态钴原子的核外电子排布式_________ 。
②按照核外电子排布,可把元素周期表划分为5个区, 在元素周期表中属于
在元素周期表中属于_________ 区。
(2) 是
是 的一种重要配合物。
的一种重要配合物。
①该配合物的一种配体是 ,
, 的空间结构呈
的空间结构呈_________ 形,是_________ (填“极性”或“非极性)分子。
② 的价层电子轨道表示式是
的价层电子轨道表示式是_________ 。
③ 中含有的
中含有的 键的数目为
键的数目为_________ (用 代表阿伏加德罗常数) 。
代表阿伏加德罗常数) 。
④设计实验证实该配合物溶于水时,离子键发生断裂,配位键没有断裂。实验如下:称取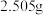 该配合物,先加水溶解,再加足量
该配合物,先加水溶解,再加足量 溶液,
溶液,_________ (补全实验操作),称量沉淀质量为_________ (精确到 ,相对分子质量
,相对分子质量 :250.5;
:250.5; :143.5) 。
:143.5) 。
(3)第ⅤA族元素及其化合物的结构和性质如下:
① 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为_________ (填化学式,下同),键角由大到小的顺序为_________ 。
②某一种氮化硼晶体的立方晶胞结构如图:
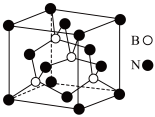
i.氮化硼 属于
属于_________ 晶体;该种氮化硼 的熔点
的熔点_________  (填>、<、=)。
(填>、<、=)。
ii.已知氮化硼 晶胞的边长为
晶胞的边长为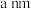 ,则晶胞密度为
,则晶胞密度为_________  (用含有a、
(用含有a、 的代数式表示)。
的代数式表示)。
(1)钴及其化合物有重要的用途,探究其结构有重要意义。
①请写出基态钴原子的核外电子排布式
②按照核外电子排布,可把元素周期表划分为5个区,
 在元素周期表中属于
在元素周期表中属于(2)
 是
是 的一种重要配合物。
的一种重要配合物。①该配合物的一种配体是
 ,
, 的空间结构呈
的空间结构呈②
 的价层电子轨道表示式是
的价层电子轨道表示式是③
 中含有的
中含有的 键的数目为
键的数目为 代表阿伏加德罗常数) 。
代表阿伏加德罗常数) 。④设计实验证实该配合物溶于水时,离子键发生断裂,配位键没有断裂。实验如下:称取
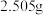 该配合物,先加水溶解,再加足量
该配合物,先加水溶解,再加足量 溶液,
溶液, ,相对分子质量
,相对分子质量 :250.5;
:250.5; :143.5) 。
:143.5) 。(3)第ⅤA族元素及其化合物的结构和性质如下:
①
 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为②某一种氮化硼晶体的立方晶胞结构如图:

i.氮化硼
 属于
属于 的熔点
的熔点 (填>、<、=)。
(填>、<、=)。ii.已知氮化硼
 晶胞的边长为
晶胞的边长为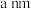 ,则晶胞密度为
,则晶胞密度为 (用含有a、
(用含有a、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解题方法
6 . 国内外学者近年来对金属-有机框架(MOFs)作为催化剂光解制氢和还原CO2等方面的研究取得了丰硕的成果。其中Masaya 等人利用Ti- MOF-NH2、H2PtCl6、 DMF 等原料制备了催化剂Pt/Ti- MOF-NH2。回答下列问题:
(1)Pt的电子排布式为[Xe]4f145d96s1,则Pt在元素周期表中的位置是___________ ,处于_____ 区,未成对电子数是________ 。
(2)PtCl 的价层电子对互斥模型如图所示,已知该离子是平面形结构,则该离子中的键角是
的价层电子对互斥模型如图所示,已知该离子是平面形结构,则该离子中的键角是___________ , 中心原子采用的杂化类型可能是___________ (填 “dsp2”“sp3”“sp2”或“sp3d2”)。

(3)DMF的结构是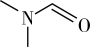 ,σ键与π键的数目比是
,σ键与π键的数目比是___________ ,其中N原子的杂化方式是___________ 。
(4)已知pKa=—lgKa,CCl3CH2OH 的pKa小于CBr3CH2OH,从分子组成与性质之间的关系解释原因______ 。
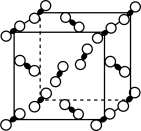
(5)一定条件下, CO2分子可形成干冰晶体,干冰的晶胞模型如图所示。在干冰中,与一个CO2分子紧邻的分子共有___________ 个。若阿伏加德罗常数为NA, 干冰的密度为ρg·cm-3, 则晶胞体对角线长度是___________ cm。
(1)Pt的电子排布式为[Xe]4f145d96s1,则Pt在元素周期表中的位置是
(2)PtCl
 的价层电子对互斥模型如图所示,已知该离子是平面形结构,则该离子中的键角是
的价层电子对互斥模型如图所示,已知该离子是平面形结构,则该离子中的键角是
(3)DMF的结构是
 ,σ键与π键的数目比是
,σ键与π键的数目比是(4)已知pKa=—lgKa,CCl3CH2OH 的pKa小于CBr3CH2OH,从分子组成与性质之间的关系解释原因
(5)一定条件下, CO2分子可形成干冰晶体,干冰的晶胞模型如图所示。在干冰中,与一个CO2分子紧邻的分子共有

您最近一年使用:0次



