名校
解题方法
1 . 工业上采用还原法冾炼黄金(Au)的原理如下:


请回答下列问题:
(1)在元素周期表中,Au与Cu位于同族,基态Au原子比基态Cu原子多2个电子层。基态Au原子的价层电子排布式为___________ ,金元素位于___________ 区。
(2)Zn和Cu相邻,第一电离能:I1(Cu)___________ (填“>”、“<”或“=”,下同)I1(Zn),第二电离能:I2(Cu)___________ I2(Zn)。
(3)1mol 中含
中含___________ molσ键。
(4)已知卤化锌的熔点如下表所示:
卤化锌的熔点存在差异的主要原因是___________ 。
(5)由金、氯、铯三种元素组成的晶体M,其晶胞结构如图1所示,M的化学式为___________ ,其中金原子形成了2种不同的配离子(均呈负一价),它们分别是___________ 和___________ (写出离子符号,不分顺序)。

(6)金晶体的晶胞结构如图2所示,其晶胞参数为408pm,金晶体的密度为___________ (只列计算式,设 为阿伏加德罗常数的值)
为阿伏加德罗常数的值) 。
。



请回答下列问题:
(1)在元素周期表中,Au与Cu位于同族,基态Au原子比基态Cu原子多2个电子层。基态Au原子的价层电子排布式为
(2)Zn和Cu相邻,第一电离能:I1(Cu)
(3)1mol
 中含
中含(4)已知卤化锌的熔点如下表所示:
| 卤化锌 |  |  | 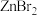 | 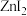 |
| 熔点/℃ | 872 | 283 | 394 | 446 |
(5)由金、氯、铯三种元素组成的晶体M,其晶胞结构如图1所示,M的化学式为

(6)金晶体的晶胞结构如图2所示,其晶胞参数为408pm,金晶体的密度为
 为阿伏加德罗常数的值)
为阿伏加德罗常数的值) 。
。
您最近一年使用:0次
2021-12-02更新
|
327次组卷
|
6卷引用:广东省2021-2022学年高三11月联考化学试题
广东省2021-2022学年高三11月联考化学试题广东省韶关市2021-2022学年高三上学期期中考试化学试题河南省名校联盟2021-2022学年高三上学期11月联考化学试题河北省保定市部分学校2021-2022学年高三上学期期中考试化学试题广东省深圳市龙华中学2021-2022学年高三下学期(二月第二次)半周测化学试题(已下线)押新高考卷15题 物质结构与性质综合题-备战2022年高考化学临考题号押题(新高考通版)
解题方法
2 . 某柔性屏手机的柔性电池以碳纳米管做电极材料,以吸收ZnSO4溶液的有机高聚物做固态电解质,其电池总反应为MnO2+ Zn+(1+
Zn+(1+ )H2O+
)H2O+ ZnSO4
ZnSO4 MnOOH+
MnOOH+ ZnSO4[Zn(OH)2]3∙xH2O,其电池结构如图甲所示,图乙是有机高聚物的结构片段。
ZnSO4[Zn(OH)2]3∙xH2O,其电池结构如图甲所示,图乙是有机高聚物的结构片段。

(1)Mn2+的核外电子排布式为___________ ;有机高聚物中C的杂化方式为___________ 。
(2)已知CN—与N2互为等电子体,推算拟卤(CN)2分子中σ键与π键数目之比为___________ 。
(3) 的空间构型为
的空间构型为___________ 。
(4)MnO是离子晶体,其晶格能可通过如图的Born-Haber循环计算得到。

①Mn的第一电离能是__ (数值用上图中字母表示,下同),O2的键能是__ ,MnO的晶格能是___________ 。
②Mn2+比Fe2+稳定,其原因是___________ 。
(5)R由Zn、S组成(S原子位于晶胞的面心和顶点),其化学式为___________ (用元素符号表示)。已知其晶胞边长为acm,则该晶胞的密度为___________ g·cm3(阿伏加德罗常数用NA表示)。

 Zn+(1+
Zn+(1+ )H2O+
)H2O+ ZnSO4
ZnSO4 MnOOH+
MnOOH+ ZnSO4[Zn(OH)2]3∙xH2O,其电池结构如图甲所示,图乙是有机高聚物的结构片段。
ZnSO4[Zn(OH)2]3∙xH2O,其电池结构如图甲所示,图乙是有机高聚物的结构片段。
(1)Mn2+的核外电子排布式为
(2)已知CN—与N2互为等电子体,推算拟卤(CN)2分子中σ键与π键数目之比为
(3)
 的空间构型为
的空间构型为(4)MnO是离子晶体,其晶格能可通过如图的Born-Haber循环计算得到。

①Mn的第一电离能是
②Mn2+比Fe2+稳定,其原因是
(5)R由Zn、S组成(S原子位于晶胞的面心和顶点),其化学式为

您最近一年使用:0次
3 .  表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.7.8g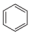 中含有的 中含有的 键数目为0.6 键数目为0.6 |
B.3.6g冰中含有的氢键数目为0.4 |
C.标准状况下,11.2L HF中含有的电子数目为5 |
D.12g 晶体中含有的Si—O键数目为0.4 晶体中含有的Si—O键数目为0.4 |
您最近一年使用:0次
2021-07-09更新
|
282次组卷
|
3卷引用:广东省肇庆市2020-2021学年高二下学期末教学质量检测化学(物质结构与性质)试题
4 . 某有机物的结构简式为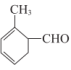 ,该分子中
,该分子中 键与
键与 键的个数比为
键的个数比为
 ,该分子中
,该分子中 键与
键与 键的个数比为
键的个数比为| A.19∶3 | B.8∶1 | C.7∶1 | D.6∶1 |
您最近一年使用:0次
2021-07-09更新
|
396次组卷
|
3卷引用:广东省肇庆市2020-2021学年高二下学期末教学质量检测化学(物质结构与性质)试题
广东省肇庆市2020-2021学年高二下学期末教学质量检测化学(物质结构与性质)试题(已下线)第2.1.1讲 共价键-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)河南省信阳市浉河区新时代学校2021-2022学年高一下学期期中教学质量检测化学试题
名校
5 . 环碳如图所示,球表示碳原子,棍表示单键双键或三键。下列有关环碳的叙述错误的是
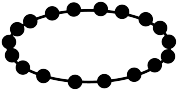

| A.与金刚石互为同素异形体 | B.环碳的摩尔质量为 |
| C.分子中的碳碳键只能都是双键 | D.能与氢气发生加成反应生成环十八烷 |
您最近一年使用:0次
2020-08-07更新
|
265次组卷
|
5卷引用:广东省揭阳普宁二中2021届上学期高三第一次月考化学试题



