解题方法
1 . 锌电池具有成本低、安全性强、可循环使用等优点。一种新型锌电池的工作原理如图所示(凝胶中允许离子生成或迁移)。下列说法错误的是
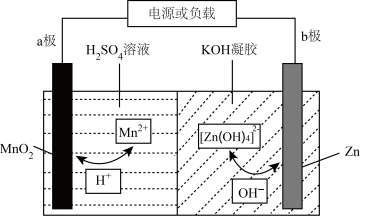
| A.充电过程中,b极接外接电源的负极 |
B.放电过程中,转移 时,b极消耗 时,b极消耗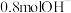 |
C.放电过程中,a极的电极反应式为 |
D.配离子 中Zn采用的是 中Zn采用的是 杂化,该配离子为空间四面体结构 杂化,该配离子为空间四面体结构 |
您最近一年使用:0次
名校
解题方法
2 . 下列分子或离子的空间结构和中心原子的杂化方式均正确的是
A. 平面三角形 平面三角形  杂化 杂化 | B. 平面三角形 平面三角形  杂化 杂化 |
C. V形 V形  杂化 杂化 | D. 三角锥形 三角锥形  杂化 杂化 |
您最近一年使用:0次
2024-04-21更新
|
243次组卷
|
7卷引用:福建省南安市侨光中学2023-2024学年高二下学期4月月考化学试题
福建省南安市侨光中学2023-2024学年高二下学期4月月考化学试题四川省内江市第六中学2022-2023学年高二上学期期中考试化学试题天津市静海区四校2022-2023学年高二下学期3月阶段性检测化学试题(已下线)期中模拟预测卷02(测试范围:选择性必修2+选择性必修3第1章)-2022-2023学年高二化学下学期期中期末考点大串讲(人教版2019)天津市第三中学2022-2023学年高二下学期期中质量检测化学试题陕西省渭南市华州区咸林中学2023-2024学年高二下学期第一次月考化学试题浙江省舟山中学2023-2024学年高二下学期4月月考化学试题
3 . 我国在商代或更早就掌握了冶炼铜的技术。以黄铜矿为原料冶炼铜涉及多个反应,其中一个反应为 。
。
(1)基态 的电子排布式为
的电子排布式为___________ ,从原子结构角度上解释,高温下 能转化为
能转化为 的原因是
的原因是___________ 。铜、铁两类原子核外电子运动状态相差___________ 种。
(2) 四种含硫微粒中,中心原子为
四种含硫微粒中,中心原子为 杂化的是
杂化的是___________
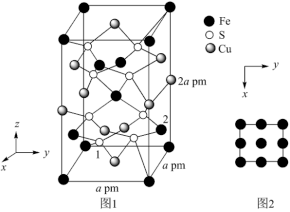
(3) 晶胞结构如图1所示。晶胞中
晶胞结构如图1所示。晶胞中 的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1的坐标分数为(
的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1的坐标分数为( ),则原子2的分数坐标为
),则原子2的分数坐标为___________ ;
 。
。(1)基态
 的电子排布式为
的电子排布式为 能转化为
能转化为 的原因是
的原因是(2)
 四种含硫微粒中,中心原子为
四种含硫微粒中,中心原子为 杂化的是
杂化的是(3)
 晶胞结构如图1所示。晶胞中
晶胞结构如图1所示。晶胞中 的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1的坐标分数为(
的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1的坐标分数为( ),则原子2的分数坐标为
),则原子2的分数坐标为
您最近一年使用:0次
名校
解题方法
4 . 下列化学用语或图示表达正确的是
A. 的电子式为 的电子式为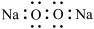 | B. 的VSEPR(价层电子对互斥)模型 的VSEPR(价层电子对互斥)模型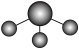 |
C.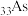 的电子排布式: 的电子排布式: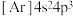 | D.中子数为10的氧原子: |
您最近一年使用:0次
名校
解题方法
5 . 价层电子对互斥理论可以预测某些微粒的空间结构。下列说法正确的是
A. 和 和 的空间构型均为直线型 的空间构型均为直线型 | B. 和 和 的价层电子对互斥模型均为四面体 的价层电子对互斥模型均为四面体 |
C. 和 和 均为非极性分子 均为非极性分子 | D. 与 与 的键角相等 的键角相等 |
您最近一年使用:0次
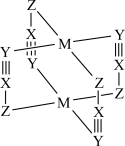
6 . 一种金属有机框架材料的化学式为 ,其结构如图。X、Y、Z、M为原子序数依次增大的1~36号元素,其中X、Z位于不同周期,四种元素中Y的第一电离能最大,
,其结构如图。X、Y、Z、M为原子序数依次增大的1~36号元素,其中X、Z位于不同周期,四种元素中Y的第一电离能最大, 的d轨道全充满。下列说法正确的是
的d轨道全充满。下列说法正确的是
 ,其结构如图。X、Y、Z、M为原子序数依次增大的1~36号元素,其中X、Z位于不同周期,四种元素中Y的第一电离能最大,
,其结构如图。X、Y、Z、M为原子序数依次增大的1~36号元素,其中X、Z位于不同周期,四种元素中Y的第一电离能最大, 的d轨道全充满。下列说法正确的是
的d轨道全充满。下列说法正确的是
A.键角: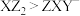 | B.最简单氢化物沸点:Z>Y>X |
| C.电负性:X>Y>M | D.最高价氧化物对应水化物酸性:Z>X |
您最近一年使用:0次
2024-02-03更新
|
182次组卷
|
3卷引用:福建省龙岩市2023-2024学年高三上学期期末考试化学试题
名校
解题方法
7 . 铼(Re)是生产飞机发动机叶片必不可少的材料。X、Y、Z、Q、W是原子序数依次增大且位于不同主族的短周期元素,其中X、Y、Z三种元素可与铼元素组成一种化合物(结构如图),该化合物与X的单质反应可得到铼。Q是地壳中含量最丰富的金属元素,Z与W形成的化合物为共价晶体。下列说法不正确的是
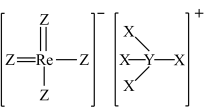
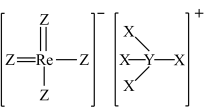
A.元素第一电离能: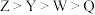 |
B.图中的阳离子与 互为等电子体,具有相同的空间结构 互为等电子体,具有相同的空间结构 |
| C.Q的最高价氧化物对应水化物可以和强碱反应 |
| D.熔点:W晶体小于W、Y形成的晶体 |
您最近一年使用:0次
2024-01-24更新
|
167次组卷
|
2卷引用:福建省三明第一中学2023-2024学年高三上学期12月月考化学试题
名校
8 . 镍、钴是重要的战略物资,但资源匮乏。一种利用酸浸出法从冶金厂废炉渣中提取镍和钴的工艺流程如下:
ii.NiSO4在水中的溶解度随温度升高而增大
回答下列问题:
(1)Co2+ 的价电子排布式________ , 空间构型为
空间构型为________
(2)提高“酸浸”速率的方法有_________ 。(任写一条)
(3)“滤渣1”的主要成分是_________ 。(写化学式)
(4)黄钠铁矾的化学式为Na2 Fe 6(SO4)4(OH)12,“除铁”的离子方程式为___________ 。
(5)“除钙镁”时,随pH降低,NaF用量急剧增加,原因是________ (结合平衡理论解释)。Ca2+和Mg2+沉淀完全时,溶液中F-的浓度c(F- )最小为______ mol·L-1(已知离子浓度≤10-5 mol·L-1时,认为该离子沉淀完全,Ksp(CaF2)=1.0 ×10-10,Ksp(MgF2)=7.5×10-11)。
(6)获得NiSO4(s)的“一系列操作”是________ 。
(7)工艺流程中,可循环利用的物质是___________ 。
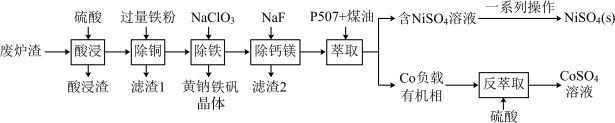
ii.NiSO4在水中的溶解度随温度升高而增大
回答下列问题:
(1)Co2+ 的价电子排布式
 空间构型为
空间构型为(2)提高“酸浸”速率的方法有
(3)“滤渣1”的主要成分是
(4)黄钠铁矾的化学式为Na2 Fe 6(SO4)4(OH)12,“除铁”的离子方程式为
(5)“除钙镁”时,随pH降低,NaF用量急剧增加,原因是
(6)获得NiSO4(s)的“一系列操作”是
(7)工艺流程中,可循环利用的物质是
您最近一年使用:0次
名校
解题方法
9 . 实验室中利用如图装置(部分装置省略)制备 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。
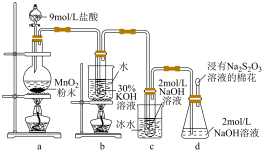
(1)盛放9mol/L盐酸的仪器名称是_______ 。
(2)b中发生化学反应的离子方程式是_______ 。
(3)d中浸有 溶液的棉花的作用是
溶液的棉花的作用是_______ 。
(4)下列相关说法不正确的是_______(填标号)。
(5)当b中试管内溶液由黄色变为无色时,反应到达终点。实际操作时,发现溶液由黄色变为紫红色甚至产生棕色沉淀影响产品纯度。针对该现象,可能混入的物质是_______ 。
(6)取少量 和NaClO溶液分别置于1号和2号试管中,滴加
和NaClO溶液分别置于1号和2号试管中,滴加 溶液。两支试管均无明显现象,但试管2试管壁发烫。在上述实验基础上,设计实验进一步验证该条件下
溶液。两支试管均无明显现象,但试管2试管壁发烫。在上述实验基础上,设计实验进一步验证该条件下 的氧化能力小于NaClO
的氧化能力小于NaClO_______ 。(供选择的试剂:稀盐酸、稀硝酸、BaCl2溶液、 溶液)
溶液)
(7) 中氧原子的p轨道上的孤对电子进入氯原子的d轨道形成d-pπ键。d-pπ键长:
中氧原子的p轨道上的孤对电子进入氯原子的d轨道形成d-pπ键。d-pπ键长:
_______  (填“>”或“<”)。
(填“>”或“<”)。
 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。
(1)盛放9mol/L盐酸的仪器名称是
(2)b中发生化学反应的离子方程式是
(3)d中浸有
 溶液的棉花的作用是
溶液的棉花的作用是(4)下列相关说法不正确的是_______(填标号)。
| A.使用选择9mol/L盐酸替换浓盐酸,有利于减少HCl挥发 |
| B.控制液体滴加速率以维持氯气气流稳定,有利于减少反应过程倒吸的可能 |
C.反应结束后,b中液体经冷却结晶、过滤、冷水洗涤、干燥,可得 晶体 晶体 |
| D.增大装置c中NaOH溶液的浓度,有利于提高NaClO产率 |
(5)当b中试管内溶液由黄色变为无色时,反应到达终点。实际操作时,发现溶液由黄色变为紫红色甚至产生棕色沉淀影响产品纯度。针对该现象,可能混入的物质是
(6)取少量
 和NaClO溶液分别置于1号和2号试管中,滴加
和NaClO溶液分别置于1号和2号试管中,滴加 溶液。两支试管均无明显现象,但试管2试管壁发烫。在上述实验基础上,设计实验进一步验证该条件下
溶液。两支试管均无明显现象,但试管2试管壁发烫。在上述实验基础上,设计实验进一步验证该条件下 的氧化能力小于NaClO
的氧化能力小于NaClO 溶液)
溶液)(7)
 中氧原子的p轨道上的孤对电子进入氯原子的d轨道形成d-pπ键。d-pπ键长:
中氧原子的p轨道上的孤对电子进入氯原子的d轨道形成d-pπ键。d-pπ键长:
 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
名校
解题方法
10 . 下列化学用语或图示表达不正确的是
A.金刚石的晶体结构: |
B.基态溴原子电子占据最高能级的电子云轮廓图: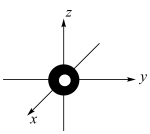 |
C.乙炔的球棍模型: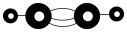 |
D. 的 的 模型为 模型为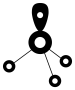 |
您最近一年使用:0次



