解题方法
1 . 下列离子的 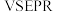 模型与其空间结构一致的是
模型与其空间结构一致的是
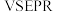 模型与其空间结构一致的是
模型与其空间结构一致的是A. | B. | C.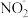 | D. |
您最近半年使用:0次
解题方法
2 . 液氨是一种很好的溶剂,液氨可以微弱的电离产生NH 和NH
和NH 。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成NH2OH(羟胺)。在有NH
。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成NH2OH(羟胺)。在有NH 存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成N2、NO、NO2、N2O4(无色)、HNO3等。下列有关NH2OH、NH3、NH
存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成N2、NO、NO2、N2O4(无色)、HNO3等。下列有关NH2OH、NH3、NH 、NO
、NO 、[Cu(NH3)4]2+的说法正确的是
、[Cu(NH3)4]2+的说法正确的是
 和NH
和NH 。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成NH2OH(羟胺)。在有NH
。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成NH2OH(羟胺)。在有NH 存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成N2、NO、NO2、N2O4(无色)、HNO3等。下列有关NH2OH、NH3、NH
存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成N2、NO、NO2、N2O4(无色)、HNO3等。下列有关NH2OH、NH3、NH 、NO
、NO 、[Cu(NH3)4]2+的说法正确的是
、[Cu(NH3)4]2+的说法正确的是A.NO 的空间构型为三角锥形 的空间构型为三角锥形 | B.NH3中N原子的杂化方式皆为sp2 |
C.NH3的键角比NH 中的大 中的大 | D.1 mol [Cu(NH3)4]2+中含有σ键的数目为12 mol |
您最近半年使用:0次
解题方法
3 . 锌电池具有成本低、安全性强、可循环使用等优点。一种新型锌电池的工作原理如图所示(凝胶中允许离子生成或迁移)。下列说法错误的是
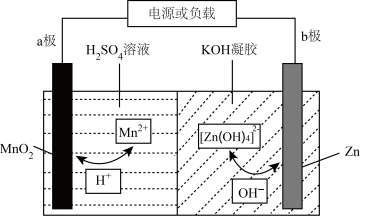
| A.充电过程中,b极接外接电源的负极 |
B.放电过程中,转移 时,b极消耗 时,b极消耗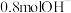 |
C.放电过程中,a极的电极反应式为 |
D.配离子 中Zn采用的是 中Zn采用的是 杂化,该配离子为空间四面体结构 杂化,该配离子为空间四面体结构 |
您最近半年使用:0次
解题方法
4 . 近日,科学家利用铁配合物催化氮气选择性转化成肼。铁配合物结构如图所示(Et为乙基:-CH2CH3)。

回答下列问题:
(1)基态 的价层电子排布式
的价层电子排布式___________ ,微粒半径Fe___________  。(填“大于”、“小于”或“等于”)
。(填“大于”、“小于”或“等于”)
(2) 所含元素中,电负性最大的元素是
所含元素中,电负性最大的元素是___________ 。P原子的杂化类型是___________ 。
(3) 和
和 的相对分子质量相同,但是常温常压下,
的相对分子质量相同,但是常温常压下, 呈液态,而
呈液态,而 呈气态,其主要原因是
呈气态,其主要原因是___________ 。
(4) 的VSEPR模型为
的VSEPR模型为___________ 。写出N2的一种等电子体___________ 。
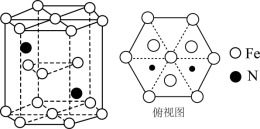
(5)某种磁性氮化铁的晶胞结构如图所示。已知: 为阿伏加德罗常数的值,六棱柱底边的边长为
为阿伏加德罗常数的值,六棱柱底边的边长为 ,高为
,高为 ,该晶体中Fe、N原子个数最简比为
,该晶体中Fe、N原子个数最简比为___________ 。该晶体的密度为___________  (只列计算式)。
(只列计算式)。

回答下列问题:
(1)基态
 的价层电子排布式
的价层电子排布式 。(填“大于”、“小于”或“等于”)
。(填“大于”、“小于”或“等于”)(2)
 所含元素中,电负性最大的元素是
所含元素中,电负性最大的元素是(3)
 和
和 的相对分子质量相同,但是常温常压下,
的相对分子质量相同,但是常温常压下, 呈液态,而
呈液态,而 呈气态,其主要原因是
呈气态,其主要原因是(4)
 的VSEPR模型为
的VSEPR模型为(5)某种磁性氮化铁的晶胞结构如图所示。已知:
 为阿伏加德罗常数的值,六棱柱底边的边长为
为阿伏加德罗常数的值,六棱柱底边的边长为 ,高为
,高为 ,该晶体中Fe、N原子个数最简比为
,该晶体中Fe、N原子个数最简比为 (只列计算式)。
(只列计算式)。
您最近半年使用:0次
解题方法
5 . 钛是20世纪50年代发展起来的一种重要的结构金属,钛合金因具有强度高、耐蚀性好、耐热性高等特点而被广泛用于各个领域。回答下列问题:
(1)钛元素在元素周期表中的位置_____ 。与钛同周期且未成对电子数最多的元素,其价层电子排布图为_____ 。
(2)二氧化钛与 (光气)、
(光气)、 (二氯亚砜)等氯化试剂反应可用于制取四氯化钛。
(二氯亚砜)等氯化试剂反应可用于制取四氯化钛。
① 的空间构型为
的空间构型为_____ , 中
中 键和
键和 键的数目比为
键的数目比为_____ 。
② 是
是_____ 分子。(填“极性”或“非极性”)
(3)钛的某配合物可用于催化环烯烃聚合,其结构如下图所示:
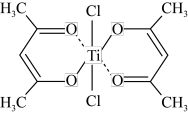
该配合物中存在的化学键有_____ (填字母)。
a.离子键 b.配位键 c.金属键 d.共价键 e.氢键
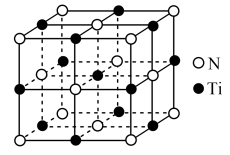
(4)氮化钛晶体的晶胞结构如图所示,该晶体结构中与 原子距离最近且相等的
原子距离最近且相等的 原子有
原子有_____ 个;若该晶胞的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶胞中
,则晶胞中 原子与
原子与 原子的最近距离为
原子的最近距离为_____  。(用含
。(用含 、
、 的代数式表示,
的代数式表示, 的相对原子质量48)
的相对原子质量48)
(5)在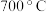 左右,将
左右,将 通过二氧化钛和炭粉的混合物可生成
通过二氧化钛和炭粉的混合物可生成 和一种含碳元素的气体,写出该反应的化学方程式
和一种含碳元素的气体,写出该反应的化学方程式_____ 。
(1)钛元素在元素周期表中的位置
(2)二氧化钛与
 (光气)、
(光气)、 (二氯亚砜)等氯化试剂反应可用于制取四氯化钛。
(二氯亚砜)等氯化试剂反应可用于制取四氯化钛。①
 的空间构型为
的空间构型为 中
中 键和
键和 键的数目比为
键的数目比为②
 是
是(3)钛的某配合物可用于催化环烯烃聚合,其结构如下图所示:

该配合物中存在的化学键有
a.离子键 b.配位键 c.金属键 d.共价键 e.氢键
(4)氮化钛晶体的晶胞结构如图所示,该晶体结构中与
 原子距离最近且相等的
原子距离最近且相等的 原子有
原子有 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶胞中
,则晶胞中 原子与
原子与 原子的最近距离为
原子的最近距离为 。(用含
。(用含 、
、 的代数式表示,
的代数式表示, 的相对原子质量48)
的相对原子质量48)
(5)在
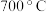 左右,将
左右,将 通过二氧化钛和炭粉的混合物可生成
通过二氧化钛和炭粉的混合物可生成 和一种含碳元素的气体,写出该反应的化学方程式
和一种含碳元素的气体,写出该反应的化学方程式
您最近半年使用:0次
6 . 工业上以菱锰矿(主要成分为MnCO3,含杂质CaCO3、FeCO3、NiCO3)为原料制取金属锰的工艺流程如下:
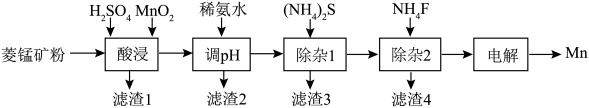
已知常温下,溶度积常数(Ksp)如下表:
(1)基态Mn2+的价层电子轨道表示式为___________ , 的空间结构为
的空间结构为___________ 。
(2)“酸浸”时,为了加快反应速率,可采取的措施有___________ (答两条),该过程一般选择硫酸而不用盐酸的原因是___________ 。
(3)“酸浸”过程中,MnO2发生的主要反应的离子方程式为___________ 。
(4)常温下,加稀氨水时调pH约为4,则滤渣2的主要成分是___________ 。
(5)“除杂1”时加入适量的(NH4)2S,除去的主要离子为___________ ,过滤后得到的滤液中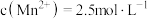 ,则其
,则其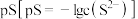 的范围是
的范围是___________ 。

已知常温下,溶度积常数(Ksp)如下表:
 |  |  |  |  |  |
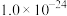 | 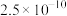 | 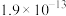 |  | 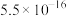 | 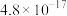 |
(1)基态Mn2+的价层电子轨道表示式为
 的空间结构为
的空间结构为(2)“酸浸”时,为了加快反应速率,可采取的措施有
(3)“酸浸”过程中,MnO2发生的主要反应的离子方程式为
(4)常温下,加稀氨水时调pH约为4,则滤渣2的主要成分是
(5)“除杂1”时加入适量的(NH4)2S,除去的主要离子为
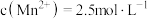 ,则其
,则其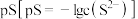 的范围是
的范围是
您最近半年使用:0次
解题方法
7 . 按要求回答下列问题:
(1)前三周期元素中,基态原子核外有7组成对电子的原子,其价层电子的轨道表示式为___________ 。
(2)已知H2O2的沸点为152℃,H2S的沸点-60.4℃。请解释两者沸点差异的原因___________ 。
(3)BF3和NaBF4是硼的重要化合物,微粒中F-B-F键角:BF3___________  (填“>”、“<”或“=” )。理由是
(填“>”、“<”或“=” )。理由是___________ 。
(4)将CH3COOH、FCH2COOH、CH3CH2COOH的酸性由强到弱排序___________ ,并解释原因___________ 。
(1)前三周期元素中,基态原子核外有7组成对电子的原子,其价层电子的轨道表示式为
(2)已知H2O2的沸点为152℃,H2S的沸点-60.4℃。请解释两者沸点差异的原因
(3)BF3和NaBF4是硼的重要化合物,微粒中F-B-F键角:BF3
 (填“>”、“<”或“=” )。理由是
(填“>”、“<”或“=” )。理由是(4)将CH3COOH、FCH2COOH、CH3CH2COOH的酸性由强到弱排序
您最近半年使用:0次
名校
8 . 类推是化学学习和研究中常用的思维方法。下列类推正确的是
A. 为直线形分子,则 为直线形分子,则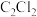 也为直线形分子 也为直线形分子 |
| B.N原子之间可以形成N=N,则P原子之间也可形成P=P |
C. 分子的空间结构为V形,则 分子的空间结构为V形,则 的VSEPR模型也是V形 的VSEPR模型也是V形 |
D.基态V的价层电子排布式为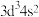 ,基态Cr的价层电子排布式为 ,基态Cr的价层电子排布式为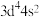 |
您最近半年使用:0次
2024-04-01更新
|
267次组卷
|
2卷引用:辽宁省朝阳市建平县实验中学2023-2024学年高二上学期期末化学试题
解题方法
9 . 下列化学用语错误的是
A.TNT的结构简式: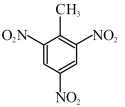 | B.基态 的简化电子排布式: 的简化电子排布式: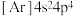 |
C.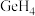 的VSEPR模型: 的VSEPR模型: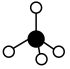 | D. 的电子式: 的电子式: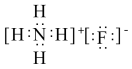 |
您最近半年使用:0次
10 . 我国在商代或更早就掌握了冶炼铜的技术。以黄铜矿为原料冶炼铜涉及多个反应,其中一个反应为 。
。
(1)基态 的电子排布式为
的电子排布式为___________ ,从原子结构角度上解释,高温下 能转化为
能转化为 的原因是
的原因是___________ 。铜、铁两类原子核外电子运动状态相差___________ 种。
(2) 四种含硫微粒中,中心原子为
四种含硫微粒中,中心原子为 杂化的是
杂化的是___________
(3) 晶胞结构如图1所示。晶胞中
晶胞结构如图1所示。晶胞中 的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1的坐标分数为(
的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1的坐标分数为( ),则原子2的分数坐标为
),则原子2的分数坐标为___________ ;
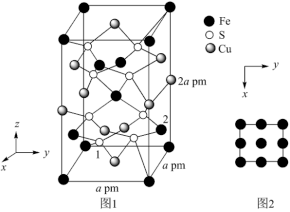
 。
。(1)基态
 的电子排布式为
的电子排布式为 能转化为
能转化为 的原因是
的原因是(2)
 四种含硫微粒中,中心原子为
四种含硫微粒中,中心原子为 杂化的是
杂化的是(3)
 晶胞结构如图1所示。晶胞中
晶胞结构如图1所示。晶胞中 的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1的坐标分数为(
的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1的坐标分数为( ),则原子2的分数坐标为
),则原子2的分数坐标为
您最近半年使用:0次



