名校
1 . 下列图示或化学用语表示不正确 的是
| A | B |
|
|
| 乙炔的空间结构模型 |  的VSEPR模型 的VSEPR模型 |
| C | D |
|
|
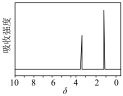
| 反-2-丁烯的结构简式 | 乙醇的核磁共振氢谱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 请按要求完成填空:
(1)完成下表中的空白:
(2)配合物[Cu(NH3)4]SO4的中心离子是___________ 、配体是___________ 、配位原子是___________ 、配位数是___________ 。
(1)完成下表中的空白:
| 粒子 | 中心原子孤电子对数 | 中心原子的杂化轨道类型 | VSEPR模型 | 空间结构 |
| CO2 | ① | ② | ③ | ④ |
SO | ⑤ | ⑥ | ⑦ | ⑧ |
您最近一年使用:0次
名校
解题方法
3 . “可燃冰”的主要气体成分是甲烷,又称甲烷水合物,外形像冰,存在于海底和大陆冰川或永久冻土底部,是巨大的潜在能源。
(1)研究甲烷分子的结构
①碳原子价层电子轨道表示式是___________ 。
②能说明或解释甲烷分子是正四体形空间结构的是___________ (填序号)。
a.二氯甲烷没有同分异构体
b.4个CH的键长相同,H—C—H的键角均为109°28'
c.碳原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个C—H 键
键
(2)研究水分子的结构
①H2O的VESPR模型为___________ 。
②H2O的H—O—H键角小于CH4的H—C—H键角,原因是___________ 。
(1)研究甲烷分子的结构
①碳原子价层电子轨道表示式是
②能说明或解释甲烷分子是正四体形空间结构的是
a.二氯甲烷没有同分异构体
b.4个CH的键长相同,H—C—H的键角均为109°28'
c.碳原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个C—H
 键
键(2)研究水分子的结构
①H2O的VESPR模型为
②H2O的H—O—H键角小于CH4的H—C—H键角,原因是
您最近一年使用:0次
解题方法
4 . 下列关于物质的结构或性质以及解释均正确的是
| 选项 | 物质的结构或性质 | 解释 |
| A | 键角:NH3>BF3 | NH3中N的孤电子对数比BF3中B的孤电子对数多 |
| B | 酸性:CF3COOH>CCl3COOH | F的电负性大于Cl的电负性,使CF3COOH中羧基上的氢更易电离 |
| C | 熔点:碳化硅>金刚石 | C﹣Si键能大于C﹣C键能 |
| D | 稳定性:H2O>CH4 | H2O分子之间除了范德华力以外还存在氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 硅烷广泛应用在现代高科技领域。
制备硅烷的反应为 。
。
(1)①基态硅原子的价层电子轨道表示式为___________ 。
② 中,硅的化合价为+4价。硅显正化合价的原因是
中,硅的化合价为+4价。硅显正化合价的原因是___________ 。
③下列说法正确的是___________ (填字母)。
a. 的稳定性比
的稳定性比 的差
的差
b. 中4个
中4个 的键长相同,
的键长相同, 的键角为
的键角为
c. 中硅原子以4个
中硅原子以4个 杂化轨道分别与4个氢原子的
杂化轨道分别与4个氢原子的 轨道重叠,形成4个
轨道重叠,形成4个 键
键
④ 的沸点(-86℃)高于
的沸点(-86℃)高于 的沸点(-112℃),原因是
的沸点(-112℃),原因是___________ 。
(2) 的晶胞结构如图所示,晶胞的体积为
的晶胞结构如图所示,晶胞的体积为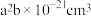 。
。 的
的 模型名称为
模型名称为___________ 。
②用 表示阿伏伽德罗常数的值。
表示阿伏伽德罗常数的值。 晶体密度为
晶体密度为___________  (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
制备硅烷的反应为
 。
。(1)①基态硅原子的价层电子轨道表示式为
②
 中,硅的化合价为+4价。硅显正化合价的原因是
中,硅的化合价为+4价。硅显正化合价的原因是③下列说法正确的是
a.
 的稳定性比
的稳定性比 的差
的差b.
 中4个
中4个 的键长相同,
的键长相同, 的键角为
的键角为
c.
 中硅原子以4个
中硅原子以4个 杂化轨道分别与4个氢原子的
杂化轨道分别与4个氢原子的 轨道重叠,形成4个
轨道重叠,形成4个 键
键④
 的沸点(-86℃)高于
的沸点(-86℃)高于 的沸点(-112℃),原因是
的沸点(-112℃),原因是(2)
 的晶胞结构如图所示,晶胞的体积为
的晶胞结构如图所示,晶胞的体积为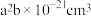 。
。
 的
的 模型名称为
模型名称为②用
 表示阿伏伽德罗常数的值。
表示阿伏伽德罗常数的值。 晶体密度为
晶体密度为 (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
6 . 随着科学的发展,氟及其化合物的用途日益广泛。
I.离子液体具有电导率高、化学稳定性高等优点,在电化学领域用途广泛。某离子液体的结构简式如图。 是制备此离子液体的原料。
是制备此离子液体的原料。
(1)微粒中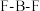 键角:
键角:
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(2) 可以与
可以与 反应生成
反应生成 的原因是
的原因是___________ 。
Ⅱ.氟化镁钾( )是一种具有优良光学性能的材料,其晶胞结构如下。以该晶胞结构为基础,将相似离子取代或部分取代,可合成多种新型材料。
)是一种具有优良光学性能的材料,其晶胞结构如下。以该晶胞结构为基础,将相似离子取代或部分取代,可合成多种新型材料。 晶体中,每个
晶体中,每个 周围有
周围有___________ 个距离最近的F。
(4) 半径与
半径与 接近,将
接近,将 部分由
部分由 取代,可以带来电荷不平衡性和反应活性。从而合成新型催化剂材料。
取代,可以带来电荷不平衡性和反应活性。从而合成新型催化剂材料。
①基态 价电子的轨道表示式为
价电子的轨道表示式为___________ 。
②某实验室合成新型催化剂材料 (
( 是平衡电荷引入的填隙阴离子,不破坏原有晶胞结构)。已知晶胞棱长为
是平衡电荷引入的填隙阴离子,不破坏原有晶胞结构)。已知晶胞棱长为 。若要合成厚度为
。若要合成厚度为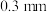 、面积为
、面积为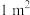 的催化剂材料,理论上需要掺杂的
的催化剂材料,理论上需要掺杂的 约为
约为___________  (
(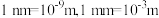 ,阿伏加德罗常数约为
,阿伏加德罗常数约为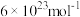 )。
)。
(5)我国科研工作者以 晶体结构为框架,依据“体积匹配原则”合成了具有独特电学性能的
晶体结构为框架,依据“体积匹配原则”合成了具有独特电学性能的 晶体。其框架中的
晶体。其框架中的 由
由 取代,
取代, 位置嵌入有机阳离子
位置嵌入有机阳离子 ,
, 位置沿棱方向嵌入直线型
位置沿棱方向嵌入直线型 。已知
。已知 与
与 的结构简式如下:
的结构简式如下: 中N原子的杂化方式为
中N原子的杂化方式为___________ , 中心N原子的杂化方式为
中心N原子的杂化方式为___________ 。
② 的转动不会影响晶体骨架,这是因为除离子键外,该晶体中微粒间还存在着其他相互作用。如邻近的
的转动不会影响晶体骨架,这是因为除离子键外,该晶体中微粒间还存在着其他相互作用。如邻近的 与
与 还存在着
还存在着___________ ,上述相互作用不会随 的转动改变。
的转动改变。
I.离子液体具有电导率高、化学稳定性高等优点,在电化学领域用途广泛。某离子液体的结构简式如图。
 是制备此离子液体的原料。
是制备此离子液体的原料。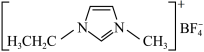
(1)微粒中
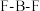 键角:
键角:
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(2)
 可以与
可以与 反应生成
反应生成 的原因是
的原因是Ⅱ.氟化镁钾(
 )是一种具有优良光学性能的材料,其晶胞结构如下。以该晶胞结构为基础,将相似离子取代或部分取代,可合成多种新型材料。
)是一种具有优良光学性能的材料,其晶胞结构如下。以该晶胞结构为基础,将相似离子取代或部分取代,可合成多种新型材料。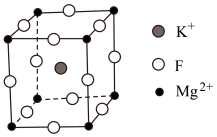
 晶体中,每个
晶体中,每个 周围有
周围有(4)
 半径与
半径与 接近,将
接近,将 部分由
部分由 取代,可以带来电荷不平衡性和反应活性。从而合成新型催化剂材料。
取代,可以带来电荷不平衡性和反应活性。从而合成新型催化剂材料。①基态
 价电子的轨道表示式为
价电子的轨道表示式为②某实验室合成新型催化剂材料
 (
( 是平衡电荷引入的填隙阴离子,不破坏原有晶胞结构)。已知晶胞棱长为
是平衡电荷引入的填隙阴离子,不破坏原有晶胞结构)。已知晶胞棱长为 。若要合成厚度为
。若要合成厚度为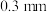 、面积为
、面积为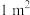 的催化剂材料,理论上需要掺杂的
的催化剂材料,理论上需要掺杂的 约为
约为 (
(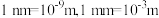 ,阿伏加德罗常数约为
,阿伏加德罗常数约为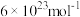 )。
)。(5)我国科研工作者以
 晶体结构为框架,依据“体积匹配原则”合成了具有独特电学性能的
晶体结构为框架,依据“体积匹配原则”合成了具有独特电学性能的 晶体。其框架中的
晶体。其框架中的 由
由 取代,
取代, 位置嵌入有机阳离子
位置嵌入有机阳离子 ,
, 位置沿棱方向嵌入直线型
位置沿棱方向嵌入直线型 。已知
。已知 与
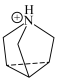
与 的结构简式如下:
的结构简式如下: :
:
 :
: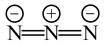
 中N原子的杂化方式为
中N原子的杂化方式为 中心N原子的杂化方式为
中心N原子的杂化方式为②
 的转动不会影响晶体骨架,这是因为除离子键外,该晶体中微粒间还存在着其他相互作用。如邻近的
的转动不会影响晶体骨架,这是因为除离子键外,该晶体中微粒间还存在着其他相互作用。如邻近的 与
与 还存在着
还存在着 的转动改变。
的转动改变。
您最近一年使用:0次
名校
解题方法
7 . 下列分子或离子的 模型与其空间结构不一致的是
模型与其空间结构不一致的是
 模型与其空间结构不一致的是
模型与其空间结构不一致的是A. | B. | C.SO2 | D. |
您最近一年使用:0次
名校
解题方法
8 . 下列化学用语或图示表达正确的是
A.HClO的电子式为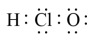 |
B.基态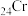 原子的价层电子轨道表示式为 原子的价层电子轨道表示式为 |
C.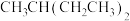 的名称为2—乙基丁烷 的名称为2—乙基丁烷 |
D. 分子的VSEPR模型为 分子的VSEPR模型为 |
您最近一年使用:0次
2024-04-04更新
|
1106次组卷
|
5卷引用:北京市第八中学2023-2024学年高三下学期零模化学试题
北京市第八中学2023-2024学年高三下学期零模化学试题北京师范大学附属中学2023-2024学年高三下学期统练 化学试题(已下线)题型2 有关化学用语的正误判断(25题)-2024年高考化学常考点必杀300题(新高考通用)重庆市名校联盟2023-2024学年高三下学期全真模拟考试化学试题山东省惠民县2023-2024学年高二下学期期中考试化学试题
名校
解题方法
9 . 过渡金属氧化物离子(以MO+表示)在烃类的选择性氧化等方面应用广泛。MO+与CH4反应的过程如下图所示。不正确 的是
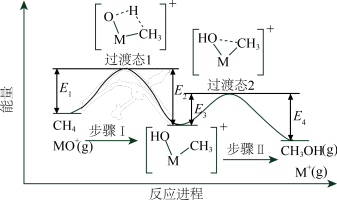
| A.反应速率:步骤I<步骤II |
| B.CH3OH分子中,键角:H—C—H>H—O—C |
| C.若MO+与CH3D反应,生成的氘代甲醇有2种 |
D.CH4(g) + MO+(g)=CH3OH(g) + M+(g)  = E2+E4-E1-E3 = E2+E4-E1-E3 |
您最近一年使用:0次
2024-04-01更新
|
609次组卷
|
5卷引用:北京市丰台区2023-2024学年高三下学期综合练习(一)化学试题
北京市丰台区2023-2024学年高三下学期综合练习(一)化学试题(已下线)通关练08 聚焦反应热、速率及化学平衡-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)江苏省常州市第一中学2023-2024学年高二下学期4月期中考试化学试题(已下线)化学(天津卷03)-2024年高考化学押题预测卷(已下线)提升练03 反应历程探究与催化原理-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
名校
解题方法
10 . 尿素CO(NH2)2是一种高效化肥和化工原料。反应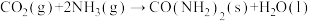 可用于尿素的制备。下列有关说法正确的是
可用于尿素的制备。下列有关说法正确的是
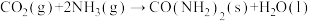 可用于尿素的制备。下列有关说法正确的是
可用于尿素的制备。下列有关说法正确的是| A.CO2分子为极性分子 | B.NH3分子的空间结构为平面三角形 |
C.H2O分子的空间填充模型 | D.尿素分子σ键和π键的数目之比为7:1 |
您最近一年使用:0次