名校
解题方法
1 . 根据杂化轨道理论和价层电子对互斥模型判断,下列各项正确的是
| 选项 | 分子或离子 | 中心原子的杂化方式 | 价电子对分布的几何构型 | 分子或离子的空间结构 |
| A |  |  | 四面体形 | V形 |
| B |  |  | 平面三角形 | 三角锥形 |
| C | 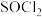 |  | 四面体形 | 三角锥形 |
| D |  |  | 平面三角形 | 平面三角形 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-08-22更新
|
231次组卷
|
6卷引用:山东省滨州市无棣县2020-2021学年高二下学期期中考试化学试题
名校
解题方法
2 . 硫及其化合物有许多用途,相关物质的物理常数如下表所示:
回答下列问题:
(1)基态S原子价层电子的电子排布图(轨道表达式)为_______ ,其电子占据最高能级的电子云轮廓图为_______ 形。
(2)根据价层电子对互斥理论, 、
、 、
、 的气态分子中,中心原子价层电子对数不同其他分子的是
的气态分子中,中心原子价层电子对数不同其他分子的是_______ 。
(3)气态三氧化硫以单分子形式存在,其分子的立体构型为_______ 形;固体三氧化硫中存在如下图所示的三聚分子,该分子中S原子的杂化轨道类型为_______ 。
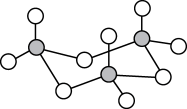
(4)已知亚硫酸根的键角小于硫酸根的键角,请用相关理论解释原因:_______ 。
(5)已知含量酸的酸性与结构中非羟基氧的数目有关,强酸一般有两个非羟基氧(如硫酸: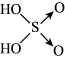 ),中强酸一般有一个非羟基氧(如磷酸:
),中强酸一般有一个非羟基氧(如磷酸: )。已知亚磷酸(H3PO3)是一种二元中强酸。
)。已知亚磷酸(H3PO3)是一种二元中强酸。
①请写出亚磷酸的结构式_______ 。
② 与过量的
与过量的 溶液反应的离子方程式为
溶液反应的离子方程式为_______ 。
| H2S | SO2 | SO3 | H2SO4 | |
| 熔点/℃ | -85.5 | -75.5 | 16.8 | 10.3 |
| 沸点/℃ | -60.3 | -10.0 | 45.0 | 337.0 |
回答下列问题:
(1)基态S原子价层电子的电子排布图(轨道表达式)为
(2)根据价层电子对互斥理论,
 、
、 、
、 的气态分子中,中心原子价层电子对数不同其他分子的是
的气态分子中,中心原子价层电子对数不同其他分子的是(3)气态三氧化硫以单分子形式存在,其分子的立体构型为

(4)已知亚硫酸根的键角小于硫酸根的键角,请用相关理论解释原因:
(5)已知含量酸的酸性与结构中非羟基氧的数目有关,强酸一般有两个非羟基氧(如硫酸:
 ),中强酸一般有一个非羟基氧(如磷酸:
),中强酸一般有一个非羟基氧(如磷酸: )。已知亚磷酸(H3PO3)是一种二元中强酸。
)。已知亚磷酸(H3PO3)是一种二元中强酸。①请写出亚磷酸的结构式
②
 与过量的
与过量的 溶液反应的离子方程式为
溶液反应的离子方程式为
您最近一年使用:0次
名校
解题方法
3 . 下列中物质中所原子都在同一平面上的是
| A.NH3 | B.CH4 | C.BF3 | D. |
您最近一年使用:0次
2021-12-21更新
|
336次组卷
|
4卷引用:四川省遂宁市射洪中学2021—2022学年高二上学期期中考试化学试题
四川省遂宁市射洪中学2021—2022学年高二上学期期中考试化学试题(已下线)第2.2.1讲 分子结构的测定和多样性 价层电子对互斥模型-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试化学试题(已下线)黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试变式汇编(1-10)
名校
4 . 短周期的四种元素位置如图所示,若四种元素的核电荷数之和为52,则与四种元素推断相关的描述不正确的是
| D | ||
| A | B | C |
| A.A的最高价氧化物用于制作光导纤维 |
| B.B的最高价氧化物的水化物是一种强酸 |
| C.C至少有两种价态的氧化物 |
| D.D简单氢化物的VSEPR模型为四面体型 |
您最近一年使用:0次
解题方法
5 . 锆是冶金工业的“维生素”,它与氧族元素(O、S、Se、Te)形成的化合物在材料工业中应用广泛。其中碲化锆(ZrTe2)和硒化锆(ZrSe2)均为新型材料,氧化锆(ZrO2)具有特殊的热电性,氧化锆常用作陶瓷绝缘材料和陶瓷遮光剂。
(1)氧族元素各基态原子第一电离能随原子序数增大依次减小的原因为________ 。
(2)Zr(ClO4)4是一种常见的锆盐, 的空间构型为
的空间构型为_______ ,其中Cl原子的杂化方式为_______ 。
(3)如图为硒化锆的分子结构(图甲)和氧化锆的晶胞结构(图乙)。
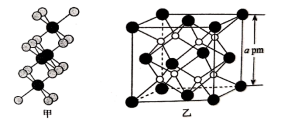
①硒化锆的沸点远低于氧化锆,原因为_______ ,硒化锆和氧化锆的配位数分别为_______ 、______ 。
②已知阿伏加德罗常数的值为NA,据图乙中数据计算氧化锆的密度为_______ g‧cm-3(用含NA和a的代数式表示,列式即可)
(1)氧族元素各基态原子第一电离能随原子序数增大依次减小的原因为
(2)Zr(ClO4)4是一种常见的锆盐,
 的空间构型为
的空间构型为(3)如图为硒化锆的分子结构(图甲)和氧化锆的晶胞结构(图乙)。

①硒化锆的沸点远低于氧化锆,原因为
②已知阿伏加德罗常数的值为NA,据图乙中数据计算氧化锆的密度为
您最近一年使用:0次
名校
解题方法
6 . 下列关于物质结构的说法错误的是
| A.铝晶体中微粒间的作用力没有方向性和饱和性 |
B.CH4和 都是正四面体结构,键角均为109°28' 都是正四面体结构,键角均为109°28' |
C.氨基氰(NH2CN)分子内 键与 键与 键数目之比为2:1 键数目之比为2:1 |
| D.甲醛(HCHO)的键角约为120°,分子之间存在氢键 |
您最近一年使用:0次
2021-09-29更新
|
327次组卷
|
8卷引用:安徽省宿州市十三所重点中学2020-2021学年高二下学期期中质量检测化学试题
安徽省宿州市十三所重点中学2020-2021学年高二下学期期中质量检测化学试题山东省新泰市第一中学东校2020-2021学年高二下学期期中考试化学试题 山东省泰安市2021届高考第二次模拟化学试题山东省泰安第一中学2021届高三二轮检测化学试题(已下线)专题13 物质结构与性质基础-备战2022年高考化学真题及地市好题专项集训【山东专用】(已下线)押新高考卷08题 物质结构与性质-备战2022年高考化学临考题号押题(新高考通版)(已下线)卷01 小题素养卷-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)山东省济南市山东省实验中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
7 . 下列说法正确的是
| A.非极性分子往往具有高度对称性,如BF3、PCl5、H2O2、CO2这样的分子 |
| B.熔融状态的HgCl2不能导电,HgCl2的稀溶液有弱的导电能力且可作手术刀的消毒液,从不同角度分类HgCl2是一种共价化合物、非电解质、盐、离子晶体 |
| C.BeF2和SF2分子的VSEPR模型分别为直线形和V形 |
D.乳酸( )分子中含有一个手性碳原子 )分子中含有一个手性碳原子 |
您最近一年使用:0次
名校
解题方法
8 . 用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,有时也能用来推测键角大小,下列判断正确的是
| A.SO2、CS2、HCN都是直线形的分子 | B.BF3键角为120°,SnBr2键角大于120° |
C.CH2O、CO 、SO3都是平面三角形的粒子 、SO3都是平面三角形的粒子 | D.PCl3、NH3、PCl5都是三角锥形的分子 |
您最近一年使用:0次
名校
解题方法
9 . 下列粒子的VSEPR模型为四面体,且空间构型结构为V型的是
| A.H2O | B.NF3 | C.H3O+ | D.SO2 |
您最近一年使用:0次
10 . X、Y、Z、W是原子序数依次增大的前四周期元素,X元素有1个2p空轨道,Y为同周期离子半径最小的金属元素,Z元素原子的最外层电子数比次外层电子数少2,W的内层电子已全充满,最外层只有2个电子。请回答下列问题:
(1)X能与氢、氮、氧三种元素构成化合物XO(NH2)2,该化合物分子中的σ键与π键的个数之比是___ ;该物质易溶于水的主要原因是___ 。
(2)元素Z的最高价氧化物中,Z原子的杂化方式是___ ,分子的空间构型是___ 。
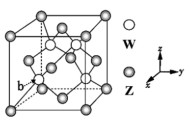
(3)元素Z.与W形成的某种化合物的晶胞结构如图所示,则该化合物的化学式为___ 。原子的分数坐标,即将晶胞参数均看做“1”所得出的三维空间坐标,则晶胞中b原子的分数坐标为___ 。
(4)Y的氯化物气态时通常以二聚分子形式存在,分子式为Y2Cl6,分子中所有原子均达到8电子稳定结构,则Y2Cl6的结构式为___ 。
(1)X能与氢、氮、氧三种元素构成化合物XO(NH2)2,该化合物分子中的σ键与π键的个数之比是
(2)元素Z的最高价氧化物中,Z原子的杂化方式是
(3)元素Z.与W形成的某种化合物的晶胞结构如图所示,则该化合物的化学式为

(4)Y的氯化物气态时通常以二聚分子形式存在,分子式为Y2Cl6,分子中所有原子均达到8电子稳定结构,则Y2Cl6的结构式为
您最近一年使用:0次



