名校
解题方法
1 . 回答下列问题。
(1)基态B原子核外电子有___________ 种运动状态。
(2)基态铜原子的电子排布式是___________ ;高温超导材料镧钡铜氧化物中含有Cu3+。基态时Cu3+ 的电子排布式为[Ar]___________ 。
(3)Fe4[Fe(CN)6]3是较早发现的CN- 配合物,其中铁元素呈现两种不同的价态。配离子的中心原子核外电子排布式为___________ 。
(4)[B(OH)4]-中氧原子的杂化轨道类型为___________ ,[B(OH)4]-的空间构型为___________ 。
(5)基态氧原子的价层电子排布式不能表示为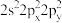 ,因为这违背了
,因为这违背了___________ (填选项)。
A.泡利原理 B.洪特规则 C.能量最低原理
(1)基态B原子核外电子有
(2)基态铜原子的电子排布式是
(3)Fe4[Fe(CN)6]3是较早发现的CN- 配合物,其中铁元素呈现两种不同的价态。配离子的中心原子核外电子排布式为
(4)[B(OH)4]-中氧原子的杂化轨道类型为
(5)基态氧原子的价层电子排布式不能表示为
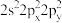 ,因为这违背了
,因为这违背了A.泡利原理 B.洪特规则 C.能量最低原理
您最近一年使用:0次
解题方法
2 . 硅及其化合物在工业中有很多用处,一些硅的卤化物的熔点如表所示:
完成下列填空:
(1)硅原子核外电子共有______ 种形状不同的电子云,画出基态硅原子最外层电子的轨道表示式______ 。
(2)表中四种卤化物分子的空间结构均为______ ,由此推断 的键角为
的键角为______ , 属于
属于______ (填“极性”或“非极性”)分子。
(3)已知 (熔点为-56.6℃)和
(熔点为-56.6℃)和 (熔点为1713℃)熔点相差较大;原因是
(熔点为1713℃)熔点相差较大;原因是______ ,表中四种卤化硅熔点存在差异的原因是______ 。
完成下列填空:
卤化物 |
|
|
|
|
熔点/℃ | -90.2 | 70.4 | 5.2 | 120.5 |
(1)硅原子核外电子共有
(2)表中四种卤化物分子的空间结构均为
 的键角为
的键角为 属于
属于(3)已知
 (熔点为-56.6℃)和
(熔点为-56.6℃)和 (熔点为1713℃)熔点相差较大;原因是
(熔点为1713℃)熔点相差较大;原因是
您最近一年使用:0次
解题方法
3 . 已知W、X、Y、Z、N是周期表中前四周期元素,它们的核电荷数依次增大。
回答下列问题:
(1)写出X的元素符号:X______ 。
(2)基态Y原子价电子的电子排布式:______ 。
(3)W、X、Z三种元素的电负性由大到小的顺序是______ (填元素符号)。
(4)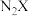 和
和 的熔点更高的是
的熔点更高的是______ (填化学式),原因是:______ 。
(5)根据价层电子对互斥理论, 的空间构型为
的空间构型为______ , 中心原子的杂化方式为
中心原子的杂化方式为______ , 和
和 中键角较小的是
中键角较小的是______ (用离子符号表示)。
元素 | 元素性质或原子结构或离子结构 |
W | 原子核内无中子 |
X | 基态原子核外s能级上的电子总数与p能级上的电子总数相等 |
Y | 元素的原子半径在同周期中最大 |
Z | 基态原子核外有9种不同空间运动状态的电子,且有两个未成对电子 |
N |
|
(1)写出X的元素符号:X
(2)基态Y原子价电子的电子排布式:
(3)W、X、Z三种元素的电负性由大到小的顺序是
(4)
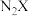 和
和 的熔点更高的是
的熔点更高的是(5)根据价层电子对互斥理论,
 的空间构型为
的空间构型为 中心原子的杂化方式为
中心原子的杂化方式为 和
和 中键角较小的是
中键角较小的是
您最近一年使用:0次
名校
4 . 按下列要求填空
(1)基态某原子的最外层电子排布式是 ,推断该元素位于第
,推断该元素位于第_____ 周期第____ 族,在元素周期表中属于____ 区。
(2)基态某原子的价层电子排布式为 ,在元素周期表中属于
,在元素周期表中属于_______ 区。
(3) 杂化类型为
杂化类型为_______ ,VSEPR模型为_______ ,离子空间构型为_______ 。
(1)基态某原子的最外层电子排布式是
 ,推断该元素位于第
,推断该元素位于第(2)基态某原子的价层电子排布式为
 ,在元素周期表中属于
,在元素周期表中属于(3)
 杂化类型为
杂化类型为
您最近一年使用:0次
名校
解题方法
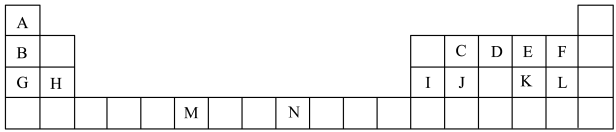
5 . 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
(1)表中元素,电负性最强的是___________ (填元素符号),J的元素名称为___________ 。N基态原子核外能级上有___________ 未成对电子。
(2)D元素原子的价电子排布图为___________ ,核外有___________ 种不同运动状态的电子。
(3)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是___________ (填“极性”或“非极性”)分子。
(4)C元素是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是___________ (填字母)。
(1)表中元素,电负性最强的是
(2)D元素原子的价电子排布图为
(3)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是
(4)C元素是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是
a.  b. CH4 c.CH2=CHCH3 d. CH3CH2C≡CH
b. CH4 c.CH2=CHCH3 d. CH3CH2C≡CH
您最近一年使用:0次
6 . 回答下列问题。
(1)①比较键长大小:C-H___________ N-H___________ H-O(用“>”或“<”填空)。
②比较键能大小:C-H___________ N-H___________ H-O(用“>”或“<”填空)。
(2)乙烯分子中的碳原子均采取___________ 杂化,碳原子与氢原子形成σ键,两碳原子之间形成双键(1个___________ 键和1个___________ 键)。
(3)乙烯分子中的所有原子都位于___________ ,相邻两个键之间的夹角约为___________ 。
(4)铁原子的价层电子排布式为:___________ 。
(1)①比较键长大小:C-H
②比较键能大小:C-H
(2)乙烯分子中的碳原子均采取
(3)乙烯分子中的所有原子都位于
(4)铁原子的价层电子排布式为:
您最近一年使用:0次
解题方法
7 . 铁是一种重要的元素,在成人体中的含量达44~5g,铁的配合物在有机合成、催化等领域中发挥重要作用。
Ⅰ.Fe³⁺的配合物在溶液中呈现不同的颜色,如 呈淡紫色(稀溶液时为无色),
呈淡紫色(稀溶液时为无色),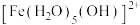 、
、 呈黄色。在黄色
呈黄色。在黄色 溶液中,加入稀
溶液中,加入稀 至溶液接近无色,再往该无色溶液加入3滴1 mol⋅L
至溶液接近无色,再往该无色溶液加入3滴1 mol⋅L NaCl溶液,溶液又变为黄色。
NaCl溶液,溶液又变为黄色。
(1)铁元素位于元素周期表的第___________ 周期第___________ 族。
(2) 中,中心离子为
中,中心离子为___________ ,配位原子是___________ ,配位数为___________ 。
(3)加入NaCl溶液后,溶液又变为黄色的原因:___________ (用离子方程式表示)。
Ⅱ. 不易被人体吸收,维生素C可帮助人体将
不易被人体吸收,维生素C可帮助人体将 转变为易吸收的
转变为易吸收的 。
。
(4)维生素C的分子结构如下图所示,分子中碳原子的杂化方式有___________ ;推测维生素C在水中的溶解性:___________ (填“难溶于水”或“易溶于水”)。
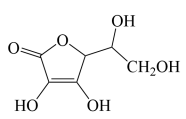
(5)根据维生素C的结构特征,分析预测其可能的化学性质,参考①的示例,完成下表。 (若不需要“可反应的试剂”,可对应填写“没有”)
②___________ 、___________ ;
③___________ 、___________ 、___________ 。
Ⅰ.Fe³⁺的配合物在溶液中呈现不同的颜色,如
 呈淡紫色(稀溶液时为无色),
呈淡紫色(稀溶液时为无色),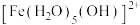 、
、 呈黄色。在黄色
呈黄色。在黄色 溶液中,加入稀
溶液中,加入稀 至溶液接近无色,再往该无色溶液加入3滴1 mol⋅L
至溶液接近无色,再往该无色溶液加入3滴1 mol⋅L NaCl溶液,溶液又变为黄色。
NaCl溶液,溶液又变为黄色。(1)铁元素位于元素周期表的第
(2)
 中,中心离子为
中,中心离子为(3)加入NaCl溶液后,溶液又变为黄色的原因:
Ⅱ.
 不易被人体吸收,维生素C可帮助人体将
不易被人体吸收,维生素C可帮助人体将 转变为易吸收的
转变为易吸收的 。
。(4)维生素C的分子结构如下图所示,分子中碳原子的杂化方式有

(5)根据维生素C的结构特征,分析预测其可能的化学性质,参考①的示例,完成下表。 (若不需要“可反应的试剂”,可对应填写“没有”)
| 序号 | 结构特征 | 可反应的试剂 | 反应类型 |
| ① | 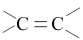 |  | 加成反应 |
| ② | 氧化反应 | ||
| ③ |
③
您最近一年使用:0次
解题方法
8 . 硼的化合物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态硼原子的价电子排布图为:___________ ;B、N、H的电负性由大到小的顺序为___________ 。
(2)科学家合成了一种含硼阴离子 ,其结构如图所示。其中硼原子的杂化方式为
,其结构如图所示。其中硼原子的杂化方式为___________ ,该结构中共有___________ 种不同化学环境的氧原子。
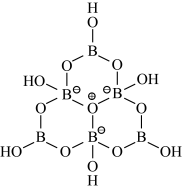
(3) 与
与 结合形成固态化合物
结合形成固态化合物 ,该物质在
,该物质在 时熔化电离出
时熔化电离出 和一含硼阴离子
和一含硼阴离子___________ (填离子符号); 空间构型为
空间构型为___________ 。
(1)基态硼原子的价电子排布图为:
(2)科学家合成了一种含硼阴离子
 ,其结构如图所示。其中硼原子的杂化方式为
,其结构如图所示。其中硼原子的杂化方式为
(3)
 与
与 结合形成固态化合物
结合形成固态化合物 ,该物质在
,该物质在 时熔化电离出
时熔化电离出 和一含硼阴离子
和一含硼阴离子 空间构型为
空间构型为
您最近一年使用:0次
9 . 已知元素 是组成物质
是组成物质 的其中一种元素。元素
的其中一种元素。元素 的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号
的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号 至
至 表示)如表所示:
表示)如表所示:
(1)元素 是
是___________ (填元素符号)。
(2)基态氮原子核外有___________ 种不同运动状态的电子,有___________ 种能量不同的电子。
(3) 中,电负性最大的元素是
中,电负性最大的元素是___________ (填元素符号), 的
的___________ 杂化轨道与 的
的 轨道形成
轨道形成___________ 键。
 是组成物质
是组成物质 的其中一种元素。元素
的其中一种元素。元素 的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号
的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号 至
至 表示)如表所示:
表示)如表所示: |  |  |  | |
电离能 | 578 | 1817 | 2745 | 11578 |
 是
是(2)基态氮原子核外有
(3)
 中,电负性最大的元素是
中,电负性最大的元素是 的
的 的
的 轨道形成
轨道形成
您最近一年使用:0次
名校
解题方法
10 . 很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物Ⅰ可与氧化汞生成化合物Ⅱ。
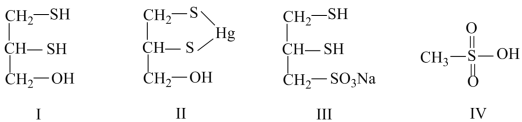
(1)1mol化合物Ⅰ含有_______ mol σ键。
(2)基态硫原子价层电子排布式为_______ 。
(3)H2S、CH4、H2O的沸点由高到低顺序为_______ 。
(4)汞的原子序数为80,位于元素周期表第_______ 周期第ⅡB族。
(5)化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有_______ 。
A.在Ⅰ中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等

(1)1mol化合物Ⅰ含有
(2)基态硫原子价层电子排布式为
(3)H2S、CH4、H2O的沸点由高到低顺序为
(4)汞的原子序数为80,位于元素周期表第
(5)化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有
A.在Ⅰ中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等
您最近一年使用:0次




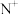 的M层全充满
的M层全充满

