名校
解题方法
1 . 药物结构的修饰有助于新药的开发与利用。由青蒿素可以获得双氢青蒿素,其变化过程示意图如图所示。下列说法错误的是

| A.青蒿素、双氢青蒿素均能发生水解反应 |
| B.双氢青蒿素分子中所有碳原子不可能共面 |
C.该过程中碳原子的杂化方式变为 |
| D.与青蒿素相比,双氢青蒿素具有更好的水溶性,疗效更佳 |
您最近一年使用:0次
2024-06-02更新
|
280次组卷
|
2卷引用:广东省华南师范大学附属中学2024届高三下学期高考适应性练习(4月)化学试题
2 . 工业合成尿素的原理:CO2+2NH3=CO(NH2)2+H2O,有关叙述表示不正确的是
| A.CO2分子中所有原子满足8电子稳定结构 |
| B.∠H-N-H:NH3>CO(NH2)2 |
| C.CO(NH2)2中N原子的杂化形式为sp3杂化 |
| D.上述反应过程中仅涉及极性共价键的断裂与形成 |
您最近一年使用:0次
名校
3 . 对如图所示两种化合物的结构或性质描述错误的是

A.均含有 键和 键和 键,且均存在采取 键,且均存在采取 和 和 杂化轨道成键的碳原子 杂化轨道成键的碳原子 |
| B.均为芳香族化合物 |
| C.二者互为同分异构体 |
| D.可用红外光谱区分,也可用核磁共振氢谱区分 |
您最近一年使用:0次
名校
4 . 有 存在时,活性炭吸附脱除NO反应的化学方程式为
存在时,活性炭吸附脱除NO反应的化学方程式为 。研究发现,活性炭的表面含有羧基等含氧官能团,化学吸附
。研究发现,活性炭的表面含有羧基等含氧官能团,化学吸附 和NO的机理如下图所示。下列说法不正确的是
和NO的机理如下图所示。下列说法不正确的是
 存在时,活性炭吸附脱除NO反应的化学方程式为
存在时,活性炭吸附脱除NO反应的化学方程式为 。研究发现,活性炭的表面含有羧基等含氧官能团,化学吸附
。研究发现,活性炭的表面含有羧基等含氧官能团,化学吸附 和NO的机理如下图所示。下列说法不正确的是
和NO的机理如下图所示。下列说法不正确的是
A. 和 和 的中心原子的杂化方式相同 的中心原子的杂化方式相同 |
B.吸附时, 中的N原子与羧基中的H原子发生作用 中的N原子与羧基中的H原子发生作用 |
C.室温时,脱除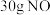 转移电子数约为 转移电子数约为 个 个 |
D.O、N、C形成的简单氢化物中,沸点最高的是 |
您最近一年使用:0次
名校
解题方法
5 . 回答下列问题。
(1)基态B原子核外电子有___________ 种运动状态。
(2)基态铜原子的电子排布式是___________ ;高温超导材料镧钡铜氧化物中含有Cu3+。基态时Cu3+ 的电子排布式为[Ar]___________ 。
(3)Fe4[Fe(CN)6]3是较早发现的CN- 配合物,其中铁元素呈现两种不同的价态。配离子的中心原子核外电子排布式为___________ 。
(4)[B(OH)4]-中氧原子的杂化轨道类型为___________ ,[B(OH)4]-的空间构型为___________ 。
(5)基态氧原子的价层电子排布式不能表示为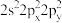 ,因为这违背了
,因为这违背了___________ (填选项)。
A.泡利原理 B.洪特规则 C.能量最低原理
(1)基态B原子核外电子有
(2)基态铜原子的电子排布式是
(3)Fe4[Fe(CN)6]3是较早发现的CN- 配合物,其中铁元素呈现两种不同的价态。配离子的中心原子核外电子排布式为
(4)[B(OH)4]-中氧原子的杂化轨道类型为
(5)基态氧原子的价层电子排布式不能表示为
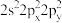 ,因为这违背了
,因为这违背了A.泡利原理 B.洪特规则 C.能量最低原理
您最近一年使用:0次
解题方法
6 . 硅及其化合物在工业中有很多用处,一些硅的卤化物的熔点如表所示:
完成下列填空:
(1)硅原子核外电子共有______ 种形状不同的电子云,画出基态硅原子最外层电子的轨道表示式______ 。
(2)表中四种卤化物分子的空间结构均为______ ,由此推断 的键角为
的键角为______ , 属于
属于______ (填“极性”或“非极性”)分子。
(3)已知 (熔点为-56.6℃)和
(熔点为-56.6℃)和 (熔点为1713℃)熔点相差较大;原因是
(熔点为1713℃)熔点相差较大;原因是______ ,表中四种卤化硅熔点存在差异的原因是______ 。
完成下列填空:
卤化物 |
|
|
|
|
熔点/℃ | -90.2 | 70.4 | 5.2 | 120.5 |
(1)硅原子核外电子共有
(2)表中四种卤化物分子的空间结构均为
 的键角为
的键角为 属于
属于(3)已知
 (熔点为-56.6℃)和
(熔点为-56.6℃)和 (熔点为1713℃)熔点相差较大;原因是
(熔点为1713℃)熔点相差较大;原因是
您最近一年使用:0次
解题方法
7 . 已知W、X、Y、Z、N是周期表中前四周期元素,它们的核电荷数依次增大。
回答下列问题:
(1)写出X的元素符号:X______ 。
(2)基态Y原子价电子的电子排布式:______ 。
(3)W、X、Z三种元素的电负性由大到小的顺序是______ (填元素符号)。
(4)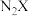 和
和 的熔点更高的是
的熔点更高的是______ (填化学式),原因是:______ 。
(5)根据价层电子对互斥理论, 的空间构型为
的空间构型为______ , 中心原子的杂化方式为
中心原子的杂化方式为______ , 和
和 中键角较小的是
中键角较小的是______ (用离子符号表示)。
元素 | 元素性质或原子结构或离子结构 |
W | 原子核内无中子 |
X | 基态原子核外s能级上的电子总数与p能级上的电子总数相等 |
Y | 元素的原子半径在同周期中最大 |
Z | 基态原子核外有9种不同空间运动状态的电子,且有两个未成对电子 |
N |
|
(1)写出X的元素符号:X
(2)基态Y原子价电子的电子排布式:
(3)W、X、Z三种元素的电负性由大到小的顺序是
(4)
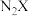 和
和 的熔点更高的是
的熔点更高的是(5)根据价层电子对互斥理论,
 的空间构型为
的空间构型为 中心原子的杂化方式为
中心原子的杂化方式为 和
和 中键角较小的是
中键角较小的是
您最近一年使用:0次
8 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.含有1mol 的水溶液中电离出来的 的水溶液中电离出来的 数目为 数目为 |
B.1mol配离子 中 中 键的数目为 键的数目为 |
C.12g金刚石中 键的数目为 键的数目为 |
D.1mol 中含有 中含有 键数目为 键数目为 |
您最近一年使用:0次
解题方法
9 . 图中1、2、3号碳原子的杂化类型分别是

A. 、 、 、 、 | B. 、 、 、 、 |
C. 、 、 、 、 | D. 、 、 、 、 |
您最近一年使用:0次
名校
10 . 微观探析是认识物质的一种途径。设 为阿伏加德罗常数,下列有关说法正确的是
为阿伏加德罗常数,下列有关说法正确的是
 为阿伏加德罗常数,下列有关说法正确的是
为阿伏加德罗常数,下列有关说法正确的是A.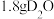 中含有的中子数目为 中含有的中子数目为 |
B.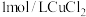 溶液中含有 溶液中含有 的数目小于 的数目小于 |
| C.1 mol CO2分子中含有2NA个σ键和2NA个sp2杂化轨道 |
D.0℃,101kPa,2.24LCl2与NaOH溶液完全反应,转移电子数目为 |
您最近一年使用:0次




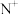 的M层全充满
的M层全充满

