名校
解题方法
1 . NA为阿伏加德罗常数的值。下列叙述错误的是
| A.0.1mol肼(H2N-NH2)含有的孤电子对数为0.2NA |
B.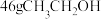 中 中 杂化的原子数为2NA 杂化的原子数为2NA |
C.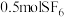 中 中 的价层电子对数为3NA 的价层电子对数为3NA |
D.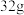 环状 环状 ( (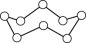 )分子中含有的 )分子中含有的 键数为 键数为 |
您最近一年使用:0次
解题方法
2 . 铁是地球上分布最广泛的金属之一,约占地壳质量的5%,仅次于氧、硅、铝,位居地壳含量第四位。蛋白琥珀酸铁(CaHbOcNdFe)口服液可以用于缺铁性贫血的治疗。请回答以下相关问题:
(1)Fe元素位于周期表中_______ 区,基态铁原子的价层电子排布式为_______ 。
(2)纳米Fe因其表面活性常用作有机催化剂,如图所示:_______ 。
②化合物N中C原子的杂化类型为_______ 。
③C、N、O的第一电离能由小到大的顺序为_______ 。
(3)将C、N、O三种元素最简单氢化物按照键角从大到小排序_______ 。
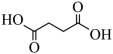
(4)琥珀酸的结构如图所示,写出琥珀酸分子中σ键与π键的个数比_______ 。_______ 。
(6)铁有多种同素异形体,在910-1400℃范围内,铁以面心立方最密堆积存在,如图为面心立方堆积的铁的晶胞。已知铁的摩尔质量为Mg/mol,NA表示阿伏加德罗常数,铁原子的半径为rpm,铁晶胞密度的表达式为_______ g•cm-3.(用含M、NA、r的代数式表示)
(1)Fe元素位于周期表中
(2)纳米Fe因其表面活性常用作有机催化剂,如图所示:
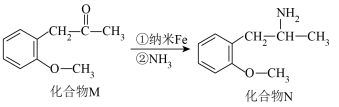
②化合物N中C原子的杂化类型为
③C、N、O的第一电离能由小到大的顺序为
(3)将C、N、O三种元素最简单氢化物按照键角从大到小排序
(4)琥珀酸的结构如图所示,写出琥珀酸分子中σ键与π键的个数比
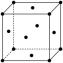
(6)铁有多种同素异形体,在910-1400℃范围内,铁以面心立方最密堆积存在,如图为面心立方堆积的铁的晶胞。已知铁的摩尔质量为Mg/mol,NA表示阿伏加德罗常数,铁原子的半径为rpm,铁晶胞密度的表达式为
您最近一年使用:0次
名校
解题方法
3 . 秦始皇帝陵博物院首次在兵马俑的彩绘中发现了古人人工合成的“中国蓝”“中国紫”颜料。通过对这些颜料的研究发现,其成分主要是钡和铜的硅酸盐(BaCuSixOy) 。
回答下列问题:
(1)“中国蓝”的发色与硫酸铜溶液呈天蓝色类似,都是由于形成了[Cu(H2O)4]2+,该配离子中Cu2+提供_______ ,配位原子是_______ ,1 mol [Cu(H2O)4]2+中σ键的数目为_________ 。
(2)写出向硫酸铜溶液里逐滴加入氨水过程中沉淀溶解的离子方程式_______________ ,再向溶液中加入乙醇,会析出深蓝色晶体____________ (写出化学式)。
(3)“中国蓝”“中国紫”中存在 四面体结构,其中Si原子采取的杂化方式为
四面体结构,其中Si原子采取的杂化方式为_______ 。
(4)BaO的熔沸点_____ MgO(填“>”“<”“=”),原因是______________ 。
(5)立方CuO晶胞结构如图所示。其中Cu2+的配位数为_______ 。NA代表阿伏加德罗常数的值,晶胞参数为a pm,则其晶体密度为___________ g·cm-3。
回答下列问题:
(1)“中国蓝”的发色与硫酸铜溶液呈天蓝色类似,都是由于形成了[Cu(H2O)4]2+,该配离子中Cu2+提供
(2)写出向硫酸铜溶液里逐滴加入氨水过程中沉淀溶解的离子方程式
(3)“中国蓝”“中国紫”中存在
 四面体结构,其中Si原子采取的杂化方式为
四面体结构,其中Si原子采取的杂化方式为(4)BaO的熔沸点
(5)立方CuO晶胞结构如图所示。其中Cu2+的配位数为

您最近一年使用:0次
名校
解题方法
4 . 离子液体是指由体积较大的阴、阳离子组成,并且在室温或接近室温下呈液态的盐,也称为低温熔融盐。有许多优点例如难挥发,有良好的导电性,可作溶剂、电解质、催化剂等。1-正丁基-3-甲基咪唑六氟磷酸盐是一种离子液体,结构简式如图,下列关于它的叙述正确的是

A.该新型化合物含有的C、N、P元素均为 杂化 杂化 |
| B.1-正丁基-3-甲基咪唑六氟磷酸盐属于含共价键的 离子化合物 |
| C.第一电离能:F<N<C |
| D.该新型化合物的组成元素全部位于元素周期表p区 |
您最近一年使用:0次
5 . 、臭氧 在
在 催化下能将烟气中的
催化下能将烟气中的 、
、 分别氧化为
分别氧化为 和
和 ,
, 也可在其他条件下被还原为
也可在其他条件下被还原为 。
。
(1)基态铁原子有___________ 种空间运动状态不同的电子; 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为___________ ; 的空间构型为
的空间构型为___________ (用文字描述); 为
为___________ 分子(填“极性”、“非极性”)。
(2)碘的四氯化碳溶液为紫红色,加入浓碘化钾水溶液,振荡后溶液紫色变浅,请用离子方程式说明原因___________ 。
(3)硫单质的常见形式为 ,其环状结构如图所示,
,其环状结构如图所示, 中含有
中含有___________ 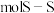 键。
键。 的熔点为1090℃,远高于
的熔点为1090℃,远高于 的192℃,由此可以判断铝氟之间的化学键为
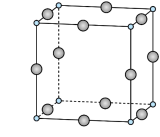
的192℃,由此可以判断铝氟之间的化学键为___________ 键。 结构属立方晶系,晶胞如图所示,
结构属立方晶系,晶胞如图所示, 的配位数为。若晶胞参数为
的配位数为。若晶胞参数为 ,晶体密度
,晶体密度
___________  (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
 在
在 催化下能将烟气中的
催化下能将烟气中的 、
、 分别氧化为
分别氧化为 和
和 ,
, 也可在其他条件下被还原为
也可在其他条件下被还原为 。
。(1)基态铁原子有
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为 的空间构型为
的空间构型为 为
为(2)碘的四氯化碳溶液为紫红色,加入浓碘化钾水溶液,振荡后溶液紫色变浅,请用离子方程式说明原因
(3)硫单质的常见形式为
 ,其环状结构如图所示,
,其环状结构如图所示, 中含有
中含有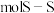 键。
键。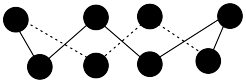
 的熔点为1090℃,远高于
的熔点为1090℃,远高于 的192℃,由此可以判断铝氟之间的化学键为
的192℃,由此可以判断铝氟之间的化学键为 结构属立方晶系,晶胞如图所示,
结构属立方晶系,晶胞如图所示, 的配位数为。若晶胞参数为
的配位数为。若晶胞参数为 ,晶体密度
,晶体密度
 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
名校
解题方法
6 .  是一种农业杀虫剂,下列相关说法错误的是
是一种农业杀虫剂,下列相关说法错误的是
 是一种农业杀虫剂,下列相关说法错误的是
是一种农业杀虫剂,下列相关说法错误的是A.该化合物中 的中心原子的杂化轨道类型为 的中心原子的杂化轨道类型为 |
| B.该化合物中存在的化学键有离子键,共价键,配位键和氢键 |
C. 极易溶于 极易溶于 形成氨水,氨水中最多可形成4种氢键 形成氨水,氨水中最多可形成4种氢键 |
D.根据VSEPR模型预测的 的空间结构是正四面体形 的空间结构是正四面体形 |
您最近一年使用:0次
解题方法
7 . 胍盐是病毒核酸保存液的重要成分之一,胍在碱性条件下不稳定,易水解,化学方程式为
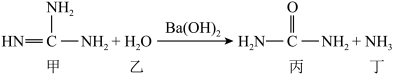
| A.乙、丁分子的VSEPR模型都是四面体形 |
B.甲和丙分子中C原子均采取 杂化 杂化 |
| C.键角:乙大于丁 |
| D.第一电离能:N>O>C |
您最近一年使用:0次
名校
解题方法
8 . I.回答下列问题:
(1)下列原子或离子的核外电子排布正确的是___________ ,违反能量最低原理的是___________ ,违反洪特规则的是___________ ,违反泡利不相容原理的是___________ 。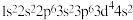 ⑤K:
⑤K: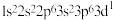 ⑥Mg:
⑥Mg:
(2)《中华本草》等中医典籍中,记载了炉甘石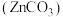 入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是___________ ,其阴离子的空间结构为___________ ,Zn位于元素周期表的___________ 区。
(3)基态锰原子有___________ 种空间运动状态的电子,锰有多种化合价,在+2、+3、+4、+5和+6中,最稳定的化合价是___________ 。
(4) 已知无水 固态时具有链状结构
固态时具有链状结构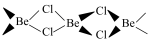 ,在二聚体分子(
,在二聚体分子(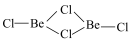 ),其中铍原子的杂化类型为
),其中铍原子的杂化类型为___________ 。
(1)下列原子或离子的核外电子排布正确的是
① :
: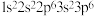 ②
② :
: ③P:
③P: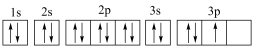
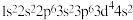 ⑤K:
⑤K: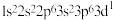 ⑥Mg:
⑥Mg:
⑦C: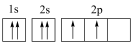
(2)《中华本草》等中医典籍中,记载了炉甘石
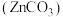 入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是(3)基态锰原子有
(4) 已知无水
 固态时具有链状结构
固态时具有链状结构 ,在二聚体分子(
,在二聚体分子( ),其中铍原子的杂化类型为
),其中铍原子的杂化类型为
您最近一年使用:0次
名校
解题方法
9 . 我国学者用氮气为氮源高效合成了活性氮物质 用于多种高附加值含氮化合物的合成。
用于多种高附加值含氮化合物的合成。 可与乙醇、有机卤代物等反应,其制备及转化为物质甲的过程如下:
可与乙醇、有机卤代物等反应,其制备及转化为物质甲的过程如下: 是一种重要的化工原料,与水接触会发生反应产生酸雾。
是一种重要的化工原料,与水接触会发生反应产生酸雾。
下列说法错误的是
 用于多种高附加值含氮化合物的合成。
用于多种高附加值含氮化合物的合成。 可与乙醇、有机卤代物等反应,其制备及转化为物质甲的过程如下:
可与乙醇、有机卤代物等反应,其制备及转化为物质甲的过程如下:
 是一种重要的化工原料,与水接触会发生反应产生酸雾。
是一种重要的化工原料,与水接触会发生反应产生酸雾。下列说法错误的是
| A.反应Ⅰ实现了氮的固定 | B. 的电子式为 的电子式为 |
| C.反应Ⅱ中的溶剂可为水 | D.物质甲中碳原子的成键方式不同 |
您最近一年使用:0次
名校
解题方法
10 .  在气态或非极性溶剂中均可通过氯桥键二聚成
在气态或非极性溶剂中均可通过氯桥键二聚成 ,熔融
,熔融 和
和 可形成
可形成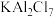 。下列说法正确的是
。下列说法正确的是
 在气态或非极性溶剂中均可通过氯桥键二聚成
在气态或非极性溶剂中均可通过氯桥键二聚成 ,熔融
,熔融 和
和 可形成
可形成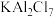 。下列说法正确的是
。下列说法正确的是A. 为极性分子 为极性分子 | B. 中 中 原子的杂化方式为 原子的杂化方式为 |
C.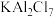 熔点高于 熔点高于 的熔点 的熔点 | D.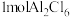 中含有 中含有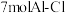 单键 单键 |
您最近一年使用:0次
2024-04-12更新
|
546次组卷
|
3卷引用:四川省成都市石室中学2023-2024学年高二下学期4月月考化学试卷



