1 . Cu可形成多种配合物,某同学在探究配合物的形成时做了以下实验,根据下列信息回答问题:
(1)将无水硫酸铜溶解于水中,溶液呈蓝色,向其中加入浓氨水,产生蓝色沉淀的离子反应方程式___________ ,继续加入浓氨水,沉淀消失,沉淀溶解的离子反应方程式___________ 。
(2)根据以上实验过程,判断 和
和 与
与 的配位能力:
的配位能力:
___________ (填“>”“=”或“<”) 。
。
(3)再向深蓝色透明溶液加入乙醇,析出深蓝色的晶体。深蓝色晶体的化学式为___________ 。
(4)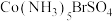 可形成两种钴的配合物。已知
可形成两种钴的配合物。已知 的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加
的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加 溶液时,产生白色沉淀,在第二种配合物的溶液中加
溶液时,产生白色沉淀,在第二种配合物的溶液中加 溶液时,则无明显现象。
溶液时,则无明显现象。
则第一种配合物的结构式可表示为___________ 。(提示: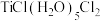 这种配合物的结构可表示为
这种配合物的结构可表示为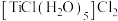 );若
);若 均为配体,则在第二种配合物的溶液中滴加
均为配体,则在第二种配合物的溶液中滴加 溶液,产生的现象是
溶液,产生的现象是___________ 。
(1)将无水硫酸铜溶解于水中,溶液呈蓝色,向其中加入浓氨水,产生蓝色沉淀的离子反应方程式
(2)根据以上实验过程,判断
 和
和 与
与 的配位能力:
的配位能力:
 。
。(3)再向深蓝色透明溶液加入乙醇,析出深蓝色的晶体。深蓝色晶体的化学式为
(4)
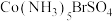 可形成两种钴的配合物。已知
可形成两种钴的配合物。已知 的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加
的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加 溶液时,产生白色沉淀,在第二种配合物的溶液中加
溶液时,产生白色沉淀,在第二种配合物的溶液中加 溶液时,则无明显现象。
溶液时,则无明显现象。则第一种配合物的结构式可表示为
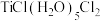 这种配合物的结构可表示为
这种配合物的结构可表示为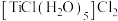 );若
);若 均为配体,则在第二种配合物的溶液中滴加
均为配体,则在第二种配合物的溶液中滴加 溶液,产生的现象是
溶液,产生的现象是
您最近一年使用:0次
名校
2 . 已知 呈粉红色,
呈粉红色, 呈蓝色,
呈蓝色,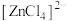 为无色。现将
为无色。现将 溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:
溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: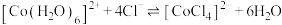 ,用该溶液做实验,溶液的颜色变化如下:
,用该溶液做实验,溶液的颜色变化如下:
 呈粉红色,
呈粉红色, 呈蓝色,
呈蓝色,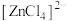 为无色。现将
为无色。现将 溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:
溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: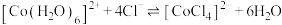 ,用该溶液做实验,溶液的颜色变化如下:
,用该溶液做实验,溶液的颜色变化如下:
A.等物质的量的 和 和 中 中 键数之比为 键数之比为 |
B.由实验1可推知 |
C.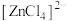 和 和 的配位数之比为 的配位数之比为 |
D.由实验③可知配离子的稳定性: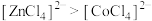 |
您最近一年使用:0次
名校
解题方法
3 . 碳铂(结构简式如图)是一种广谱抗癌药物。下列关于碳铂的说法错误的是


| A.中心原子的配位数为4 | B. 和 和 杂化的碳原子数之比为 杂化的碳原子数之比为 |
C.分子中σ键与π键的数目之比为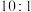 | D.分子中含有极性键、非极性键和配位键 |
您最近一年使用:0次
2024-02-10更新
|
212次组卷
|
7卷引用:山东省枣庄市2021-2022学年高三高考适应性练习(一)化学试题
山东省枣庄市2021-2022学年高三高考适应性练习(一)化学试题(已下线)微专题50 分子的立体结构的判断-备战2023年高考化学一轮复习考点微专题湖南省张家界市慈利县第一中学2022-2023学年高三上学期第四次月考化学试卷山东省淄博实验中学2022-2023学年高二下学期3月月考化学试题新疆乌鲁木齐市第六十八中学2023-2024学年高三上学期1月月考化学试题陕西省咸阳市实验中学2023-2024学年高二上学期段性检测(一)化学试题(已下线)3.4.1 配合物与超分子(基础)
名校
4 . 冠醚是一类皇冠状的分子,可有不同大小的空穴适配不同大小的碱金属离子。18-冠-6可以通过图示方法制备。下列说法错误的是

| A.18-冠-6分子中C、O都采用sp3杂化 |
| B.18-冠-6和碱金属离子通过共价键形成超分子 |
| C.冠醚的空穴结构对离子有选择作用,在有机反应中可作催化剂 |
| D.制取方法中(1)为取代反应,另一种产物为HCl |
您最近一年使用:0次
2023-09-08更新
|
383次组卷
|
2卷引用:湖北省恩高芳华中学2022-2023学年高二上学期期末考试化学试卷
名校
5 . 材料科学发展日新月异。

(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,基态镍原子 层上的未成对电子数为
层上的未成对电子数为_____ 。
(2)硫酸镍溶于氨水形成 蓝色溶液。
蓝色溶液。
① 中阴离子的立体构型是
中阴离子的立体构型是_____ 。
②在 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为_____ ,提供孤电子对的成键原子是_____ 。
(3)将 应用于超导体、材料科学等领域的探索正在不断地深入。
应用于超导体、材料科学等领域的探索正在不断地深入。 的结构如图1,
的结构如图1,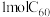 分子中
分子中 键的数目为
键的数目为_____ 。 能在二硫化碳中溶解而不溶于水的原因是
能在二硫化碳中溶解而不溶于水的原因是_____ 。
(4)某金属 与
与 可制备一种超导材料,晶胞如图2所示,
可制备一种超导材料,晶胞如图2所示, 原子位于晶胞的棱上与内部。该材料的化学式为
原子位于晶胞的棱上与内部。该材料的化学式为_____ 。
(5)石墨的晶体结构如图3(甲)所示,碳原子的杂化方式为_____ ,图3(乙)虚线勾勒出的是其晶胞,则石墨晶胞含碳原子个数为_____ 个。
(6)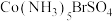 可形成两种配合物,已知
可形成两种配合物,已知 的配位数是6,为确定
的配位数是6,为确定 的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加
的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加 溶液时,产生白色沉淀;在第二种配合物溶液中加入
溶液时,产生白色沉淀;在第二种配合物溶液中加入 溶液时,无明显现象。第二种配合物的化学式为
溶液时,无明显现象。第二种配合物的化学式为_____ ,该配合物的配体是_____ 。

(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,基态镍原子
 层上的未成对电子数为
层上的未成对电子数为(2)硫酸镍溶于氨水形成
 蓝色溶液。
蓝色溶液。①
 中阴离子的立体构型是
中阴离子的立体构型是②在
 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为(3)将
 应用于超导体、材料科学等领域的探索正在不断地深入。
应用于超导体、材料科学等领域的探索正在不断地深入。 的结构如图1,
的结构如图1,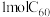 分子中
分子中 键的数目为
键的数目为 能在二硫化碳中溶解而不溶于水的原因是
能在二硫化碳中溶解而不溶于水的原因是(4)某金属
 与
与 可制备一种超导材料,晶胞如图2所示,
可制备一种超导材料,晶胞如图2所示, 原子位于晶胞的棱上与内部。该材料的化学式为
原子位于晶胞的棱上与内部。该材料的化学式为(5)石墨的晶体结构如图3(甲)所示,碳原子的杂化方式为
(6)
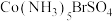 可形成两种配合物,已知
可形成两种配合物,已知 的配位数是6,为确定
的配位数是6,为确定 的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加
的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加 溶液时,产生白色沉淀;在第二种配合物溶液中加入
溶液时,产生白色沉淀;在第二种配合物溶液中加入 溶液时,无明显现象。第二种配合物的化学式为
溶液时,无明显现象。第二种配合物的化学式为
您最近一年使用:0次
名校
解题方法
6 . 利用氧化法制备配合物: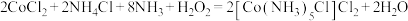 ,下列说法正确的是
,下列说法正确的是
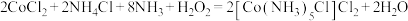 ,下列说法正确的是
,下列说法正确的是| A.该配位化合物的配位数是5 |
B. 中存在配位键、共价键和离子键 中存在配位键、共价键和离子键 |
C. 发生了氧化反应 发生了氧化反应 |
| D.提供孤电子对的成键原子是N和Cl |
您最近一年使用:0次
2023-11-23更新
|
161次组卷
|
2卷引用:北京市首都师范大学附属中学2022-2023学年高三上学期开学测试化学试题
7 . 氮族元素在化学领域具有重要的地位。请回答下列问题:
(1)基态氮原子的核外电子排布式为___________ 。
(2)在PH3分子中,中心原子的杂化方式为___________ ,PH3的空间结构为___________ 。
(3)向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液,向该溶液中加入一定量的乙醇,析出[Cu(NH3)4]SO4·H2O固体。
①[Cu(NH3)4]SO4·H2O晶体中不存在的作用力是___________ (填字母)。
A.离子键 B.共价键 C.氢键 D.金属键 E.配位键
②将[Cu(NH3)4]SO4配合物溶于水,电离方程式为___________ 。
(1)基态氮原子的核外电子排布式为
(2)在PH3分子中,中心原子的杂化方式为
(3)向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液,向该溶液中加入一定量的乙醇,析出[Cu(NH3)4]SO4·H2O固体。
①[Cu(NH3)4]SO4·H2O晶体中不存在的作用力是
A.离子键 B.共价键 C.氢键 D.金属键 E.配位键
②将[Cu(NH3)4]SO4配合物溶于水,电离方程式为
您最近一年使用:0次
8 . 下列说法正确的是
| A.在铝—海水—空气电池中,可直接利用海水,由此可知海水是电解质 |
| B.向硫酸铜溶液中逐滴加氨水至生成的难溶物溶解后,再加入乙醇,析出深蓝色的[Cu(NH3)4]SO4·H2O |
| C.向1mol[TiCl(H2O)5]Cl2·H2O的配合物中加入足量的AgNO3溶液,生成3mol的AgCl沉淀 |
| D.已知稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1,则稀醋酸与稀氢氧化钠溶液反应生成1mol水时放出57.3kJ的热量 |
您最近一年使用:0次
名校
9 . 向盛有少量CuCl2溶液的试管中滴入少量NaOH溶液,再滴入适量浓氨水,下列叙述不正确的是
| A.Cu(OH)2溶于浓氨水的离子方程式是Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH- |
| B.开始生成蓝色沉淀,加入过量氢氧化钠时,形成深蓝色溶液 |
| C.开始生成Cu(OH)2,之后生成更稳定的配合物 |
| D.开始生成蓝色沉淀,加入氨水后,沉淀溶解形成深蓝色溶液 |
您最近一年使用:0次
名校
解题方法
10 . 下列实验方案设计、预期现象和结论都正确的是
| 实验方案设计 | 现象和结论 | |
| A | 对 溶液进行加热 溶液进行加热 | 溶液由蓝色变为黄绿色,说明平衡: (蓝色) (蓝色)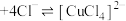 (黄绿色) (黄绿色) |
| B | 向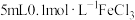 溶液中滴加 溶液中滴加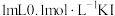 溶液,再滴加几滴 溶液,再滴加几滴 溶液,观察溶液颜色变化 溶液,观察溶液颜色变化 | 溶液变红,说明 与 与 的反应为可逆反应 的反应为可逆反应 |
| C | 将 通入 通入 溶液后,将混合气体依次通入酸性 溶液后,将混合气体依次通入酸性 溶液、品红溶液和澄清石灰水 溶液、品红溶液和澄清石灰水 | 酸性 溶液褪色、品红溶液不褪色、澄清石灰水变浑浊,说明非金属性: 溶液褪色、品红溶液不褪色、澄清石灰水变浑浊,说明非金属性: |
| D | 在相同条件下,向试管①中加入 和 和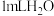 ,向试管②中加入 ,向试管②中加入 和 和 溶液,观察并比较实验现象 溶液,观察并比较实验现象 | 试管②产生气泡的速率更快,说明 是 是 分解的催化剂 分解的催化剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



