名校
1 . 下列反应的离子方程式正确的是
| A.硝酸钡溶液中通入SO2:Ba2++SO2+H2O=BaSO3↓+2H+ |
B.Ca(HCO3)2溶液中加少量NaOH溶液:Ca2++ +OH-=CaCO3↓+H2O +OH-=CaCO3↓+H2O |
C.饱和Na2CO3溶液中通入过量CO2: +CO2+H2O=2 +CO2+H2O=2 |
D.硫酸铜溶液中加过量浓氨水:Cu2++2NH3⋅H2O=Cu(OH)2↓+2 |
您最近一年使用:0次
2 . 氢叠氮酸( )属于叠氮化物,是一种弱酸,其酸性类似于醋酸,能微弱电离出
)属于叠氮化物,是一种弱酸,其酸性类似于醋酸,能微弱电离出 和
和 。分子结构示意图如图所示。回答下列问题:
。分子结构示意图如图所示。回答下列问题:
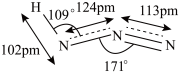
(1)下列有关说法正确的是_____(填字母符号)。
(2)叠氮酸根可作为一种配体,在 中钴显
中钴显_____ 价,基态钴原子的价电子排布式为_____ 。 空间形状为
空间形状为_______ 。
(3) 与
与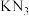 结构类似,前者晶格能比后者
结构类似,前者晶格能比后者_____ (填“大”或“小”), 中氮原子的第一电离能比氧原子
中氮原子的第一电离能比氧原子______ (填“大”或“小”)。
(4)与 互为等电子体的分子有
互为等电子体的分子有______ (写出两种即可)。
(5)人造立方氮化硼是超硬材料,其晶胞如图所示。

①晶体中硼原子的配位数为____ 。
②设该晶体的摩尔质量为 ,晶体的密度为
,晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶体中的距离最近的硼原子之间的距离为
,则晶体中的距离最近的硼原子之间的距离为______ cm。
 )属于叠氮化物,是一种弱酸,其酸性类似于醋酸,能微弱电离出
)属于叠氮化物,是一种弱酸,其酸性类似于醋酸,能微弱电离出 和
和 。分子结构示意图如图所示。回答下列问题:
。分子结构示意图如图所示。回答下列问题:
(1)下列有关说法正确的是_____(填字母符号)。
A. 中含有5个 中含有5个 键 键 | B. 中三个氮原子采用的都是 中三个氮原子采用的都是 杂化 杂化 |
C. 、 、 都是极性分子 都是极性分子 | D. 、 、 、 、 分子间都可以形成氢键 分子间都可以形成氢键 |
(2)叠氮酸根可作为一种配体,在
 中钴显
中钴显 空间形状为
空间形状为(3)
 与
与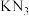 结构类似,前者晶格能比后者
结构类似,前者晶格能比后者 中氮原子的第一电离能比氧原子
中氮原子的第一电离能比氧原子(4)与
 互为等电子体的分子有
互为等电子体的分子有(5)人造立方氮化硼是超硬材料,其晶胞如图所示。

①晶体中硼原子的配位数为
②设该晶体的摩尔质量为
 ,晶体的密度为
,晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶体中的距离最近的硼原子之间的距离为
,则晶体中的距离最近的硼原子之间的距离为
您最近一年使用:0次
名校
解题方法
3 . X、Y、R、Q为前四周期元素且原子序数依次增大,X的单质与氢气可以化合生成气体G,其水溶液呈碱性;Y的一种单质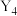 中分子为正四面体结构;R基态原子的核外有6个单电子;Q的基态原子M层电子全充满,N层只有一个电子。请回答下列问题:
中分子为正四面体结构;R基态原子的核外有6个单电子;Q的基态原子M层电子全充满,N层只有一个电子。请回答下列问题:
(1)Q元素在周期表中的位置是______ 。
(2) 价层的轨道表示式是
价层的轨道表示式是______ 。
(3)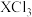 与
与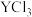 的键角大小为:
的键角大小为: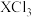
______  (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。
(4)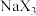 可用于安全气囊的产气药剂,
可用于安全气囊的产气药剂, 离子中中心原子的杂化方式为
离子中中心原子的杂化方式为______ 杂化。
(5)如下图所示Y可形成多种含氧酸根:
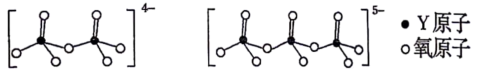
这类酸根离子的化学式可用通式表示为______ (用n代表Y原子数)。
(6)已知R元素形成的配合物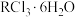 中心原子
中心原子 配位数为6,向含
配位数为6,向含 的溶液中滴加
的溶液中滴加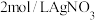 溶液,反应完全后消耗
溶液,反应完全后消耗 溶液
溶液 ,则该配离子的化学式为
,则该配离子的化学式为______ 。
(7)已知 晶体结构单元如下图所示,离H最近且等距的H的个数为
晶体结构单元如下图所示,离H最近且等距的H的个数为______ 。

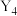 中分子为正四面体结构;R基态原子的核外有6个单电子;Q的基态原子M层电子全充满,N层只有一个电子。请回答下列问题:
中分子为正四面体结构;R基态原子的核外有6个单电子;Q的基态原子M层电子全充满,N层只有一个电子。请回答下列问题:(1)Q元素在周期表中的位置是
(2)
 价层的轨道表示式是
价层的轨道表示式是(3)
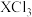 与
与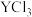 的键角大小为:
的键角大小为: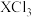
 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。(4)
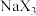 可用于安全气囊的产气药剂,
可用于安全气囊的产气药剂, 离子中中心原子的杂化方式为
离子中中心原子的杂化方式为(5)如下图所示Y可形成多种含氧酸根:

这类酸根离子的化学式可用通式表示为
(6)已知R元素形成的配合物
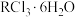 中心原子
中心原子 配位数为6,向含
配位数为6,向含 的溶液中滴加
的溶液中滴加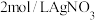 溶液,反应完全后消耗
溶液,反应完全后消耗 溶液
溶液 ,则该配离子的化学式为
,则该配离子的化学式为(7)已知
 晶体结构单元如下图所示,离H最近且等距的H的个数为
晶体结构单元如下图所示,离H最近且等距的H的个数为
您最近一年使用:0次
名校
解题方法
4 . 下列方程式与所给事实不相符的是
A.硫酸铜溶液中加少量氨水:Cu2++2NH3·H2O=Cu(OH)2↓+2 |
B.氢气燃烧热为285.8kJ/mol:H2(g)+ O2(g)=H2O(l) ΔH=−285.8kJ/mol O2(g)=H2O(l) ΔH=−285.8kJ/mol |
| C.用KSCN溶液检验Fe3+:Fe3++3SCN−=Fe(SCN)3↓ |
| D.加热CuCl2溶液,溶液变成黄绿色:[Cu(H2O)4]2++4Cl−⇌[CuCl4]2−+4H2O ΔH>0 |
您最近一年使用:0次
名校
解题方法
5 . 向盛有少量蒸馏水的试管里滴加2滴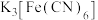 溶液,然后再滴加2滴硫氰化钾溶液。
溶液,然后再滴加2滴硫氰化钾溶液。
下列说法正确的是
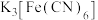 溶液,然后再滴加2滴硫氰化钾溶液。
溶液,然后再滴加2滴硫氰化钾溶液。下列说法正确的是
| A.溶液颜色由黄色变为红色 |
B. 中由 中由 提供孤电子对, 提供孤电子对, 提供空轨道 提供空轨道 |
C. 和 和 与 与 的配位能力: 的配位能力: |
D. 中含 中含 键的物质的量为 键的物质的量为 |
您最近一年使用:0次
2024-02-16更新
|
242次组卷
|
2卷引用:重庆市南开中学2023-2024学年高二上学期期末考试化学试题
6 . [Co(NH3)6]Cl2晶体的晶胞如下图所示(已知该立方晶胞的边长为a pm,阿伏加德罗常数为NA,[Co(NH3)6]Cl2的摩尔质量为M g/mol),以下说法正确的是
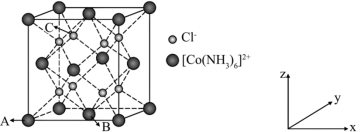

| A.[Co(NH3)6]Cl2中,中心离子的配位数为8 |
| B.离[Co(NH3)6]2+最近的Cl- 有4个 |
C.若规定A点原子坐标为(0,0,0),则C点原子坐标为(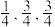 ) ) |
D.[Co(NH3)6]Cl2晶体的密度为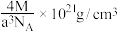 |
您最近一年使用:0次
名校
解题方法
7 . 向下列溶液中加入指定离子,一定有沉淀生成的是
A.向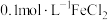 溶液中加入 溶液中加入 、 、 、 、 、 、 |
B.向 溶液中加入 溶液中加入 、 、 、 、 、 、 |
C.向 氨水中加入 氨水中加入 、 、 、 、 、 、 |
D.向新制氯水中加入 、 、 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
8 . 硫代硫酸盐是一类具有应用前景的浸金试剂。 的晶胞形状为长方体,边长分别为anm、bnm、cnm,结构如图所示,其中
的晶胞形状为长方体,边长分别为anm、bnm、cnm,结构如图所示,其中 可看作
可看作 中一个氧原子被硫原子所替代。下列说法
中一个氧原子被硫原子所替代。下列说法错误 的是
 的晶胞形状为长方体,边长分别为anm、bnm、cnm,结构如图所示,其中
的晶胞形状为长方体,边长分别为anm、bnm、cnm,结构如图所示,其中 可看作
可看作 中一个氧原子被硫原子所替代。下列说法
中一个氧原子被硫原子所替代。下列说法
| A.晶体中存在的相互作用有共价键、配位键和离子键 |
| B.该晶体属于离子晶体,阴、阳离子的配位数不相等 |
C.阴离子的VSEPR模型与 、 、 相同 相同 |
D.晶体的摩尔质量是 ,该晶体的密度为 ,该晶体的密度为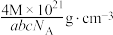 |
您最近一年使用:0次
2024-01-15更新
|
265次组卷
|
2卷引用:重庆市第八中学校2023-2024学年高三上学期一诊适应性考试化学试卷
名校
解题方法
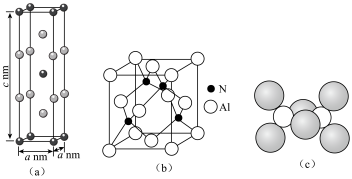
9 . Al元素可以形成多种类型的物质。例如AlCr2晶体具有体心四方结构,如图(a)所示;AlN晶胞结构如图(b)所示;气态AlCl3通常以二聚体Al2Cl6形式存在,其空间结构如图(c)所示。下列说法正确的是

A.基态铬原子的核外电子排布式为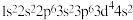 |
B.AlCr2晶体的密度为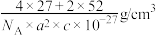 |
| C.AlN中各原子均未达到8电子稳定结构 |
D.二聚体Al2Cl6中Al的轨道杂化类型为 |
您最近一年使用:0次
名校
10 . 二氯化一氯五氨合钴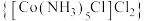 可用作聚氯乙烯的染色剂和稳定剂。已知:
可用作聚氯乙烯的染色剂和稳定剂。已知: 不溶于水和乙醇;
不溶于水和乙醇; 是粉红色不溶于水的固体;
是粉红色不溶于水的固体; 是棕褐色不溶于水的固体。
是棕褐色不溶于水的固体。
Ⅰ.制备
某实验小组利用以下装置和流程制备 。
。
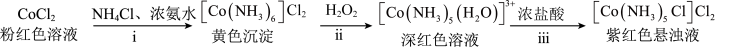
(1)步骤ⅱ,滴入 5%
5% ,发生反应的离子方程式为
,发生反应的离子方程式为___________ 。
(2)步骤ⅲ,待溶液中停止产生气泡后,缓慢加入 浓盐酸,在85℃水浴中加热
浓盐酸,在85℃水浴中加热 ,所得混合物冷却至室温,抽滤、洗涤、烘干得到产品。洗涤过程需要用到冰水和无水乙醇,使用无水乙醇的原因
,所得混合物冷却至室温,抽滤、洗涤、烘干得到产品。洗涤过程需要用到冰水和无水乙醇,使用无水乙醇的原因___________ 。
Ⅱ.产品结构分析
(3) 中存在的化学键有
中存在的化学键有___________ (填标号)。
a.离子键 b.范德华力 c.非极性共价键 d.极性共价键 e.配位键 f.氢键
(4) 中含
中含 键的数目为
键的数目为___________ 。
Ⅲ.实验探究
(5)实验小组在制备过程中发现 溶液中直接加入
溶液中直接加入 ,
, 不被氧化,据此认为加入浓氨水和氯化铵对
不被氧化,据此认为加入浓氨水和氯化铵对 的氧化产生了影响,提出以下猜想并设计实验验证。
的氧化产生了影响,提出以下猜想并设计实验验证。
猜想1:加入氯化铵溶液,增强了 的氧化性。
的氧化性。
猜想2:加入浓氨水形成配合物,增强了 离子的还原性。
离子的还原性。
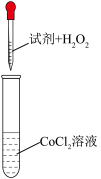
实验结论:猜想1不合理,猜想2合理。
①a是___________ ,b是___________ 。
②步骤ⅰ中氯化铵的作用是___________ 。
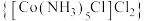 可用作聚氯乙烯的染色剂和稳定剂。已知:
可用作聚氯乙烯的染色剂和稳定剂。已知: 不溶于水和乙醇;
不溶于水和乙醇; 是粉红色不溶于水的固体;
是粉红色不溶于水的固体; 是棕褐色不溶于水的固体。
是棕褐色不溶于水的固体。Ⅰ.制备

某实验小组利用以下装置和流程制备
 。
。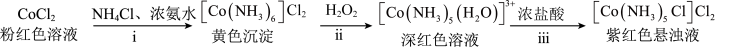
(1)步骤ⅱ,滴入
 5%
5% ,发生反应的离子方程式为
,发生反应的离子方程式为(2)步骤ⅲ,待溶液中停止产生气泡后,缓慢加入
 浓盐酸,在85℃水浴中加热
浓盐酸,在85℃水浴中加热 ,所得混合物冷却至室温,抽滤、洗涤、烘干得到产品。洗涤过程需要用到冰水和无水乙醇,使用无水乙醇的原因
,所得混合物冷却至室温,抽滤、洗涤、烘干得到产品。洗涤过程需要用到冰水和无水乙醇,使用无水乙醇的原因Ⅱ.产品结构分析
(3)
 中存在的化学键有
中存在的化学键有a.离子键 b.范德华力 c.非极性共价键 d.极性共价键 e.配位键 f.氢键
(4)
 中含
中含 键的数目为
键的数目为Ⅲ.实验探究
(5)实验小组在制备过程中发现
 溶液中直接加入
溶液中直接加入 ,
, 不被氧化,据此认为加入浓氨水和氯化铵对
不被氧化,据此认为加入浓氨水和氯化铵对 的氧化产生了影响,提出以下猜想并设计实验验证。
的氧化产生了影响,提出以下猜想并设计实验验证。猜想1:加入氯化铵溶液,增强了
 的氧化性。
的氧化性。猜想2:加入浓氨水形成配合物,增强了
 离子的还原性。
离子的还原性。
| 实验编号 | 试剂 | 现象 |
| 1 |  水 水 | 无明显变化 |
| 2 | a | 无明显变化 |
| 3 | b | 溶液变为深红色,且出现棕褐色沉淀 |
①a是
②步骤ⅰ中氯化铵的作用是
您最近一年使用:0次
2023-12-12更新
|
435次组卷
|
3卷引用:重庆市万州第二高级中学2023-2024学年高二下学期3月月考化学试题
重庆市万州第二高级中学2023-2024学年高二下学期3月月考化学试题海南省海南中学2023-2024学年高三上学期第三次月考化学试题(已下线)题型17 化学实验综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)



