名校
解题方法
1 . 尿素CO(NH2)2是一种高效化肥和化工原料。反应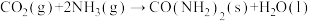 可用于尿素的制备。下列有关说法正确的是
可用于尿素的制备。下列有关说法正确的是
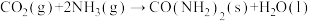 可用于尿素的制备。下列有关说法正确的是
可用于尿素的制备。下列有关说法正确的是| A.CO2分子为极性分子 | B.NH3分子的空间结构为平面三角形 |
C.H2O分子的空间填充模型 | D.尿素分子σ键和π键的数目之比为7:1 |
您最近一年使用:0次
名校
解题方法
2 . 某油脂厂废弃的油脂加氢反应的镍催化剂主要含金属Ni、Al、Fe 及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O);

回答下列问题:
(1)“碱浸”中NaOH除了能够将铝元素去除外,另一个作用是___________ 。
(2)基态Ni2+的价层电子排布图为___________ ,Ni在元素周期表中位于___________ 区。
(3)“转化”过程宜控制较低温度的原因是___________ ;H2O2的结构如图所示,则 H2O2是_________ 分子(填“极性”或“非极性”),转化过程中的双氧水可用O3代替,O3中的中心O原子的杂化方式为___________ ,O3的空间构型是___________ ,O3是___________ 分子(填“极性”或“非极性”)。

(4)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的 NiOOH,写出该反应的离子方程式:___________ 。
(5)Ni 和La 的合金是目前使用广泛的储氢材料。该合金的晶胞结构如下图所示。该晶胞中粒子个数比La:Ni=__________ ,该合金储氢后,如下图,1mol该合金可吸附H2的物质的量为___________ 。


回答下列问题:
(1)“碱浸”中NaOH除了能够将铝元素去除外,另一个作用是
(2)基态Ni2+的价层电子排布图为
(3)“转化”过程宜控制较低温度的原因是

(4)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的 NiOOH,写出该反应的离子方程式:
(5)Ni 和La 的合金是目前使用广泛的储氢材料。该合金的晶胞结构如下图所示。该晶胞中粒子个数比La:Ni=

您最近一年使用:0次
3 . 某种天然沸石的化学式为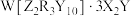 ,X、Y、Z、R、W为原子序数依次增大的主族元素,且占据前四个周期。Y元素在地壳中含量最高,R元素的单质可用于制造太阳能电池板,基态W原子的核外电子恰好填满10个原子轨道。下列说法错误的是
,X、Y、Z、R、W为原子序数依次增大的主族元素,且占据前四个周期。Y元素在地壳中含量最高,R元素的单质可用于制造太阳能电池板,基态W原子的核外电子恰好填满10个原子轨道。下列说法错误的是
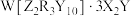 ,X、Y、Z、R、W为原子序数依次增大的主族元素,且占据前四个周期。Y元素在地壳中含量最高,R元素的单质可用于制造太阳能电池板,基态W原子的核外电子恰好填满10个原子轨道。下列说法错误的是
,X、Y、Z、R、W为原子序数依次增大的主族元素,且占据前四个周期。Y元素在地壳中含量最高,R元素的单质可用于制造太阳能电池板,基态W原子的核外电子恰好填满10个原子轨道。下列说法错误的是| A.同周期第一电离能比Z小的元素有2种 | B.由Y构成的单质可以为极性分子 |
| C.简单氢化物的稳定性:Y>R | D.氯化物熔点:W>Z |
您最近一年使用:0次
名校
解题方法
4 . 碳氮硫共脱除工艺可以协同除去工业废水中的S2-、NO 和CH3COO-,过程如图所示。已知:成键原子共平面,每个原子能提供一个相互平行的p轨道且p轨道电子数小于参加成键的p轨道数的两倍时可形成离域π键。下列说法错误的是
和CH3COO-,过程如图所示。已知:成键原子共平面,每个原子能提供一个相互平行的p轨道且p轨道电子数小于参加成键的p轨道数的两倍时可形成离域π键。下列说法错误的是
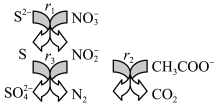
 和CH3COO-,过程如图所示。已知:成键原子共平面,每个原子能提供一个相互平行的p轨道且p轨道电子数小于参加成键的p轨道数的两倍时可形成离域π键。下列说法错误的是
和CH3COO-,过程如图所示。已知:成键原子共平面,每个原子能提供一个相互平行的p轨道且p轨道电子数小于参加成键的p轨道数的两倍时可形成离域π键。下列说法错误的是
| A.N2和CO2都是非极性分子 |
B.NO 和NO 和NO 的空间构型相同 的空间构型相同 |
C.NO 中存在离域π键 中存在离域π键 |
| D.冰醋酸中CH3COOH分子间存在范德华力和氢键 |
您最近一年使用:0次
2023-01-15更新
|
580次组卷
|
4卷引用:山东省潍坊市2022-2023学年高三上学期期末考试化学试题
解题方法
5 . 下列说法正确的是
A. 分子的极性比 分子的极性比 的大 的大 |
B.无机含氧酸的酸性: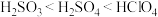 |
C. 的分子构型为 的分子构型为 形,则二甲醚的分子骨架 形,则二甲醚的分子骨架 构型为 构型为 形 形 |
D.键角: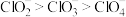 |
您最近一年使用:0次
名校
解题方法
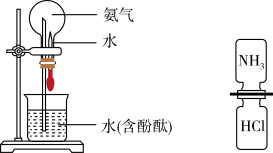
6 . 下列关于氨气的说法不正确 的是

A.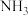 分子呈三角锥形,属于极性分子 分子呈三角锥形,属于极性分子 |
B.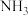 易液化、易溶于水均与氢键的形成有关 易液化、易溶于水均与氢键的形成有关 |
C.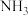 与HCl反应的过程包含配位键的形成, 与HCl反应的过程包含配位键的形成,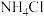 属于共价化合物 属于共价化合物 |
D.烧瓶中溶液红色不变时,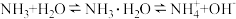 达平衡 达平衡 |
您最近一年使用:0次
解题方法
7 .  是电池的一种电解质,该电解质阴离子由同周期元素原子W、X、Y、Z构成(如图),Y的最外层电子数等于X的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是
是电池的一种电解质,该电解质阴离子由同周期元素原子W、X、Y、Z构成(如图),Y的最外层电子数等于X的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是

 是电池的一种电解质,该电解质阴离子由同周期元素原子W、X、Y、Z构成(如图),Y的最外层电子数等于X的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是
是电池的一种电解质,该电解质阴离子由同周期元素原子W、X、Y、Z构成(如图),Y的最外层电子数等于X的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是
A.原子半径: |
| B.W、Z形成的化合物分子为含有极性键的非极性分子 |
| C.四种元素形成的简单氢化物中X的最稳定 |
| D.四种元素的单质中,有分子晶体、共价晶体和金属晶体三种情况 |
您最近一年使用:0次
名校
解题方法
8 . 膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,电石气的杂质中常含有磷化氢。以下关于PH3的叙述正确的是
| A.PH3分子中无未成键的孤对电子 | B.PH3是极性分子 |
| C.它的分子构型是三角锥形 | D.磷原子采用sp2杂化方式 |
您最近一年使用:0次
2021-04-12更新
|
157次组卷
|
2卷引用:海南省海南鑫源高级中学2020-2021学年高二下学期第一次月考化学试题
解题方法
9 . 已知A、B、C、D、E、F是前四周期的核电荷数依次增大的主族元素,A的最外层电子数是其电子层数的2倍,C、D同一主族,D元素原子M层有两对成对电子,E在前四周期主族元素中原子半径最大,F的基态原子中有4个未成对电子。
(1)基态F2+的电子排布式是______ 。
(2)B、C、D的第一电离能由大到小的顺序是______ (填字母对应的元素符号)。
(3) 离子的空间构型为
离子的空间构型为_______ 。
(4)某F的配合物化学式是[F(H2O)5Cl]Cl2·H2O,与中心F3+的形成配位键的原子或离子是_____ 。
(5)F(AC)5常温下是一种浅黄色液体,熔点-20℃,不溶于水、易溶于苯。每个AC分子与F原子间均有1个配位键。
①1molF(AC)5中所含σ键的数目为______ 。
②1molF(AC)5分子的结构可能为下图中的______ (填“甲”或“乙"),理由是______ 。

(6)由A、B、E、F元素形成的一种蓝色晶体,其晶体结构示意图如图两所示(图中E的离子未画出)。该蓝色晶体的化学式为____ 。
(1)基态F2+的电子排布式是
(2)B、C、D的第一电离能由大到小的顺序是
(3)
 离子的空间构型为
离子的空间构型为(4)某F的配合物化学式是[F(H2O)5Cl]Cl2·H2O,与中心F3+的形成配位键的原子或离子是
(5)F(AC)5常温下是一种浅黄色液体,熔点-20℃,不溶于水、易溶于苯。每个AC分子与F原子间均有1个配位键。
①1molF(AC)5中所含σ键的数目为
②1molF(AC)5分子的结构可能为下图中的

(6)由A、B、E、F元素形成的一种蓝色晶体,其晶体结构示意图如图两所示(图中E的离子未画出)。该蓝色晶体的化学式为
您最近一年使用:0次
解题方法
10 . 焦性没食子酸在气体分析中可用作氧的吸收剂,其结构简式为 ,下列关于焦性没食子酸的说法错误的( )
,下列关于焦性没食子酸的说法错误的( )
 ,下列关于焦性没食子酸的说法错误的( )
,下列关于焦性没食子酸的说法错误的( )| A.所有原子可能共平面 |
| B.含有三种极性共价键 |
| C.熔点高于苯的原因为其键能总和更大 |
| D.相同条件下,在乙醇中的溶解度大于在二硫化碳中的溶解度 |
您最近一年使用:0次
2020-10-04更新
|
242次组卷
|
3卷引用:河北省石家庄市2021届高三上学期质量检测(一)化学试题



