名校
解题方法
1 . 已知PH3与NH3结构相似,回答下列问题:
①PH3的电子式________ ,结构式________ 。
②几何构型为________ 。
③中心原子采取________ 杂化。
④PH3分子中的化学键________ (填“有”或“无”)极性,其分子为________ (填“极性”或”非极性”)分子。
⑤PH3与NH3的热稳定性:________ 更强。
①PH3的电子式
②几何构型为
③中心原子采取
④PH3分子中的化学键
⑤PH3与NH3的热稳定性:
您最近一年使用:0次
2020-03-06更新
|
316次组卷
|
2卷引用:黑龙江省桦南县第二中学2019-2020学年高二下学期期中考试化学试题
11-12高二上·四川雅安·期中
名校
2 . 下列各组分子中,都属于含极性键的非极性分子的是
| A.CO2 H2S | B.CH4 BF3 | C.C60 C2H4 | D.NH3 HCl |
您最近一年使用:0次
解题方法
3 . 我国科学家借助自主研制的新型钨钴合金催化剂攻克了单壁碳纳米管结构的可控制备难题。

(1)基态钴原子的核外未成对电子数为__________ 。单壁碳纳米管可看作石墨烯沿一定方向卷曲而成的空心圆柱体,其结构如图所示,其中碳原子的杂化方式为_______ 。
(2)纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化,已知甲醛各原子均满足稳定结构,甲醛分子属______ 分子(选填“极性”“非极性”),其分子的空间构型为_____ 。新制备的Cu(OH)2可将乙醛(CH3CHO)氧化为乙酸,而自身还原成Cu2O,乙酸的沸点明显高于乙醛,其主要原因是______ 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有______ 个铜原子。金属Cu为________ 堆积,配位数为_______ 。
(3)橙红色晶体羰基钴的熔点为52℃,分子式为Co2(CO)8,是一种重要的配合物,可溶于多数有机溶剂。该晶体属于______ 晶体,三种元素电负性由大到小的顺序为(填元素符号)_____ 。配体CO的任意一种等电子体的电子式:_____ 。配体CO中与Co形成配位键的原子是C而不是O的原因是________ 。

(1)基态钴原子的核外未成对电子数为
(2)纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化,已知甲醛各原子均满足稳定结构,甲醛分子属
(3)橙红色晶体羰基钴的熔点为52℃,分子式为Co2(CO)8,是一种重要的配合物,可溶于多数有机溶剂。该晶体属于
您最近一年使用:0次
4 . 下列叙述中正确的是( )
| A.CH3Cl是手性分子 | B.CH4、CCl4都是含有极性键的非极性分子 |
| C.HF、HCl、HBr、HI的稳定性依次增强 | D.CS2、H2O、C2H2都是直线型分子 |
您最近一年使用:0次
5 . 下列说法中正确 的是:( )
| A.SO2、SO3都是极性分子 |
| B.在 [Cu(NH3)4]2+中存在配位键而NH4+中不存在配位键 |
| C.元素电负性越大的原子,吸引电子的能力越强 |
| D.物质的沸点按HF、HCl、HBr、HI的顺序依次增大 |
您最近一年使用:0次
名校
6 . 第ⅤA族元素的原子R与A原子结合形成RA3气态分子,其立体结构呈三角锥形。RCl5在气态和液态时,分子结构如下图所示,下列关于RCl5分子的说法中正确的是( )
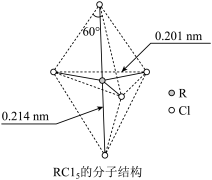

| A.每个原子都达到8电子稳定结构 |
| B.分子中5个R—Cl键键能不相同 |
| C.键角(Cl—R—Cl)有90°、120°、180°几种 |
| D.RCl5受热后会分解生成分子RCl3,RCl5和RCl3都是极性分子 |
您最近一年使用:0次
2019-05-28更新
|
226次组卷
|
11卷引用:【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二下学期期中考试化学试题
【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二下学期期中考试化学试题山西省朔州市怀仁县怀仁一中云东校区2019-2020学年高二下学期期中考试化学试题福建省厦门市湖滨中学2022-2023学年高二下学期期中考试化学试题江苏省溧水高级中学2018-2019高二上学期期末考试化学试题安徽省亳州市第二中学2018-2019学年高二下学期5月月考化学试题山东省枣庄市第三中学2019-2020学年高二下学期3月网上测试化学试题安徽省滁州市明光中学2019-2020学年高二下学期开学考试化学试题江西省宜春市第九中学2019-2020学年高二下学期第二次月考化学(网班)试题福建省福州市八县一中2019-2020学年高二年下学期适应性考试化学试题河南省辉县市一中2020-2021学年高二(培优班)下学期第二次阶段性考试化学试题福建省厦门英才学校中学部22021-2022学年高二下学期4月月考化学试题
名校
7 . 下列叙述正确的是( )
①不同核素之间形成的共价键一定是极性键②当一个碳原子连接四个不同的原子或原子团时,该碳原子叫手性碳原子③Ge是ⅣA族的一个主族元素,其核外电子排布式为Ge:[Ar]4s24p2,属于P区元素④非极性分子往往是高度对称的分子,比如BF3,PCl5,H2O,CO2这样的分子⑤冰中存在极性共价键和氢键两种化学键的作用⑥熔融状态的HgCl2不能导电,HgCl2的稀溶液有弱的导电能力且可作手术刀的消毒液,从不同角度分类HgCl2是一种共价化合物、电解质、盐⑦氨水中大部分NH3与H2O以氢键(用“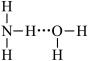 …”表示)结合成NH3•H2O分子,根据氨水的性质可知NH3•H2O的结构式为⑧σ键重叠方式为头碰头,成镜像对称;ð键重叠方式为肩并肩,成轴对称⑨干冰汽化破坏了共价键,氯化钠溶于水破坏了离子键.
…”表示)结合成NH3•H2O分子,根据氨水的性质可知NH3•H2O的结构式为⑧σ键重叠方式为头碰头,成镜像对称;ð键重叠方式为肩并肩,成轴对称⑨干冰汽化破坏了共价键,氯化钠溶于水破坏了离子键.
①不同核素之间形成的共价键一定是极性键②当一个碳原子连接四个不同的原子或原子团时,该碳原子叫手性碳原子③Ge是ⅣA族的一个主族元素,其核外电子排布式为Ge:[Ar]4s24p2,属于P区元素④非极性分子往往是高度对称的分子,比如BF3,PCl5,H2O,CO2这样的分子⑤冰中存在极性共价键和氢键两种化学键的作用⑥熔融状态的HgCl2不能导电,HgCl2的稀溶液有弱的导电能力且可作手术刀的消毒液,从不同角度分类HgCl2是一种共价化合物、电解质、盐⑦氨水中大部分NH3与H2O以氢键(用“
 …”表示)结合成NH3•H2O分子,根据氨水的性质可知NH3•H2O的结构式为⑧σ键重叠方式为头碰头,成镜像对称;ð键重叠方式为肩并肩,成轴对称⑨干冰汽化破坏了共价键,氯化钠溶于水破坏了离子键.
…”表示)结合成NH3•H2O分子,根据氨水的性质可知NH3•H2O的结构式为⑧σ键重叠方式为头碰头,成镜像对称;ð键重叠方式为肩并肩,成轴对称⑨干冰汽化破坏了共价键,氯化钠溶于水破坏了离子键.| A.②⑥ | B.①②⑥ | C.②⑤⑥⑧ | D.③④⑥⑦⑨ |
您最近一年使用:0次
名校
8 . 通常状况下,NCl3是一种油状液体,其分子空间构型与氨分子相似,下列对NCl3的有关叙述正确的是
| A.分子中N-Cl键键长比CCl4分子中C-Cl键键长长 |
| B.分子中不含孤电子对 |
| C.NCl3分子是极性分子 |
| D.NBr3比NCl3易挥发 |
您最近一年使用:0次
名校
9 . 下列实验事实及理论解释都正确的是
| 选项 | 实验事实 | 理论解释 |
| A | 酸性: H3BO3、 H2SiO3 相近 | B、Si电负性相近,符合“对角线规则” |
| B | 熔点: SiO2> SiCl4 | 键能:Si-O>Si-Cl |
| C | 密度:干冰>冰 | 相对分子质量:CO2>H2O |
| D | 沸点: Cl2> N2>CO | CO为极性分子:且相对分子质量:Cl2>CO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-05-18更新
|
196次组卷
|
2卷引用:【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二下学期期中考试化学试题
名校
解题方法
10 . 下列各组分子中都属于含极性键的非极性分子的是( )
| A.SO2、H2O、NH3 | B.CH4、C2H4、C6H6 |
| C.N2、Cl2、CHCl3 | D.H2O2、C2H6、PCl3 |
您最近一年使用:0次



