名校
解题方法
1 . 在半导体生产或灭火剂的使用中,会向空气逸散气体,如 、
、 与
与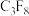 ,它们虽是微量的,有些却是强温室气体,下列有关推测正确的是
,它们虽是微量的,有些却是强温室气体,下列有关推测正确的是
 、
、 与
与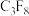 ,它们虽是微量的,有些却是强温室气体,下列有关推测正确的是
,它们虽是微量的,有些却是强温室气体,下列有关推测正确的是A. 属于非极性分子 属于非极性分子 |
B. 属于手性分子 属于手性分子 |
C.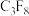 的三个碳原子在同一条直线上 的三个碳原子在同一条直线上 |
D.由价层电子对互斥理论可确定 分子中N原了是 分子中N原了是 杂化,分子呈平面三角形 杂化,分子呈平面三角形 |
您最近半年使用:0次
名校
解题方法
2 . 下列叙述正确的是
| A.只含非极性键的分子一定是非极性分子 |
| B.非极性分子中不可能既含极性键又含有非极性键 |
| C.非极性分子中一定含有非极性键 |
| D.离子化合物中不可能存在非极性键 |
您最近半年使用:0次
2024·黑龙江·模拟预测
3 . 下列有关物质的结构与性质说法正确的是
| A.第二、三周期B、Al的第一电离能高于相邻元素,N、P的第一电离能低于相邻元素 |
| B.键能:F-F大于Cl-Cl |
| C.O3是极性分子,它在水中溶解度高于在四氯化碳的溶解度 |
| D.甲醇分子间的氢键键能大于水分子间的氢键键能 |
您最近半年使用:0次
4 . 下列关于分子的结构和性质的描述中,错误的是
| A.冠醚利用不同大小的空穴适配不同大小的碱金属离子进行“分子识别” |
B.乳酸(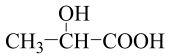 )分子中含有一个手性碳原子 )分子中含有一个手性碳原子 |
| C.碘易溶于浓碘化钾溶液,甲烷难溶于水都可用“相似相溶”原理解释 |
| D.分子极性HF>HCl>HBr>HI |
您最近半年使用:0次
5 . 按要求回答下列问题:
(1)CH4是_______ 形分子,是_______ 分子(填“极性”“非极性”)。
(2)①基态原子的N层有1个未成对电子,M层未成对电子数最多的元素的价电子排布式为_______ 。
②最外层电子数是次外层电子数3倍的元素的轨道表示式为_______ 。
③Cu原子的结构示意图为_______ 。
(3)某元素+3价离子的电子排布式为1s22s22p63s23p63d3,该元素在周期表中的_______ 区。
(4)已知下列四种酸①CH3CBr2COOH②CH3CF2COOH③CH3CH2COOH④CH3COOH酸性由弱到强的顺序为_______ 。
(1)CH4是
(2)①基态原子的N层有1个未成对电子,M层未成对电子数最多的元素的价电子排布式为
②最外层电子数是次外层电子数3倍的元素的轨道表示式为
③Cu原子的结构示意图为
(3)某元素+3价离子的电子排布式为1s22s22p63s23p63d3,该元素在周期表中的
(4)已知下列四种酸①CH3CBr2COOH②CH3CF2COOH③CH3CH2COOH④CH3COOH酸性由弱到强的顺序为
您最近半年使用:0次
解题方法
6 . 硫元素与氯元素可形成 、
、 两种化合物,两种物质中各原子均满足最外层8电子稳定结构,其中
两种化合物,两种物质中各原子均满足最外层8电子稳定结构,其中 是广泛用于橡胶工业的硫化剂,其分子结构如图所示。下列说法错误的是
是广泛用于橡胶工业的硫化剂,其分子结构如图所示。下列说法错误的是
 、
、 两种化合物,两种物质中各原子均满足最外层8电子稳定结构,其中
两种化合物,两种物质中各原子均满足最外层8电子稳定结构,其中 是广泛用于橡胶工业的硫化剂,其分子结构如图所示。下列说法错误的是
是广泛用于橡胶工业的硫化剂,其分子结构如图所示。下列说法错误的是
| A.该分子中S-Cl键的键能大于S-S键的键能 |
B.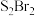 与 与 结构相似,熔沸点: 结构相似,熔沸点: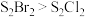 |
C. 为含有极性键和非极性键的非极性分子 为含有极性键和非极性键的非极性分子 |
D. 与 与 分子中的硫原子均采取 分子中的硫原子均采取 杂化 杂化 |
您最近半年使用:0次
名校
7 . 下列有关物质结构与性质的说法错误的是
A. 易溶于 易溶于 ,可从 ,可从 和 和 都是非极性分子的角度解释 都是非极性分子的角度解释 |
B.熔融 能导电,是由于熔融状态下产生了自由移动的 能导电,是由于熔融状态下产生了自由移动的 和 和 |
C. 溶于氨水,是由于 溶于氨水,是由于 与 与 反应生成了可溶性配合物 反应生成了可溶性配合物 |
| D.对羟基苯甲酸存在分子内氢键,是其沸点比邻羟基苯甲酸高的主要原因 |
您最近半年使用:0次
名校
8 . 下列对有关事实的解释不正确的是
| 选项 | 事实 | 解释 |
| A | 氟化氢的沸点比溴化氢的沸点高 | 氟化氢分子间形成氢键 |
| B | 在CS2中的溶解度:CCl4>H2O | CS2、CCl4为非极性分子,而H2O为极性分子 |
| C | 用质谱仪检测乙酸时,谱图出现了质荷比为120的峰 | 两个乙酸分子通过范德华力形成了二聚体 |
| D | 稳定性:[Cu(H2O)4]2+<[Cu(NH3)4]2+ | N的电负性小于O的电负性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
9 . 已知O3的空间结构为V形,分子中正电中心和负电中心不重合,下列有关说法正确的是
A.O3中含有离域π键:π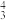 | B.O3分子为非极性分子 |
| C.O3转化为O2为物理变化 | D.O3在水中溶解度比O2在水中溶解度小 |
您最近半年使用:0次
名校
解题方法
10 . 下列各组物质性质的比较,结论正确的是
A.分子的极性: | B.物质的键能:C-C<Si-Si |
C.物质的沸点: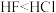 | D.在CS2中的溶解度:CCl4<H2O |
您最近半年使用:0次
2024-04-30更新
|
71次组卷
|
2卷引用:黑龙江省哈尔滨市第三十二中学校2023-2024学年高二下学期4月期中考试化学试题



