名校
1 . 按要求填空:
(1)在①N2②CS2③H2Se④AsH3⑤(CN)2⑥HCHO⑦CH2Cl2⑧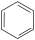 ⑨BF3⑩H2O2中,仅由
⑨BF3⑩H2O2中,仅由 极性键构成的极性分子有
极性键构成的极性分子有_____ ;含有π键,且属于非极性分子的是_____ ;既含有极性键又含有非极性键的分子为_____ ;⑩为_____ (填”极性”或“非极性”)分子。
(2)已知下列四种酸①CH3CBr2COOH②CH3CF2COOH③CH3CH2COOH④CH3COOH酸性由弱到强的顺序为_____ 。
(3)已知BF3和过量NaF作用可生成NaBF4,BF 的空间结构为
的空间结构为_____ ;NaBF4的电子式为_____ 。
(1)在①N2②CS2③H2Se④AsH3⑤(CN)2⑥HCHO⑦CH2Cl2⑧
 ⑨BF3⑩H2O2中,仅由
⑨BF3⑩H2O2中,仅由 极性键构成的极性分子有
极性键构成的极性分子有(2)已知下列四种酸①CH3CBr2COOH②CH3CF2COOH③CH3CH2COOH④CH3COOH酸性由弱到强的顺序为
(3)已知BF3和过量NaF作用可生成NaBF4,BF
 的空间结构为
的空间结构为
您最近一年使用:0次
名校
解题方法
2 . 按要求回答下列问题。
(1)H3O+中心原子采用______ 杂化,其键角比H2O中键角______ (填“大”或“小”)。
(2)有如下分子:①PCl5②PCl3③BF3④BeCl2⑤NF3⑥CO2⑦HCl⑧H2O2⑨CH4⑩C2H4
①上述分子中每个原子周围都满足8电子结构的是______ (填序号)。
②CO2分子中σ键和π键个数之比为______ 。
③含有极性键的极性分子有_____ (填序号)。
④空间结构为三角锥形的分子是______ (填序号)。
(1)H3O+中心原子采用
(2)有如下分子:①PCl5②PCl3③BF3④BeCl2⑤NF3⑥CO2⑦HCl⑧H2O2⑨CH4⑩C2H4
①上述分子中每个原子周围都满足8电子结构的是
②CO2分子中σ键和π键个数之比为
③含有极性键的极性分子有
④空间结构为三角锥形的分子是
您最近一年使用:0次
2023-05-07更新
|
192次组卷
|
3卷引用:黑龙江省牡丹江市第三高级中学2022-2023学年高二下学期期中考试化学试题
名校
3 . 按要求回答下列问题:
(1)①基态原子的N能层有1个未成对电子,M能层未成对电子数最多的元素是__________ (填元素符号,下同),其价层电子排布式为__________ 。
②最外层电子数是次外层电子数3倍的元素是__________ ,其轨道表示式为__________ 。
③ 原子的结构示意图为
原子的结构示意图为__________ 。
(2)H、C、N、O、 的原子半径从小到大的顺序为
的原子半径从小到大的顺序为__________ 。
(3) 是直线形分子,
是直线形分子, 是
是__________ 分子(填“极性”“非极性”)。
(1)①基态原子的N能层有1个未成对电子,M能层未成对电子数最多的元素是
②最外层电子数是次外层电子数3倍的元素是
③
 原子的结构示意图为
原子的结构示意图为(2)H、C、N、O、
 的原子半径从小到大的顺序为
的原子半径从小到大的顺序为(3)
 是直线形分子,
是直线形分子, 是
是
您最近一年使用:0次
4 . 已知: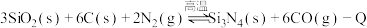 (Q>0),在反应条件下,向
(Q>0),在反应条件下,向 密闭容器中加入反应物,
密闭容器中加入反应物, 后达到平衡。完成下列填空:
后达到平衡。完成下列填空:
(1)氮原子的核外电子排布式:_______ ;硅原子核外电子的运动状态有_______ 种。
(2)上述反应混合物中的极性分子是_______ ,写出非极性分子的电子式_______ 。
(3)将 三种离子的半径按由大到小的顺序排列
三种离子的半径按由大到小的顺序排列_______ 。
(4)氧原子核外电子占有_______ 种能量不同的轨道。
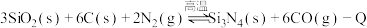 (Q>0),在反应条件下,向
(Q>0),在反应条件下,向 密闭容器中加入反应物,
密闭容器中加入反应物, 后达到平衡。完成下列填空:
后达到平衡。完成下列填空:(1)氮原子的核外电子排布式:
(2)上述反应混合物中的极性分子是
(3)将
 三种离子的半径按由大到小的顺序排列
三种离子的半径按由大到小的顺序排列(4)氧原子核外电子占有
您最近一年使用:0次
名校
解题方法
5 . ①NH3 ②CO2 ③SiCl4 ④BF3 ⑤C2H4 ⑥H2O2 ⑦Cl2 ⑧P4 ⑨H2S
(1)含极性共价键的非极性分子___________ (填序号,下同)
(2)含非极性共价键的非极性分子___________
(3)含极性共价键的极性分子___________
(4)①NH3中心原子杂化方式___________ 分子的空间构型___________
(5)④BF3中心原子杂化方式___________ 分子的空间构型___________
(1)含极性共价键的非极性分子
(2)含非极性共价键的非极性分子
(3)含极性共价键的极性分子
(4)①NH3中心原子杂化方式
(5)④BF3中心原子杂化方式
您最近一年使用:0次
解题方法
6 . 已知H与O可以形成 和
和 两种化合物。请完成下列空白:
两种化合物。请完成下列空白:
(1) 内的O—H、水分子间的范德华力和氢键,从强到弱依次为
内的O—H、水分子间的范德华力和氢键,从强到弱依次为___________ 。 可与
可与 形成
形成 ,
, 中O采用
中O采用___________ 杂化。 中
中 键角比
键角比 中的
中的___________ ,原因为___________ 。
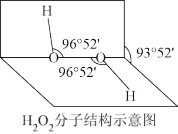
(2) 是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。
是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。 的电子式是
的电子式是___________ ,结构式是___________ 。 是含有
是含有___________ 键和___________ 键的分子(填“极性”或“非极性”)。 能与水混溶,却不溶于
能与水混溶,却不溶于 。请予以解释:
。请予以解释:___________ 。
 和
和 两种化合物。请完成下列空白:
两种化合物。请完成下列空白:(1)
 内的O—H、水分子间的范德华力和氢键,从强到弱依次为
内的O—H、水分子间的范德华力和氢键,从强到弱依次为 可与
可与 形成
形成 ,
, 中O采用
中O采用 中
中 键角比
键角比 中的
中的(2)
 是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。
是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。 的电子式是
的电子式是 是含有
是含有 能与水混溶,却不溶于
能与水混溶,却不溶于 。请予以解释:
。请予以解释:
您最近一年使用:0次
2021-12-03更新
|
1137次组卷
|
2卷引用:黑龙江省肇东市第四中学2021-2022学年高二下学期期中考试化学试题
名校
7 . 根据所学内容填空:
(1)有下列物质:① 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ ,其中属于极性分子的是
,其中属于极性分子的是___________  填序号,下同
填序号,下同 ,既有
,既有 键又有
键又有 键的是
键的是___________ 。
(2)下列分子中,空间构型为正四面体形且键角为 的是
的是___________ 。
a.PCl3 b.SiF4 c.CH2F2 d.P4 e.CH4 f.NH3
(3)下列分子或离子中不存在配位键的是___________ 。
a.H3O+ b. c.Fe(SCN)2+ d.Ni(CO)4 e.
c.Fe(SCN)2+ d.Ni(CO)4 e. ]2+
]2+
(4) 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是___________ 。
(5)丙烯腈分子 中碳原子轨道杂化类型是
中碳原子轨道杂化类型是___________ 。
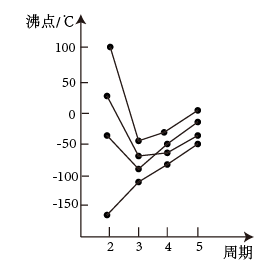
(6)如图所示,每条折线表示周期表ⅣA-ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是___________ (化学式)。
(1)有下列物质:①
 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ ,其中属于极性分子的是
,其中属于极性分子的是 填序号,下同
填序号,下同 ,既有
,既有 键又有
键又有 键的是
键的是(2)下列分子中,空间构型为正四面体形且键角为
 的是
的是a.PCl3 b.SiF4 c.CH2F2 d.P4 e.CH4 f.NH3
(3)下列分子或离子中不存在配位键的是
a.H3O+ b.
 c.Fe(SCN)2+ d.Ni(CO)4 e.
c.Fe(SCN)2+ d.Ni(CO)4 e. ]2+
]2+(4)
 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是(5)丙烯腈分子
 中碳原子轨道杂化类型是
中碳原子轨道杂化类型是(6)如图所示,每条折线表示周期表ⅣA-ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是

您最近一年使用:0次
名校
解题方法
8 . 已知PH3与NH3结构相似,回答下列问题:
①PH3的电子式________ ,结构式________ 。
②几何构型为________ 。
③中心原子采取________ 杂化。
④PH3分子中的化学键________ (填“有”或“无”)极性,其分子为________ (填“极性”或”非极性”)分子。
⑤PH3与NH3的热稳定性:________ 更强。
①PH3的电子式
②几何构型为
③中心原子采取
④PH3分子中的化学键
⑤PH3与NH3的热稳定性:
您最近一年使用:0次
2020-03-06更新
|
316次组卷
|
2卷引用:黑龙江省桦南县第二中学2019-2020学年高二下学期期中考试化学试题
解题方法
9 . 我国科学家借助自主研制的新型钨钴合金催化剂攻克了单壁碳纳米管结构的可控制备难题。

(1)基态钴原子的核外未成对电子数为__________ 。单壁碳纳米管可看作石墨烯沿一定方向卷曲而成的空心圆柱体,其结构如图所示,其中碳原子的杂化方式为_______ 。
(2)纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化,已知甲醛各原子均满足稳定结构,甲醛分子属______ 分子(选填“极性”“非极性”),其分子的空间构型为_____ 。新制备的Cu(OH)2可将乙醛(CH3CHO)氧化为乙酸,而自身还原成Cu2O,乙酸的沸点明显高于乙醛,其主要原因是______ 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有______ 个铜原子。金属Cu为________ 堆积,配位数为_______ 。
(3)橙红色晶体羰基钴的熔点为52℃,分子式为Co2(CO)8,是一种重要的配合物,可溶于多数有机溶剂。该晶体属于______ 晶体,三种元素电负性由大到小的顺序为(填元素符号)_____ 。配体CO的任意一种等电子体的电子式:_____ 。配体CO中与Co形成配位键的原子是C而不是O的原因是________ 。

(1)基态钴原子的核外未成对电子数为
(2)纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化,已知甲醛各原子均满足稳定结构,甲醛分子属
(3)橙红色晶体羰基钴的熔点为52℃,分子式为Co2(CO)8,是一种重要的配合物,可溶于多数有机溶剂。该晶体属于
您最近一年使用:0次
名校
10 . 元素A、B、C都是短周期元素,A元素原子的2p轨道上只有两个未成对电子,B的3p轨道上有空轨道,A、B同主族,B、C同周期,C是本周期中电负性最大的.
请回答:
(1)A原子的核外电子排布的电子排布图______________ ,B原子的核外电子排布式________ ,C原子的价电子排布式____________ 。
(2)A、B、C的气态氢化物的化学式分别是___________ ,其中最不稳定的是__________ 。
(3)它们的最高价氧化物的水化物中,酸性最强的是_________ 。
(4)AC4的化学式___________ ,结构式__________ ,中心原子A的杂化方式________ 杂化,是__________ (填“极性”或“非极性”)分子。
请回答:
(1)A原子的核外电子排布的电子排布图
(2)A、B、C的气态氢化物的化学式分别是
(3)它们的最高价氧化物的水化物中,酸性最强的是
(4)AC4的化学式
您最近一年使用:0次



