名校
解题方法
1 . 化合物T是一种用于合成药物的重要试剂,其结构简式如图所示。已知X、Y、Z、M、N为原子序数依次增大的前四周期主族元素,Z、M位于同一主族,X、Y、N的最外层电子数之和等于Z的最外层电子数。下列有关叙述正确的是


| A.原子半径:M>N>Z |
| B.简单氢化物稳定性和沸点均为:Z>M |
| C.化合物YM2与YZM均为非极性分子 |
| D.化合物T中所有原子均满足8电子相对稳定结构 |
您最近一年使用:0次
名校
2 . 按要求填空:
(1)在①N2②CS2③H2Se④AsH3⑤(CN)2⑥HCHO⑦CH2Cl2⑧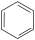 ⑨BF3⑩H2O2中,仅由
⑨BF3⑩H2O2中,仅由 极性键构成的极性分子有
极性键构成的极性分子有_____ ;含有π键,且属于非极性分子的是_____ ;既含有极性键又含有非极性键的分子为_____ ;⑩为_____ (填”极性”或“非极性”)分子。
(2)已知下列四种酸①CH3CBr2COOH②CH3CF2COOH③CH3CH2COOH④CH3COOH酸性由弱到强的顺序为_____ 。
(3)已知BF3和过量NaF作用可生成NaBF4,BF 的空间结构为
的空间结构为_____ ;NaBF4的电子式为_____ 。
(1)在①N2②CS2③H2Se④AsH3⑤(CN)2⑥HCHO⑦CH2Cl2⑧
 ⑨BF3⑩H2O2中,仅由
⑨BF3⑩H2O2中,仅由 极性键构成的极性分子有
极性键构成的极性分子有(2)已知下列四种酸①CH3CBr2COOH②CH3CF2COOH③CH3CH2COOH④CH3COOH酸性由弱到强的顺序为
(3)已知BF3和过量NaF作用可生成NaBF4,BF
 的空间结构为
的空间结构为
您最近一年使用:0次
名校
解题方法
3 . 按要求回答下列问题。
(1)H3O+中心原子采用______ 杂化,其键角比H2O中键角______ (填“大”或“小”)。
(2)有如下分子:①PCl5②PCl3③BF3④BeCl2⑤NF3⑥CO2⑦HCl⑧H2O2⑨CH4⑩C2H4
①上述分子中每个原子周围都满足8电子结构的是______ (填序号)。
②CO2分子中σ键和π键个数之比为______ 。
③含有极性键的极性分子有_____ (填序号)。
④空间结构为三角锥形的分子是______ (填序号)。
(1)H3O+中心原子采用
(2)有如下分子:①PCl5②PCl3③BF3④BeCl2⑤NF3⑥CO2⑦HCl⑧H2O2⑨CH4⑩C2H4
①上述分子中每个原子周围都满足8电子结构的是
②CO2分子中σ键和π键个数之比为
③含有极性键的极性分子有
④空间结构为三角锥形的分子是
您最近一年使用:0次
2023-05-07更新
|
187次组卷
|
3卷引用:黑龙江省牡丹江市第三高级中学2022-2023学年高二下学期期中考试化学试题
名校
4 . 磷化氢( )是一种无色剧毒,有类似大蒜气味的气体,微溶于冷水。下列关于
)是一种无色剧毒,有类似大蒜气味的气体,微溶于冷水。下列关于 的叙述错误的是
的叙述错误的是
 )是一种无色剧毒,有类似大蒜气味的气体,微溶于冷水。下列关于
)是一种无色剧毒,有类似大蒜气味的气体,微溶于冷水。下列关于 的叙述错误的是
的叙述错误的是A. 分子中有未成键的电子对 分子中有未成键的电子对 | B. 是极性分子 是极性分子 |
C. 分子构型为三角锥形 分子构型为三角锥形 | D. 能与水形成分子间氢键 能与水形成分子间氢键 |
您最近一年使用:0次
2023-05-06更新
|
45次组卷
|
2卷引用:黑龙江省绥化市绥棱县第一中学2023-2024学年高二下学期开学化学试题
5 . 六氟化硫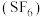 分子为正八面体构型,难溶于水,在高温下仍有良好的绝缘性,在电器工业方面具有广泛用途。下列推测正确的是
分子为正八面体构型,难溶于水,在高温下仍有良好的绝缘性,在电器工业方面具有广泛用途。下列推测正确的是
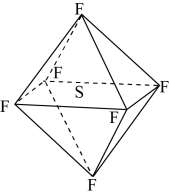
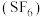 分子为正八面体构型,难溶于水,在高温下仍有良好的绝缘性,在电器工业方面具有广泛用途。下列推测正确的是
分子为正八面体构型,难溶于水,在高温下仍有良好的绝缘性,在电器工业方面具有广泛用途。下列推测正确的是
A. 中心原子的价层电子对数为4 中心原子的价层电子对数为4 |
B. 各原子均达到最外层8电子稳定结构 各原子均达到最外层8电子稳定结构 |
C. 分子是极性分子 分子是极性分子 |
D. 分子中的 分子中的 键都是 键都是 键,且键长、键能都相等 键,且键长、键能都相等 |
您最近一年使用:0次
名校
6 . 有A、B、C、D、E、F、G7种元素,它们的核电荷数依次增大,且A~E都为短周期元素。其中G元素是1826年一位法国青年科学家发现的,他在研究海水制盐时向剩余的副产物(苦卤)中通入氯气后发现溶液的颜色变深,经过一步提取可得红棕色液体,有刺激性气味;A为非金属元素,A和F属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上的电子数等于D原子最外层上电子数的一半。请回答下列问题:
(1)写出下列元素的名称:A:_____ ,C:_____ ,E:_____ ,G:_____ 。
(2)G元素在周期表中的位置为:______ ;其价电子排布图为:______ 。
(3)由A、B、C、D、F五种元素组成的一种化合物为______ (写化学式),并写出该物质的一种用途______ 。
(4)已知由D和E形成的一种化合物D2E2是一种橙黄色液体遇水剧烈反应,产生能使品红溶液褪色的气体。
①D2E2中E为_____ 价;且该物质为_____ (填”极性”或“非极性”)分子。
②写出D2E2与水反应的化学方程式______ 。
(1)写出下列元素的名称:A:
(2)G元素在周期表中的位置为:
(3)由A、B、C、D、F五种元素组成的一种化合物为
(4)已知由D和E形成的一种化合物D2E2是一种橙黄色液体遇水剧烈反应,产生能使品红溶液褪色的气体。
①D2E2中E为
②写出D2E2与水反应的化学方程式
您最近一年使用:0次
名校
解题方法
7 . 原子总数相同、价电子总数相同的分子称为等电子体,它们具有相似的化学键特征。B3N3H6(无机苯)的结构与苯类似。下列关于B3N3H6的说法错误的是
| A.无机苯与苯互为等电子体 | B.B3N3H6中含有3个π键 |
| C.分子中B和N均为sp2杂化 | D.B3N3H6(无机苯)难溶于水 |
您最近一年使用:0次
名校
8 . 下列说法不正确的是
| A.乙烯分子中的σ键和π键之比为5∶1 |
| B.某元素气态基态原子的逐级电离能(kJ•mol-1)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是X2+ |
| C.Na、P、Cl的电负性依次增大 |
| D.乙醇和水都是非极性分子,符合相似相溶规律,且它们易形成分子间氢键,故乙醇易溶于水 |
您最近一年使用:0次
名校
9 . 按要求回答下列问题:
(1)①基态原子的N能层有1个未成对电子,M能层未成对电子数最多的元素是__________ (填元素符号,下同),其价层电子排布式为__________ 。
②最外层电子数是次外层电子数3倍的元素是__________ ,其轨道表示式为__________ 。
③ 原子的结构示意图为
原子的结构示意图为__________ 。
(2)H、C、N、O、 的原子半径从小到大的顺序为
的原子半径从小到大的顺序为__________ 。
(3) 是直线形分子,
是直线形分子, 是
是__________ 分子(填“极性”“非极性”)。
(1)①基态原子的N能层有1个未成对电子,M能层未成对电子数最多的元素是
②最外层电子数是次外层电子数3倍的元素是
③
 原子的结构示意图为
原子的结构示意图为(2)H、C、N、O、
 的原子半径从小到大的顺序为
的原子半径从小到大的顺序为(3)
 是直线形分子,
是直线形分子, 是
是
您最近一年使用:0次
名校
解题方法
10 . 下列叙述中,错误的是
A. 的熔沸点比 的熔沸点比 高,与分子间的范德华力有关系 高,与分子间的范德华力有关系 |
B. 易溶于 易溶于 ,可用相似相溶规律解释 ,可用相似相溶规律解释 |
C. 分子中 分子中 键与 键与 键个数比为4∶1 键个数比为4∶1 |
D. 为V形极性分子,微粒间的作用力为范德华力 为V形极性分子,微粒间的作用力为范德华力 |
您最近一年使用:0次
2023-03-31更新
|
289次组卷
|
2卷引用:黑龙江省 牡丹江市第二高级中学2023-2024学年高三上学期12月月考化学试题



