名校
解题方法
1 . 下列各组物质性质的比较,结论正确的是
A.分子的极性: | B.物质的键能:C-C<Si-Si |
C.物质的沸点: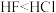 | D.在CS2中的溶解度:CCl4<H2O |
您最近一年使用:0次
2024-04-30更新
|
74次组卷
|
2卷引用:黑龙江省哈尔滨市第三十二中学校2023-2024学年高二下学期4月期中考试化学试题
名校
解题方法
2 . 下列说法中正确的是
| A.CH4、C2H4、HCN都是含有极性键的非极性分子 |
B. 与 与 的立体构型相似,都是非极性分子 的立体构型相似,都是非极性分子 |
C.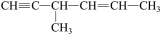 分子中含有 分子中含有 个手性碳原子 个手性碳原子 |
D. 键的电子云图形是镜面对称的,而 键的电子云图形是镜面对称的,而 键的电子云图形是轴对称的 键的电子云图形是轴对称的 |
您最近一年使用:0次
名校
3 . 下列关系错误的是
A.沸点: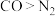 | B.第一电离能: |
C.在水中的溶解度: | D.还原性:稀盐酸<浓盐酸 |
您最近一年使用:0次
名校
4 .  和CO是污染性气体,可在
和CO是污染性气体,可在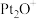 表面转化为无害气体,有关化学反应的物质变化过程如图1所示,总反应的能量变化过程如图2所示,下列说法正确的是
表面转化为无害气体,有关化学反应的物质变化过程如图1所示,总反应的能量变化过程如图2所示,下列说法正确的是
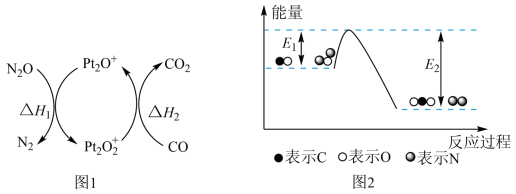
 和CO是污染性气体,可在
和CO是污染性气体,可在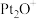 表面转化为无害气体,有关化学反应的物质变化过程如图1所示,总反应的能量变化过程如图2所示,下列说法正确的是
表面转化为无害气体,有关化学反应的物质变化过程如图1所示,总反应的能量变化过程如图2所示,下列说法正确的是
A.总反应的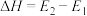 |
B.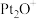 降低了总反应的焓变 降低了总反应的焓变 |
| C.总反应中氧化剂和还原剂的物质的量之比为2:1 |
D. 、 、 均为非极性分子 均为非极性分子 |
您最近一年使用:0次
2023-11-10更新
|
140次组卷
|
2卷引用:黑龙江省大庆铁人中学2023-2024学年高三上学期期中考试化学试题
名校
5 . 一种含Pt催化剂活化甲烷中碳氢键的反应机理如图所示。下列说法错误的是
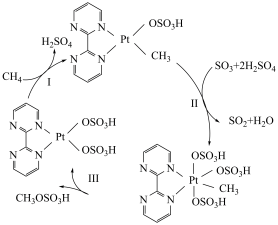

A. 、 、 分别是非极性分子、极性分子 分别是非极性分子、极性分子 |
| B.催化循环中S的VSEPR模型相同 |
C.配体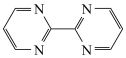 完全加氢后产物含两个手性碳原子 完全加氢后产物含两个手性碳原子 |
D.上述过程的总反应: |
您最近一年使用:0次
名校
6 . 化学学习中常用类推方法,下列类推正确的是
| A.CO2为直线形分子,SO2也为直线形分子 |
| B.CH4为非极性分子,则CCl4也为非极性分子 |
| C.NH3的VSEPR模型为四面体,BF3的VSEPR模型也为四面体 |
| D.CO2中存在π键,则SiO2中也存在π键 |
您最近一年使用:0次
名校
解题方法
7 . 某研究小组制造了一种“水瓶”,用富勒烯(C60)的球形笼子作“瓶体”,一种磷酸盐作“瓶盖”,恰好可将一个水分子关在里面。下列说法正确的是
| A.“水瓶”是纯净物 | B.水分子空间构型是V形 |
| C.C60是极性分子 | D.富勒烯与石墨是同分异构体 |
您最近一年使用:0次
名校
8 . 下表为周期表的一部分,其中的编号代表对应的元素。
请回答下列问题:
(1)③基态原子的核外电子轨道表示式是___________ 。
(2)写出元素⑩的一价离子的核外电子排布式:___________ ,该元素属于___________ 区元素。
(3)由元素④构成的三原子分子的空间结构为___________ 。
(4)元素④⑥⑦的气态氢化物热稳定性由强到弱的顺序为:___________ (填化学式)。
(5)③与①以原子个数比为 形成的化合物X可用于火箭发射的燃料,其中③的杂化轨道类型为
形成的化合物X可用于火箭发射的燃料,其中③的杂化轨道类型为___________ ,X为___________ (极性分子或非极性分子)
(6)已知周期表中存在对角相似规则,如②与⑤在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑨的氢氧化物反应的化学方程式___________ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑨ | ⑤ | ⑥ | ⑦ | ⑧ | |||||||||||||
| ⑩ | |||||||||||||||||
(1)③基态原子的核外电子轨道表示式是
(2)写出元素⑩的一价离子的核外电子排布式:
(3)由元素④构成的三原子分子的空间结构为
(4)元素④⑥⑦的气态氢化物热稳定性由强到弱的顺序为:
(5)③与①以原子个数比为
 形成的化合物X可用于火箭发射的燃料,其中③的杂化轨道类型为
形成的化合物X可用于火箭发射的燃料,其中③的杂化轨道类型为(6)已知周期表中存在对角相似规则,如②与⑤在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑨的氢氧化物反应的化学方程式
您最近一年使用:0次
名校
9 . 下列说法中正确的是
A.价层电子排布为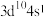 的原子位于第四周期第ⅠA族,属于s区元素 的原子位于第四周期第ⅠA族,属于s区元素 |
B. 为极性分子, 为极性分子, 为非极性分子 为非极性分子 |
C.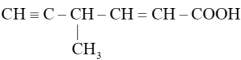 分子中含有2个手性碳原子 分子中含有2个手性碳原子 |
D. 和的中心原 和的中心原 子均为 子均为 杂化, 杂化, 分子呈正四面体形, 分子呈正四面体形, 呈三角锥形 呈三角锥形 |
您最近一年使用:0次
名校
10 . 下列说法中不正确的是
| A.HF、HCl、HBr、HI的熔、沸点依次升高 |
| B.氨气极易溶于水,是因为氨气与水分子间可形成氢键 |
C.萘(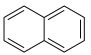 )和碘易溶于四氯化碳,难溶于水,因为萘、碘、四氯化碳都是非极性分子 )和碘易溶于四氯化碳,难溶于水,因为萘、碘、四氯化碳都是非极性分子 |
D.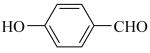 的沸点高于 的沸点高于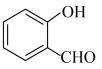 |
您最近一年使用:0次



