1 . 下列对一些实验事实的解释错误的是
| 选项 | 实验事实 | 解释 |
| A | 水加热到较高温度难以分解 | 水分子中共价键键能较大 |
| B | 石墨棒作为原电池的电极材料 | 石墨晶体能导电 |
| C |  的沸点高于 的沸点高于 | H-N键的键长比H-P键的键长短 |
| D | 用X射线实验区分玻璃和水晶 | 水晶的衍射图上有明锐的衍射峰 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 离子液体因其不挥发性、无色、无臭、较好的化学稳定性被誉为二十一世纪的绿色化学溶剂,某离子液体(结构如下)在触觉传感器中应用广泛。X、Y、Z均为短周期主族元素,原子序数依次增大,Y是非金属性最强的元素。下列说法正确的是
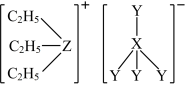
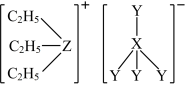
| A.原子半径:X>Y>Z |
| B.最高价氧化物的水化物的酸性:Y>Z>X |
| C.简单氢化物的沸点:Y>Z |
| D.该离子液体中各元素原子均满足8电子稳定结构 |
您最近一年使用:0次
名校
3 . 下列有关物质结构与性质的说法错误的是
A. 所含元素中基态原子未成对电子数最多的是P 所含元素中基态原子未成对电子数最多的是P |
| B.HF在标准状况下为液态的重要原因是HF分子间存在氢键 |
| C.晶莹剔透的水晶中含有硅氧四面体结构 |
| D.石墨晶体的层状结构之间存在分子间作用力,因此具有导电性 |
您最近一年使用:0次
4 . 以CO2为原料催化加氢可以制备CH4、CH3OH、C2H4,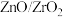 为我国科学家发明的二氧化碳加氢的一种催化剂。回答下列问题:
为我国科学家发明的二氧化碳加氢的一种催化剂。回答下列问题:
(1)基态 原子电子排布式为
原子电子排布式为______ ,其核外电子空间运动状态有______ 种。
(2)每个基态氧原子含有未成对电子的数目为______ ,同一周期第一电离能大趋势在逐渐增大,但是存在反常,比如 ,请解释原因:
,请解释原因:________________________ 。
(3) 催化加氢制备
催化加氢制备 的化学方程式为
的化学方程式为 。
。
①等物质的量的CH3OH和CO2分子中 键数目之比为
键数目之比为______ 。
②沸点:CH3OH______ (填“>”或“<”)CH4,其原因为______ 。
(4)四方体 晶胞结构如图所示,原子坐标参数表示晶胞内部各原子的相对位置,
晶胞结构如图所示,原子坐标参数表示晶胞内部各原子的相对位置, 、
、 、
、 原子的坐标参数分别为
原子的坐标参数分别为 、
、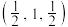 ,
, 。
。

①R原子的坐标参数为______ 。
②假设ZrO2的密度为 ,摩尔质量为
,摩尔质量为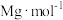 ,
, 表示阿伏加德罗常数的值,则晶胞中Zr原子和O原子的最短距离为
表示阿伏加德罗常数的值,则晶胞中Zr原子和O原子的最短距离为______  (列出算式即可)。
(列出算式即可)。
 为我国科学家发明的二氧化碳加氢的一种催化剂。回答下列问题:
为我国科学家发明的二氧化碳加氢的一种催化剂。回答下列问题:(1)基态
 原子电子排布式为
原子电子排布式为(2)每个基态氧原子含有未成对电子的数目为
 ,请解释原因:
,请解释原因:(3)
 催化加氢制备
催化加氢制备 的化学方程式为
的化学方程式为 。
。①等物质的量的CH3OH和CO2分子中
 键数目之比为
键数目之比为②沸点:CH3OH
(4)四方体
 晶胞结构如图所示,原子坐标参数表示晶胞内部各原子的相对位置,
晶胞结构如图所示,原子坐标参数表示晶胞内部各原子的相对位置, 、
、 、
、 原子的坐标参数分别为
原子的坐标参数分别为 、
、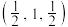 ,
, 。
。
①R原子的坐标参数为
②假设ZrO2的密度为
 ,摩尔质量为
,摩尔质量为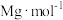 ,
, 表示阿伏加德罗常数的值,则晶胞中Zr原子和O原子的最短距离为
表示阿伏加德罗常数的值,则晶胞中Zr原子和O原子的最短距离为 (列出算式即可)。
(列出算式即可)。
您最近一年使用:0次
解题方法
5 . 已知 是阿伏加德罗常数的值。下列说法中正确的是
是阿伏加德罗常数的值。下列说法中正确的是
 是阿伏加德罗常数的值。下列说法中正确的是
是阿伏加德罗常数的值。下列说法中正确的是A.含 共价键的水蒸气中,分子间存在 共价键的水蒸气中,分子间存在 个氢键 个氢键 |
B.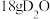 和 和 含有的质子数均为 含有的质子数均为 |
C.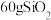 中 中 键的个数为 键的个数为 |
D.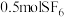 中硫的价层电子对数为 中硫的价层电子对数为 |
您最近一年使用:0次
解题方法
6 . 化合物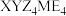 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为
可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周期,E元素原子最外层电子数是次外层的3倍。下列说法正确的是
,X与M同周期,E元素原子最外层电子数是次外层的3倍。下列说法正确的是
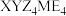 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为
可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周期,E元素原子最外层电子数是次外层的3倍。下列说法正确的是
,X与M同周期,E元素原子最外层电子数是次外层的3倍。下列说法正确的是A.元素电负性: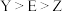 |
B.最简单氢化物沸点: |
C.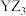 和 和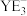 的空间结构均为三角锥形 的空间结构均为三角锥形 |
D.第一电离能: |
您最近一年使用:0次
7 . 下列说法正确的是
A. 分子中的键角为120° 分子中的键角为120° | B. 和 和 均为Ⅴ形分子 均为Ⅴ形分子 |
C. 能形成分子间氢键 能形成分子间氢键 | D. 分子中 分子中 键和 键和 键的数目之比为1∶2 键的数目之比为1∶2 |
您最近一年使用:0次
解题方法
8 . 随原子序数递增,下列关于ⅦA族元素性质变化的说法错误的是
| A.原子半径逐渐增大 | B.第一电离能逐渐减小 |
| C.氢化物的沸点逐渐升高 | D.最高价氧化物水化物的酸性逐渐减弱 |
您最近一年使用:0次
名校
9 . 物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
| 选项 | 性质差异 | 结构因素 |
| A | 沸点:正戊烷(36.1℃)高于新戊烷(9.5℃) | 分子间作用力 |
| B | 溶解度(20℃): 大于 大于 | 阴离子电荷 |
| C | 熔点: 远高于 远高于 (178℃升华) (178℃升华) | 晶体类型 |
| D | 酸性: 远强于 远强于 | 羟基极性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-12更新
|
216次组卷
|
2卷引用:河南省驻马店市2022-2023学年高二下学期期末考试化学试题
解题方法
10 . 下列物质结构或性质比较中,前者大于后者的是
A.熔点:NaCl、 | B.沸点: 、 、 |
C.简单离子半径: 、 、 | D.酸性: 、 、 |
您最近一年使用:0次



