名校
解题方法
1 . 元素周期表中第四周期的某些过渡元素(如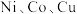 等)在生产、生活中有着广泛的应用.
等)在生产、生活中有着广泛的应用.
(1) 能与水杨醛缩对氯苯胺形成具有发光性的配合物,水杨醛缩对氯苯胺制备反应方程式如下:
能与水杨醛缩对氯苯胺形成具有发光性的配合物,水杨醛缩对氯苯胺制备反应方程式如下: 核外电子排布式
核外电子排布式_________ ;
② 元素的第一电离能由大到小的顺序为
元素的第一电离能由大到小的顺序为__________ . 的晶胞如图1所示,距离每个
的晶胞如图1所示,距离每个 最近的
最近的 的个数为
的个数为_________ .
(3)已知: 结构如图2所示,该反应
结构如图2所示,该反应________ (选填“是”或“不是”)氧化还原反应,理由是__________ .
(4)有机净化剂的基本组分为大分子立体网格结构的聚合物,可用于工业废水“除钴镍”.其净化原理可表示为: ”表示出
”表示出 参与的配位键
参与的配位键_________ .
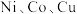 等)在生产、生活中有着广泛的应用.
等)在生产、生活中有着广泛的应用.(1)
 能与水杨醛缩对氯苯胺形成具有发光性的配合物,水杨醛缩对氯苯胺制备反应方程式如下:
能与水杨醛缩对氯苯胺形成具有发光性的配合物,水杨醛缩对氯苯胺制备反应方程式如下:
 核外电子排布式
核外电子排布式②
 元素的第一电离能由大到小的顺序为
元素的第一电离能由大到小的顺序为③对羟基苯甲醛( )的沸点为
)的沸点为 ,而水杨醛(
,而水杨醛(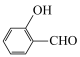 )的沸点为
)的沸点为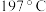 ,请从结构角度解释二者沸点差异原因
,请从结构角度解释二者沸点差异原因
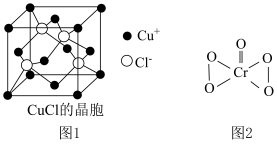
 的晶胞如图1所示,距离每个
的晶胞如图1所示,距离每个 最近的
最近的 的个数为
的个数为(3)已知:
 结构如图2所示,该反应
结构如图2所示,该反应(4)有机净化剂的基本组分为大分子立体网格结构的聚合物,可用于工业废水“除钴镍”.其净化原理可表示为:
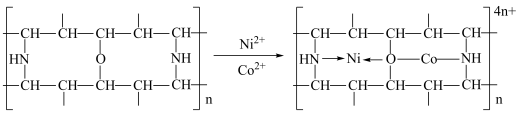
 ”表示出
”表示出 参与的配位键
参与的配位键
您最近一年使用:0次
2024-05-04更新
|
203次组卷
|
2卷引用:河南省郑州市宇华实验学校2023-2024学年高二下学期4月期中考试化学试题
名校
2 . 已知 、
、 分别在850℃、300℃能大量分解,对此事实解释合理的是
分别在850℃、300℃能大量分解,对此事实解释合理的是
 、
、 分别在850℃、300℃能大量分解,对此事实解释合理的是
分别在850℃、300℃能大量分解,对此事实解释合理的是A. 能形成氢键而 能形成氢键而 不能 不能 | B.As—H键的键能小于N—H键的键能 |
C. 是极性分子而 是极性分子而 是非极性分子 是非极性分子 | D. 极易溶于水而 极易溶于水而 不能 不能 |
您最近一年使用:0次
名校
3 . 下列事实与氢键无关的是
A. 的沸点低于 的沸点低于 | B. 的熔点高于 的熔点高于 |
C. 的沸点高于 的沸点高于 | D. 比 比 更易溶于水 更易溶于水 |
您最近一年使用:0次
2023-12-26更新
|
135次组卷
|
4卷引用:河南省商丘市二十校2023-2024学年高二下学期期中联考化学试卷
名校
4 . 2022年诺贝尔化学奖授予了点击化学等领域。我国科学家在研究点击反应砌块的过程中,发现了一种结构如图的化合物,X、Y、Z和W是原子序数依次增大的短周期元素,Y和W是同主族元素。下列说法错误的是
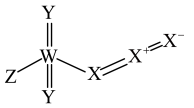
A.简单离子半径: | B.简单氢化物的沸点: |
C.最高价含氧酸的酸性: | D.Y与X、Y与W均能形成多种化合物 |
您最近一年使用:0次
2023-08-21更新
|
160次组卷
|
2卷引用:河南省郑州市十校2022-2023学年高一下学期期中联考化学试题
名校
解题方法
5 . 已知 的结构为
的结构为 ,下列叙述不正确的是
,下列叙述不正确的是
 的结构为
的结构为 ,下列叙述不正确的是
,下列叙述不正确的是A. 的结构中,两边的S原子无孤电子对 的结构中,两边的S原子无孤电子对 |
B. 的结构中,中间的两个S原子均有两对孤电子对 的结构中,中间的两个S原子均有两对孤电子对 |
C. 的结构中,a、b为键长,则a>b 的结构中,a、b为键长,则a>b |
D.沸点: < < |
您最近一年使用:0次
2023-08-05更新
|
169次组卷
|
2卷引用:河南省周口市项城市2022-2023学年高二下学期4月期中考试化学试题
名校
6 . 布洛芬具有抗炎、镇痛、解热的作用,但口服该药对肠道、胃有刺激性,解决方法之一是对该分子进行成酯修饰(如图所示)。下列说法正确的是


| A.电负性:N>C>O | B.R和T中均无手性碳原子 |
C.沸点: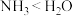 | D.R和T均不能与氧气发生氧化反应 |
您最近一年使用:0次
名校
7 . 下列说法中正确的是
A.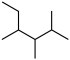 的名称为3,4-二甲基-2-乙基戊烷 的名称为3,4-二甲基-2-乙基戊烷 |
B. 、 、 的空间结构均为平面三角形 的空间结构均为平面三角形 |
| C.HF比HCl沸点高的原因是HF分子内存在氢键 |
D.键角: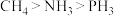 |
您最近一年使用:0次
名校
解题方法
8 . 铜及其化合物在工农业生产中有广泛的应用。
(1)向CuSO4溶液中加入过量NaOH溶液可生成Na2[Cu(OH)4]。Na2[Cu(OH)4]中除了配位键外,还存在的化学键类型有___________(填字母)。
(2)将CuO投入NH3、(NH4)2SO4的混合溶液中进行“氨浸”,控制温度为50℃至55℃,pH约为9.5,CuO转化为溶液。
①CuO被浸取的离子方程式为___________ 。
②[Cu(NH3)4]2+结构中,若用两个H2O分子代替两个NH3分子,可以得到两种不同结构的化合物,由此推测的[Cu(NH3)4]2+空间构型为___________ 。
(3)Cu2+可以与乙二胺(H2N-CH2-CH2-NH2) 形成配离子,结构如图所示:
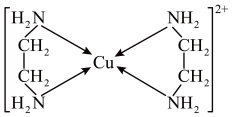
乙二胺分子中N原子成键时采取的VSEPR模型是___________ 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高很多,原因是___________ 。
(1)向CuSO4溶液中加入过量NaOH溶液可生成Na2[Cu(OH)4]。Na2[Cu(OH)4]中除了配位键外,还存在的化学键类型有___________(填字母)。
| A.离子键 | B.金属键 | C.极性共价键 | D.非极性共价键 |
①CuO被浸取的离子方程式为
②[Cu(NH3)4]2+结构中,若用两个H2O分子代替两个NH3分子,可以得到两种不同结构的化合物,由此推测的[Cu(NH3)4]2+空间构型为
(3)Cu2+可以与乙二胺(H2N-CH2-CH2-NH2) 形成配离子,结构如图所示:

乙二胺分子中N原子成键时采取的VSEPR模型是
您最近一年使用:0次
9 . 水是生命之源,水的状态除了气、液、固之外,还有玻璃态。玻璃态水是由液态水急速冷却到-108℃时形成的一种无定形状态,其密度与普通液态水的密度相同,有关玻璃态水的叙述正确的是
| A.玻璃态水中也存在范德华力与氢键 |
| B.玻璃态水是分子晶体 |
| C.玻璃态中水分子间距离比普通液态水中分子间距离大 |
D.玻璃态水中氧原子为 杂化 杂化 |
您最近一年使用:0次
2023-05-21更新
|
210次组卷
|
4卷引用:河南省商丘市二十校2023-2024学年高二下学期期中联考化学试卷
名校
解题方法
10 . 锂离子电池是现代高性能电池的代表,高性能的电极材料与物质结构密切相关。
(1)LiFePO4因具有良好的结构稳定性而成为新一代正极材料,这与PO 的结构密切相关,PO
的结构密切相关,PO 的立体构型为
的立体构型为____________ 。P、O、S的电负性从大到小的顺序为__________ 。
(2)通常在电极材料表面进行“碳”包覆处理以增强其导电性。抗坏血酸(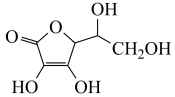 )常被用作碳包覆的碳源,其易溶于水的原因是
)常被用作碳包覆的碳源,其易溶于水的原因是_______________ ,抗坏血酸中碳原子的杂化方式为_______ ,1 mol抗坏血酸中手性碳原子的数目为_____ 。
(3)目前最常用的电极材料有锂钴复合氧化物和石墨。
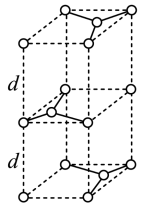
石墨晶胞(如图)层间距为d pm,C—C键长为a pm,石墨晶体的密度为ρ g·cm-3,列式表示阿伏加德罗常数为________ mol-1。
(1)LiFePO4因具有良好的结构稳定性而成为新一代正极材料,这与PO
 的结构密切相关,PO
的结构密切相关,PO 的立体构型为
的立体构型为(2)通常在电极材料表面进行“碳”包覆处理以增强其导电性。抗坏血酸(
 )常被用作碳包覆的碳源,其易溶于水的原因是
)常被用作碳包覆的碳源,其易溶于水的原因是(3)目前最常用的电极材料有锂钴复合氧化物和石墨。
石墨晶胞(如图)层间距为d pm,C—C键长为a pm,石墨晶体的密度为ρ g·cm-3,列式表示阿伏加德罗常数为

您最近一年使用:0次
2023-04-29更新
|
116次组卷
|
2卷引用:河南省实验中学2022-2023学年高二下学期期中考试化学试题



