名校
1 . 下列物质结构与性质或物质性质与用途具有对应关系的是
| A.键能:H-F>H-Cl,HF的沸点比HCl的高 |
B.乙酸中 使羟基的极性减小,乙酸的酸性比甲酸的弱 使羟基的极性减小,乙酸的酸性比甲酸的弱 |
| C.HClO具有弱酸性,可用于杀菌消毒 |
D. 能与NaOH溶液反应,可用作净水剂 能与NaOH溶液反应,可用作净水剂 |
您最近一年使用:0次
2 . 对金属材料中C、O、N、S的含量进行定性和定量分析,可以确定金属材料的等级。下列说法正确的是
| A.电离能大小:I1(N)>I1(O)>I1(S) | B.沸点高低:H2S>H2O>NH3 |
| C.酸性强弱:H2SO3>HNO3>H2CO3 | D.半径大小:r(S2-)>r(O2-)>r(N3-) |
您最近一年使用:0次
解题方法
3 .  与
与 可以形成
可以形成 和
和 两种化合物,其中
两种化合物,其中 的结构如图所示。
的结构如图所示。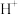 可与
可与 形成
形成 。下列说法正确的是
。下列说法正确的是
 与
与 可以形成
可以形成 和
和 两种化合物,其中
两种化合物,其中 的结构如图所示。
的结构如图所示。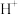 可与
可与 形成
形成 。下列说法正确的是
。下列说法正确的是
A. 分子中 分子中 原子采用 原子采用 杂化 杂化 |
B.相同条件下 在 在 中的溶解度大于在水中的溶解度 中的溶解度大于在水中的溶解度 |
C.液态水中的作用力由强到弱的顺序是:氢键 范德华力 范德华力 |
D. 的空间结构为三角锥形 的空间结构为三角锥形 |
您最近一年使用:0次
名校
4 .  可用于生产铵盐、硝酸等。
可用于生产铵盐、硝酸等。 与
与 都可用作火箭的燃料,下列物质结构与性质或物质性质与用途具有对应关系的是
都可用作火箭的燃料,下列物质结构与性质或物质性质与用途具有对应关系的是
 可用于生产铵盐、硝酸等。
可用于生产铵盐、硝酸等。 与
与 都可用作火箭的燃料,下列物质结构与性质或物质性质与用途具有对应关系的是
都可用作火箭的燃料,下列物质结构与性质或物质性质与用途具有对应关系的是A. 极易溶于水,液氨可用作制冷剂 极易溶于水,液氨可用作制冷剂 |
B. 具有还原性,可用作火箭的燃料 具有还原性,可用作火箭的燃料 |
C. 易分解,可用作化肥 易分解,可用作化肥 |
D. 共价键数目大于 共价键数目大于 , , 的热稳定性比 的热稳定性比 的高 的高 |
您最近一年使用:0次
名校
5 . 下列物质结构与性质或性质与用途不具有对应关系的是
| A.MgCl2易溶于水,可用于制作豆腐的凝固剂 |
| B.MgO是碱性氧化物,可用于吸收燃煤烟气中的SO2 |
| C.NaCl晶体中离子间存在较强的离子键,NaCl晶体的硬度较大 |
D. 通过氢键缔合成较大的酸根,NaHCO3的溶解度小于Na2CO3 通过氢键缔合成较大的酸根,NaHCO3的溶解度小于Na2CO3 |
您最近一年使用:0次
2024-06-03更新
|
366次组卷
|
3卷引用:江苏省南京市2024届高三下学期第二次模拟考试化学试题
6 . 硫元素约占地球总质量的1.9%,广泛分布并循环于地球内部各圈层。硫有32S、34S、33S和36S四种同位素。硫元素主要以氢化物、硫化物、含氧酸和含氧酸盐等形式存在。硫的单质有S2、S4、S8等多种分子形态;硫的氢化物(H2S、H2S2)均有弱酸性;低价硫易被氧气氧化。硫在生物圈的演化中扮演了重要角色,在细菌作用下硫元素可发生氧化或还原反应,促进了硫元素在地球各圈层中的循环。下列有关物质的性质与结构或物质性质与用途有对应关系的是
| A.SO2有氧化性,可用作葡萄酒的防腐剂 |
| B.S单质为淡黄色固体,可制备硫化橡胶 |
| C.H-O键键能大于H-S键键能,因此H2O的沸点比H2S的高 |
| D.浓硫酸具有吸水性,可以作气体干燥剂 |
您最近一年使用:0次
7 . 卤族元素单质及其化合物应用广泛。海洋是一个巨大的卤素资源宝库,从海水中能获得NaCl,NaCl的晶胞如下图所示。以NaCl为原料可制得Cl2、HClO、ClO2、 、
、 。工业常通过电解NaCl饱和溶液制备Cl2,Cl2氧化卤水中Br-可得到Br2.KClO3酸性溶液中加入H2C2O4可制得黄绿色气体ClO2,该气体常用作自来水消毒剂。F2能与熔融的Na2SO4反应生成硫酰氟(SO2F2)。标况下,氟化氢呈液态。
。工业常通过电解NaCl饱和溶液制备Cl2,Cl2氧化卤水中Br-可得到Br2.KClO3酸性溶液中加入H2C2O4可制得黄绿色气体ClO2,该气体常用作自来水消毒剂。F2能与熔融的Na2SO4反应生成硫酰氟(SO2F2)。标况下,氟化氢呈液态。
 、
、 。工业常通过电解NaCl饱和溶液制备Cl2,Cl2氧化卤水中Br-可得到Br2.KClO3酸性溶液中加入H2C2O4可制得黄绿色气体ClO2,该气体常用作自来水消毒剂。F2能与熔融的Na2SO4反应生成硫酰氟(SO2F2)。标况下,氟化氢呈液态。
。工业常通过电解NaCl饱和溶液制备Cl2,Cl2氧化卤水中Br-可得到Br2.KClO3酸性溶液中加入H2C2O4可制得黄绿色气体ClO2,该气体常用作自来水消毒剂。F2能与熔融的Na2SO4反应生成硫酰氟(SO2F2)。标况下,氟化氢呈液态。 
| A.HClO呈弱酸性,可用于漂白纸张 |
| B.ClO2具有强氧化性,可用于自来水杀菌消毒 |
C.Cl-有孤电子对,可与 形成 形成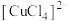 |
| D.HF分子间存在氢键,HF沸点较高 |
您最近一年使用:0次
解题方法
8 . 氯及其化合物应用广泛。 易液化,可储存于钢瓶中。氯气可用于生产
易液化,可储存于钢瓶中。氯气可用于生产 、
、 、
、 、
、 等化工产品。
等化工产品。 和
和 的化学性质相似,能与
的化学性质相似,能与 反应生成两种酸。
反应生成两种酸。 (其中
(其中 为
为 价)可用于漂白和杀菌消毒,其水解可生成
价)可用于漂白和杀菌消毒,其水解可生成 和
和 。下列物质的结构与性质或物质的性质与用途具有对应关系的是
。下列物质的结构与性质或物质的性质与用途具有对应关系的是
 易液化,可储存于钢瓶中。氯气可用于生产
易液化,可储存于钢瓶中。氯气可用于生产 、
、 、
、 、
、 等化工产品。
等化工产品。 和
和 的化学性质相似,能与
的化学性质相似,能与 反应生成两种酸。
反应生成两种酸。 (其中
(其中 为
为 价)可用于漂白和杀菌消毒,其水解可生成
价)可用于漂白和杀菌消毒,其水解可生成 和
和 。下列物质的结构与性质或物质的性质与用途具有对应关系的是
。下列物质的结构与性质或物质的性质与用途具有对应关系的是A. 的键能大于 的键能大于 , , 的热稳定性大于 的热稳定性大于 |
B. 分子间存在氢键, 分子间存在氢键, 不易分解 不易分解 |
C. 具有弱酸性,可用于杀菌消毒 具有弱酸性,可用于杀菌消毒 |
D. 溶液呈棕黄色,可用于蚀刻铜制印刷电路板 溶液呈棕黄色,可用于蚀刻铜制印刷电路板 |
您最近一年使用:0次
名校
9 . 短周期主族元素X、Y、Z、W、R的原子序数依次增加,X、Y、W位于不同周期,原子序数:3Y=Z+R,常温下,X与Y可组成两种液体二元化合物。某种缓冲溶液的主要成分结构如图。
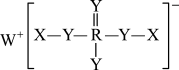
| A.简单氢化物的沸点:Y>Z |
| B.简单离子半径:Y>Z>W |
| C.W分别与X、Y组成的化合物均含离子键 |
D.电解WZ溶液可制得WYX、 |
您最近一年使用:0次
名校
10 . PtNiFe—LDHGO催化甲醛氧化的反应机理如图:
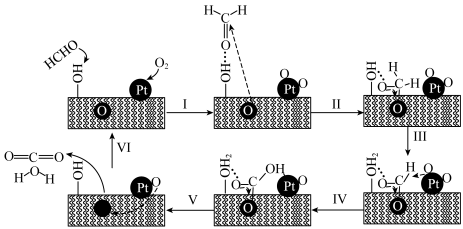
A.步骤Ⅰ中甲醛通过氢键吸附在催化剂表面的 上 上 |
| B.上述反应机理涉及极性键和非极性键的形成 |
C.该反应每生成1 mol ,转移电子的数目约为 ,转移电子的数目约为 |
| D.PtNiFe—LDHGO降低了该反应的活化能 |
您最近一年使用:0次



