解题方法
1 . 下列有关物质性质差异的解释不合理的是
| 选项 | 性质差异 | 解释 |
| A | 硬度:金刚石>晶体硅 | 键能: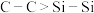 |
| B | 熔点:石墨> | 石墨是共价晶体, 是分子晶体 是分子晶体 |
| C | 沸点: |  分子间存在氢键 分子间存在氢键 |
| D | 酸性: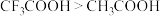 | 电负性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 前20号主族元素X、Y、Z、W的原子序数依次增大,它们的原子序数之和等于49.Y的某种氢化物遇浓盐酸有白烟生成,基态 原子的
原子的 轨道上有2个未成对电子,基态
轨道上有2个未成对电子,基态 原子的最外层电子数和最内层电子数相等。下列叙述正确的是
原子的最外层电子数和最内层电子数相等。下列叙述正确的是
 原子的
原子的 轨道上有2个未成对电子,基态
轨道上有2个未成对电子,基态 原子的最外层电子数和最内层电子数相等。下列叙述正确的是
原子的最外层电子数和最内层电子数相等。下列叙述正确的是A. 和 和 的最高价含氧酸均为强酸 的最高价含氧酸均为强酸 | B.简单氢化物的沸点: |
| C.X、Z可形成非极性分子 | D. 为只含离子键的离子晶体 为只含离子键的离子晶体 |
您最近一年使用:0次
解题方法
3 . 碳酸氢钠溶液中碳酸氢根离子以氢键相连成二聚离子,其结构如图所示。
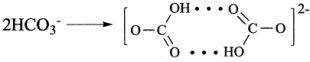
A.键能: | B. 的空间结构:平面三角形 的空间结构:平面三角形 |
C.溶解度: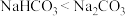 | D. 形成 形成 发生了化学反应 发生了化学反应 |
您最近一年使用:0次
2024-05-17更新
|
108次组卷
|
2卷引用:2024届贵州省遵义市高三下学期三模化学试题
名校
4 . 实验室用电石(主要成分为CaC2)与水反应制备的C2H2中混有H2S,可用CuSO4溶液净化,反应的化学方程式为H2S+CuSO4=CuS↓+H2SO4。下列说法正确的是
A.H2S的VSEPR模型为 |
| B.1molC2H2中σ键和π键的个数比为1∶1 |
| C.H2S是由极性键构成的极性分子 |
| D.H2S可溶于水是因为与H2O形成分子间氢键 |
您最近一年使用:0次
5 . 某人体内可合成的重要化合物结构如图,W、X、Y、Z、Q是原子序数依次增大的短周期主族元素。下列叙述错误的是
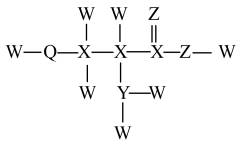
A.第一电离能: | B.物质沸点: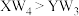 |
C.共价键键角: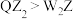 | D.基态Y、Z原子的未成对电子数之比为3:2 |
您最近一年使用:0次
解题方法
6 . 四种短周期主族元素X、Y、Z、W原子序数依次增大,X的最高正化合价和最低负化合价的代数和为0,Y和W的最外层电子数相同,Z元素的焰色试验呈黄色,四种元素的最外层电子数之和为17。下列说法错误的是
A.原子半径: |
B.最高价氧化物对应的水化物的酸性: |
C.简单氢化物的沸点: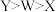 |
| D.由X、Y两种元素组成的化合物一定是极性分子 |
您最近一年使用:0次
名校
解题方法
7 . 下列说法错误的是
| A.MgO的离子键的键能大于CaO的 | B.BF3键角为120°,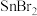 的键角大于120° 的键角大于120° |
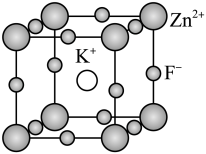
C.如图所示的晶胞的化学式为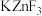 | D.DNA双螺旋的两个螺旋链通过氢键相互结合 |
您最近一年使用:0次
名校
8 . 下列有关说法正确的是
| A.某晶体溶于水后可以导电,该晶体一定是离子晶体 |
B.干冰和 的晶体类型相同 的晶体类型相同 |
| C.分子晶体的结构特征都是分子密堆积,一个分子周围有12个紧邻的分子 |
| D.标准状况下HF不是气体的原因是HF分子间可以形成分子间氢键,沸点较高 |
您最近一年使用:0次
名校
9 . 下列说法中正确的有
①由原子构成的晶体不一定是共价晶体
②水结成冰密度减小与水分子之间能形成氢键有关
③HF、HCl、HBr、HI的热稳定性和还原性依次减弱
④共价键的强弱决定分子晶体熔、沸点的高低
⑤ 、
、 、
、 的热稳定性依次减弱,熔沸点依次升高
的热稳定性依次减弱,熔沸点依次升高
⑥硬度由大到小:金刚石>碳化硅>晶体硅
①由原子构成的晶体不一定是共价晶体
②水结成冰密度减小与水分子之间能形成氢键有关
③HF、HCl、HBr、HI的热稳定性和还原性依次减弱
④共价键的强弱决定分子晶体熔、沸点的高低
⑤
 、
、 、
、 的热稳定性依次减弱,熔沸点依次升高
的热稳定性依次减弱,熔沸点依次升高⑥硬度由大到小:金刚石>碳化硅>晶体硅
| A.②③④⑥ | B.①②③⑥ | C.①②④⑤ | D.①②⑤⑥ |
您最近一年使用:0次
2024-04-25更新
|
272次组卷
|
4卷引用:贵州省安龙县第一中学2023-2024学年高二下学期第一次阶段考试化学试题
名校
解题方法
10 . 下列有关说法中正确的是
A.如图所示,HCl分子由H原子的1s轨道和Cl原子的3p轨道重叠形成 |
| B.ZnCO3入药可用于治疗皮肤炎症,ZnCO3中阴离子空间结构为四面体形 |
| C.基态As原子的电子排布式和价电子排布式分别为[Ar]3d104s24p3和4s24p3 |
| D.对羟基苯甲酸存在分子内氢键,是其沸点比邻羟基苯甲酸的高的主要原因 |
您最近一年使用:0次



