1 . Wolff-Kishner-黄鸣龙还原反应机理如下( 均代表烃基),下列有关说法不正确的是
均代表烃基),下列有关说法不正确的是
 均代表烃基),下列有关说法不正确的是
均代表烃基),下列有关说法不正确的是
| A.肼的沸点高于氨气,原因是分子间氢键数目更多,且相对分子质量更大 |
| B.过程①发生加成反应,过程②发生消去反应 |
C.增大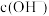 ,可以使过程③反应速率增大,促进平衡正向移动 ,可以使过程③反应速率增大,促进平衡正向移动 |
D.应用该机理, 可以在碱性条件下转变为 可以在碱性条件下转变为 |
您最近一年使用:0次
名校
2 . 乙醛主要用作还原剂、杀菌剂、合成橡胶等,以乙烷为原料合成乙醛的反应机理如图所示。下列说法正确的是
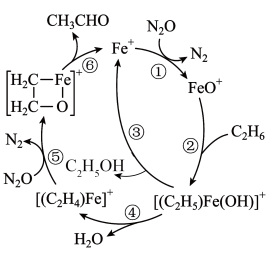
A.反应①中消耗的氧化剂与还原剂的物质的量之比为 |
B.理论上该合成方法中每消耗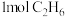 可得到 可得到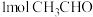 |
C.反应⑤、⑥中均有含 键的产物生成 键的产物生成 |
D.乙醛分子中没有 键,故其与水分子间不能形成氢键 键,故其与水分子间不能形成氢键 |
您最近一年使用:0次
2024-06-05更新
|
169次组卷
|
2卷引用:2024届东三省高三下学期5月份大联考化学试题
3 . 向 溶液中通入
溶液中通入 ,反应的离子方程式为
,反应的离子方程式为
 。下列说法错误的是
。下列说法错误的是
 溶液中通入
溶液中通入 ,反应的离子方程式为
,反应的离子方程式为
 。下列说法错误的是
。下列说法错误的是A.电负性: | B. 中碳原子的杂化方式为 中碳原子的杂化方式为 |
C. 的空间结构为 的空间结构为 形 形 | D. 可以与 可以与 分子形成氢键 分子形成氢键 |
您最近一年使用:0次
2024高三·全国·专题练习
4 . 工业合成氨常选择反应:N2+3H2 2NH3,设NA为阿伏加德罗常数的值,下列说法正确的是
2NH3,设NA为阿伏加德罗常数的值,下列说法正确的是
 2NH3,设NA为阿伏加德罗常数的值,下列说法正确的是
2NH3,设NA为阿伏加德罗常数的值,下列说法正确的是| A.28 g N2完全反应,转移的电子数为3NA |
| B.混合气中物质的沸点:NH3>N2>H2 |
| C.在一定温度的固定容器中进行反应,通入氦气,能提高氢气的转化率 |
| D.反应物断裂NA个σ键的同时生成物断裂NA个σ键,反应达到平衡状态 |
您最近一年使用:0次
2024高三·全国·专题练习
解题方法
5 . 下列表述错误的是
| A.干冰和金刚石的晶体类型不同 |
| B.简单氢化物的沸点:H2O>SiH4>CH4 |
C.CO 、HCN中碳原子的杂化方式相同 、HCN中碳原子的杂化方式相同 |
| D.HCl比Cl2易溶于水可用“相似相溶”原理解释 |
您最近一年使用:0次
2024高三·全国·专题练习
解题方法
6 . 乙醛常用于有机合成,可由乙醇氧化得到。乙醇催化氧化制取乙醛的反应如下:2CH3CH2OH+O2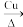 2CH3CHO+2H2O。下列说法正确的是
2CH3CHO+2H2O。下列说法正确的是
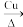 2CH3CHO+2H2O。下列说法正确的是
2CH3CHO+2H2O。下列说法正确的是| A.CH3CH2OH的沸点高于CH3OCH3 |
| B.基态Cu的核外电子排布式为[Ar]3d94s2 |
| C.1molCH3CHO中所含σ键的数目为5NA |
| D.H2O分子的空间结构为直线形 |
您最近一年使用:0次
2024高三·全国·专题练习
解题方法
7 . 探究影响H2O2分解速率的影响因素,实验方案如图所示。
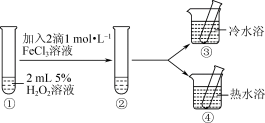
| A.热水浴的温度越高,其对比实验现象越明显 |
| B.H2O2易溶于水,主要是由于H2O2与H2O分子之间能形成氢键 |
| C.对比①②,可探究FeCl3溶液对H2O2分解速率的影响 |
| D.对比②③④,可探究温度对H2O2分解速率的影响 |
您最近一年使用:0次
2024高三·全国·专题练习
解题方法
8 . 科学家探测用Pt0.2Pd1.8Ge催化O2和H2制备双氧水和水的过程如图所示。下列说法错误的是

| A.等物质的量的H2O和H2O2的中子数之比为1∶2 |
| B.制备等物质的量的H2O2和H2O时转移电子数之比为1∶1 |
| C.沸点:H2O2<H2S2 |
| D.上述合成H2O2过程中存在非极性键的断裂和极性键、非极性键的形成 |
您最近一年使用:0次
2024高三·全国·专题练习
9 . 对下列事实的解释错误的是
| 选项 | 事实 | 解释 |
| A | 稳定性:HF>HI | HF分子间存在氢键,HI分子间不存在氢键 |
| B | 键角:NH >H2O >H2O | 中心原子均采取sp3杂化,孤电子对有较大的斥力 |
| C | 熔点:SiO2>SO2 | SiO2是共价晶体,SO2是分子晶体;共价键比分子间作用力强 |
| D | 酸性:CF3COOH>CCl3COOH | F的电负性大于Cl,F-C的极性大于Cl-C,使F3C-的极性大于Cl3C-的极性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 下列物质的性质或数据与氢键无关的是
| A.氨气很容易液化 |
B.邻羟基苯甲酸(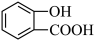 )的熔点为 )的熔点为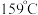 ,对羟基苯甲酸( ,对羟基苯甲酸(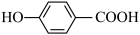 )的熔点为 )的熔点为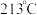 |
| C.乙醚微溶于水,而乙醇可与水以任意比互溶 |
D. 分解时吸收的热量比 分解时吸收的热量比 分解时吸收的热量多 分解时吸收的热量多 |
您最近一年使用:0次
2024-05-01更新
|
158次组卷
|
2卷引用:天津市南开中学2023-2024学年高二下学期期中考试化学试卷



