1 . 铁及其化合物有着广泛的用途,氧化铁可用作颜料,氮化铁用于硬磁和软磁性材料、信息记录材料、磁性密封液等。
(1)氮化铁晶体的晶胞结构如图所示。该晶体中铁、氮的微粒个数之比为_______ 。

(2)氧化亚铁晶体的晶胞如图所示。氧化亚铁晶胞中,与Fe2+紧邻且等距离的Fe2+数目为_____ 。

(1)氮化铁晶体的晶胞结构如图所示。该晶体中铁、氮的微粒个数之比为

(2)氧化亚铁晶体的晶胞如图所示。氧化亚铁晶胞中,与Fe2+紧邻且等距离的Fe2+数目为

您最近一年使用:0次
名校
2 . 氯化铵是“侯氏制碱法”的副产品,在工农业生产中具有重要用途。回答下列问题:
(1)氯化铵的立方晶胞结构如图所示:

①与 等距离且最近的Cl-有
等距离且最近的Cl-有_______ 个。
②若氯化铵的密度为 ,设
,设 为阿伏加德罗常数的值,则晶胞参数a=
为阿伏加德罗常数的值,则晶胞参数a=_______ nm(用含d、 的代数式表示)。
的代数式表示)。
(2)常温下,用 计测得某
计测得某 溶液的
溶液的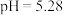 。
。
①用离子方程式表示 溶液呈酸性的原因:
溶液呈酸性的原因:____________ 。
②若溶液中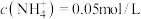 ,则水解常数
,则水解常数
_______ (提示: 和
和 的物质的量浓度几乎相等,
的物质的量浓度几乎相等,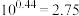 。结果保留2位有效数字)。
。结果保留2位有效数字)。
(3)为探究溶液浓度和 浓度对氯化铵水解的影响,学习小组利用
浓度对氯化铵水解的影响,学习小组利用 溶液和
溶液和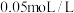 的
的 溶液,按下表配制总体积相同的系列溶液。测定
溶液,按下表配制总体积相同的系列溶液。测定 ,记录数据。
,记录数据。
①补充表中数据:a=_______ 。
②由实验I和II可知,稀释 溶液,
溶液,_______ (填“促进"或“抑制”) 水解,结合表中数据,给出判断理由:
水解,结合表中数据,给出判断理由:_______
③结合表中数据分析 增大,
增大, 水解程度
水解程度_______ (填“增大”、“减小”或“不变”)。
④画出稀释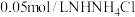 溶液时,
溶液时, 随加入水量的变化曲线图
随加入水量的变化曲线图_______ ,标注出 的变化范围。
的变化范围。
(1)氯化铵的立方晶胞结构如图所示:

①与
 等距离且最近的Cl-有
等距离且最近的Cl-有②若氯化铵的密度为
 ,设
,设 为阿伏加德罗常数的值,则晶胞参数a=
为阿伏加德罗常数的值,则晶胞参数a= 的代数式表示)。
的代数式表示)。(2)常温下,用
 计测得某
计测得某 溶液的
溶液的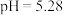 。
。①用离子方程式表示
 溶液呈酸性的原因:
溶液呈酸性的原因:②若溶液中
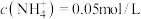 ,则水解常数
,则水解常数
 和
和 的物质的量浓度几乎相等,
的物质的量浓度几乎相等,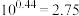 。结果保留2位有效数字)。
。结果保留2位有效数字)。(3)为探究溶液浓度和
 浓度对氯化铵水解的影响,学习小组利用
浓度对氯化铵水解的影响,学习小组利用 溶液和
溶液和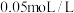 的
的 溶液,按下表配制总体积相同的系列溶液。测定
溶液,按下表配制总体积相同的系列溶液。测定 ,记录数据。
,记录数据。| 序号 | 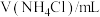 |  | 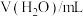 |  |
| I | 20 | 0 | 0 | 5.28 |
| II | 2 | 0 | 18 | 5.78 |
| III | 2 | a | 16 | 5.78 |
| IV | 2 | 10 | 8 | 5.78 |
②由实验I和II可知,稀释
 溶液,
溶液, 水解,结合表中数据,给出判断理由:
水解,结合表中数据,给出判断理由:③结合表中数据分析
 增大,
增大, 水解程度
水解程度④画出稀释
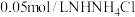 溶液时,
溶液时, 随加入水量的变化曲线图
随加入水量的变化曲线图 的变化范围。
的变化范围。
您最近一年使用:0次
2022-08-05更新
|
225次组卷
|
2卷引用:广东省2023届高三上学期开学联考化学试题
3 . 2022年北京冬季奥运会场馆建设使用了大量不锈钢材质,不锈钢属于铁碳合金,常含铬 、镍
、镍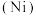 等元素。回答下列问题:
等元素。回答下列问题:
(1)碳的价电子排布式为_______ 碳的一种单质石墨是单层二维蜂窝状晶格结构的新材料(如图1),其中碳原子采取_______ 杂化,在层中碳原子的配位数为_______ 。

(2)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图2所示。晶体中每个镁原子周围距离最近的铁原子有_______ 个,该铁镁合金中原子个数比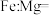
_______ ;原子坐标参数可以表示晶胞内部各原子的相对位置,其中原子坐标参数A为 ,C为
,C为 ,B点坐标参数为
,B点坐标参数为_______ 。

(3)金属铬晶胞如图3,已知其密度为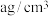 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶体中铬原子的半径为
,则晶体中铬原子的半径为_______ cm(用含 的表达式表示)。
的表达式表示)。
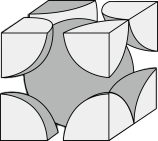
图3
 、镍
、镍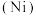 等元素。回答下列问题:
等元素。回答下列问题:(1)碳的价电子排布式为

(2)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图2所示。晶体中每个镁原子周围距离最近的铁原子有
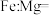
 ,C为
,C为 ,B点坐标参数为
,B点坐标参数为
(3)金属铬晶胞如图3,已知其密度为
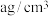 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶体中铬原子的半径为
,则晶体中铬原子的半径为 的表达式表示)。
的表达式表示)。
图3
您最近一年使用:0次
2022高三·全国·专题练习
4 . 氨、磷、铁、钴等元素的化合物在现代农业、科技、国防建设中有着许多独特的用途。Co可以形成六方晶系的CoO(OH),晶胞结构如图2所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子坐标。已知晶胞含对称中心,其中1号O原子的坐标为(0.6667,0.3333,0.1077),则2号O原子的坐标为_______ 。设NA为阿伏加德罗常数的值,该晶体的密度为_______ g/cm3(用代数式表示)。


您最近一年使用:0次
名校
解题方法
5 . N、P、As及其化合物在生产生活方面都有重要的用途。回答下列问题:
(1)As原子的基态核外电子排布式为___________ 。
(2)Pt(NH3)2Cl2有如图所示两种结构,Pt2+的配位体是___________ 。顺铂在水中溶解度较大,反铂在水中溶解度小,顺铂在水中溶解度较大的原因是___________ 。
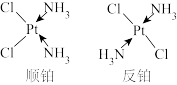
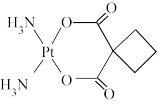
(3)碳铂是一种广谱抗癌药物,其结构如图。其分子中碳原子轨道杂化类型为___________ 。
(4)PCl3和BCl3混合与H2在1000℃条件下可得到一种半导体材料,其晶胞结构如图所示。BCl3的空间构型为___________ (用文字描述),该反应的化学方程式为___________ 。

(1)As原子的基态核外电子排布式为
(2)Pt(NH3)2Cl2有如图所示两种结构,Pt2+的配位体是
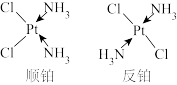
(3)碳铂是一种广谱抗癌药物,其结构如图。其分子中碳原子轨道杂化类型为

(4)PCl3和BCl3混合与H2在1000℃条件下可得到一种半导体材料,其晶胞结构如图所示。BCl3的空间构型为

您最近一年使用:0次
6 . 氮元素及其化合物在生产、生活中用途广泛。回答下列问题:
(1)基态氮原子的价电子排布式为___________ 。
(2)与N同周期的元素中第一电离能比N大的元素有____________ 种。
(3)三硝基胺N(NO2)3(其结构为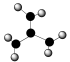 )是一种新型的火箭燃料,因硝基吸电子能力强,中心N原子上无孤电子对,则中心N原子的杂化方式为
)是一种新型的火箭燃料,因硝基吸电子能力强,中心N原子上无孤电子对,则中心N原子的杂化方式为___________ ,并且与三个硝基中的N构成___________ 形。
(4)(CN)2、(SCN)2的性质与卤素单质的相似,称为拟卤素。其分子内各原子均达到8电子稳定结构,则1mol(CN)2分子中含___________ molπ键,SCN-的空间构型为___________ 形。
(5)白磷在氯气中燃烧可以得到PCl3和PCl5,研究发现固态PCl4和PBr5均为离子晶体,但其结构分别为[PCl4]+[PCl6]-和[PBr4]+Br-,分析PCl5和PBr5结构存在差异的原因:___________ 。
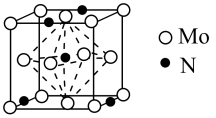
(6)过渡金属氮化物因其优异的催化性能(加氢处理、光和电化学催化等)受到了广泛关注。贵金属钼(Mo)的氮化物可作将N2还原为氨的反应的催化剂。贵金属钼的氮化物的立方晶胞如图所示。已知晶胞参数为anm,则该晶体的化学式为___________ ,晶体的密度为___________ (列出计算式)g·cm-3。
(1)基态氮原子的价电子排布式为
(2)与N同周期的元素中第一电离能比N大的元素有
(3)三硝基胺N(NO2)3(其结构为
 )是一种新型的火箭燃料,因硝基吸电子能力强,中心N原子上无孤电子对,则中心N原子的杂化方式为
)是一种新型的火箭燃料,因硝基吸电子能力强,中心N原子上无孤电子对,则中心N原子的杂化方式为(4)(CN)2、(SCN)2的性质与卤素单质的相似,称为拟卤素。其分子内各原子均达到8电子稳定结构,则1mol(CN)2分子中含
(5)白磷在氯气中燃烧可以得到PCl3和PCl5,研究发现固态PCl4和PBr5均为离子晶体,但其结构分别为[PCl4]+[PCl6]-和[PBr4]+Br-,分析PCl5和PBr5结构存在差异的原因:
(6)过渡金属氮化物因其优异的催化性能(加氢处理、光和电化学催化等)受到了广泛关注。贵金属钼(Mo)的氮化物可作将N2还原为氨的反应的催化剂。贵金属钼的氮化物的立方晶胞如图所示。已知晶胞参数为anm,则该晶体的化学式为

您最近一年使用:0次
2021-12-20更新
|
624次组卷
|
4卷引用:解密13 物质结构与性质(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)
(已下线)解密13 物质结构与性质(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)回归教材重难点11 物质结构与性质-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)回归教材重难点11 物质结构与性质(选考)-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)山东省2021-2022学年上学期高三12月备考监测第二次联合考试化学试题
2021高三·全国·专题练习
7 . ZnGeP2和KTiOPO4都是非线性光学晶体材料,在激光技术方面有广泛用途。回答下列问题:
以Zn为顶点的ZnGeP2晶胞结构如图所示。
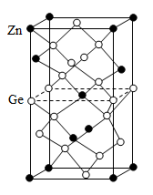
①Zn的配位数为___________ 。
②以Ge为顶点的晶胞中,Zn原子位于___________ 。
以Zn为顶点的ZnGeP2晶胞结构如图所示。

①Zn的配位数为
②以Ge为顶点的晶胞中,Zn原子位于
您最近一年使用:0次
名校
8 . 含氮、磷化合物在生活和生产中有许多重要用途,如:(CH3)3N、磷化硼(BP)、磷青铜(Cu3SnP)等。
回答下列问题:
(1)锡(Sn)是第五周期ⅣA元素。基态锡原子的价电子排布式为_________ ,据此推测,锡的最高正价是_________ 。
(2)与P同周期的主族元素中,电负性比P小的元素有____ 种 ,第一电离能比P大有____ 种。
(3)PH3分子的空间构型为___________ 。PH3的键角小于NH3的原因是__________ 。
(4)化合物(CH3)3N能溶于水,试解析其原因____________ 。
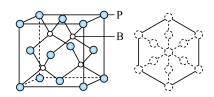
(5)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。磷化硼晶体晶胞如图所示:
①在一个晶胞中磷原子空间堆积方式为________ ,磷原子的配位数为________ 。
②已知晶胞边长a pm,阿伏伽德罗常数为NA。则磷化硼晶体的密度为______ g/cm3。
③磷化硼晶胞沿着体对角线方向的投影如图,请将表示B原子的圆圈涂黑________ 。
回答下列问题:
(1)锡(Sn)是第五周期ⅣA元素。基态锡原子的价电子排布式为
(2)与P同周期的主族元素中,电负性比P小的元素有
(3)PH3分子的空间构型为
(4)化合物(CH3)3N能溶于水,试解析其原因

(5)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。磷化硼晶体晶胞如图所示:
①在一个晶胞中磷原子空间堆积方式为
②已知晶胞边长a pm,阿伏伽德罗常数为NA。则磷化硼晶体的密度为
③磷化硼晶胞沿着体对角线方向的投影如图,请将表示B原子的圆圈涂黑
您最近一年使用:0次
2019-02-13更新
|
2517次组卷
|
8卷引用:河南省驻马店市新蔡县第一高级中学2021-2022学年高二下学期7月份月考化学试题
河南省驻马店市新蔡县第一高级中学2021-2022学年高二下学期7月份月考化学试题【市级联考】四川省攀枝花市2019届高三上学期第二次统考化学试题【市级联考】山东省泰安市2019届高三下学期二轮模拟考试理科综合化学试题江西省上饶市2020届第一次高考模拟考试理科综合化学试题解题达人.化学选择题(2021全国卷)精编特训06(已下线)2021年高考全国甲卷化学试题变式题2020年全国卷Ⅰ理综化学高考真题变式题(已下线)2020年海南卷化学高考真题变式题15-19
名校
9 . 据报道,科研人员应用计算机模拟出结构类似C60的物质N60,已知N60分子中每个氮原子均以N—N键结合三个N原子而形成8电子稳定结构。已知N—N键键能为159 kJ·mol-1,试回答下列问题:
(1)根据上述信息推测N60的结构特点:________________ 。
(2)1 mol N60分解成N2时吸收或放出的热量是____ kJ。(已知N≡N的键能为946 kJ·mol-1)
(3)由(2)列举N60的一些用途:______________________________________ 。
(4)若N60分子中只含x个五边形和y个六边形,则x=________ ,y=____________ 。(已知:多面体中,棱边数=顶点数+面数-2)
(5)∠NNN=________ 。
(1)根据上述信息推测N60的结构特点:
(2)1 mol N60分解成N2时吸收或放出的热量是
(3)由(2)列举N60的一些用途:
(4)若N60分子中只含x个五边形和y个六边形,则x=
(5)∠NNN=
您最近一年使用:0次
2018-12-27更新
|
157次组卷
|
2卷引用:云南省宁蒗彝族自治县第一中学2021-2022学年高二下学期3月考试化学试题



