1 . 从废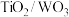 纳米薄膜中回收钛和钨等稀缺金属,既有利于资源综合利用,又避免污染环境。回收的工艺流程如下:
纳米薄膜中回收钛和钨等稀缺金属,既有利于资源综合利用,又避免污染环境。回收的工艺流程如下:

已知:
Ⅰ.乙胺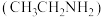 是无色极易挥发的液体,呈碱性,能与酸发生反应:
是无色极易挥发的液体,呈碱性,能与酸发生反应: 。
。
Ⅱ.酸性条件下,乙胺萃取 的反应为
的反应为 。
。
Ⅲ. 易溶于水,属于强电解质。偏钛酸难溶于水,其化学式可表示为
易溶于水,属于强电解质。偏钛酸难溶于水,其化学式可表示为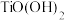 或
或 ,室温时
,室温时 。
。
回答下列问题:
(1)“碱浸”时发生反应的化学方程式为___________ 。“萃取”前,需要将“滤液I”的 调整到3.5左右,目的是
调整到3.5左右,目的是___________ 。
(2)试剂a为________ (写名称)。“反萃取”过程中发生反应的化学方程式为___________ 。
(3)检验“过滤Ⅱ”所得 已洗涤干净的方法是
已洗涤干净的方法是___________ 。
(4)室温下测得“滤液Ⅲ”的 ,则此时“滤液Ⅲ”中
,则此时“滤液Ⅲ”中
___________  。
。
(5) 与
与 同周期,
同周期, 、
、 、
、 可形成一种具有特殊导电性的晶体(化学式为
可形成一种具有特殊导电性的晶体(化学式为 ,
, 、
、 为整数),其立方晶胞如图所示,
为整数),其立方晶胞如图所示, 与
与 最小间距大于
最小间距大于 与
与 最小间距。
最小间距。

该晶体中,1个 周围与其最近的
周围与其最近的 的个数为
的个数为___________ 。
②若 与
与 最小间距为
最小间距为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该晶体的密度为
,则该晶体的密度为___________  (列出计算式)。
(列出计算式)。
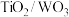 纳米薄膜中回收钛和钨等稀缺金属,既有利于资源综合利用,又避免污染环境。回收的工艺流程如下:
纳米薄膜中回收钛和钨等稀缺金属,既有利于资源综合利用,又避免污染环境。回收的工艺流程如下:
已知:
Ⅰ.乙胺
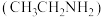 是无色极易挥发的液体,呈碱性,能与酸发生反应:
是无色极易挥发的液体,呈碱性,能与酸发生反应: 。
。Ⅱ.酸性条件下,乙胺萃取
 的反应为
的反应为 。
。Ⅲ.
 易溶于水,属于强电解质。偏钛酸难溶于水,其化学式可表示为
易溶于水,属于强电解质。偏钛酸难溶于水,其化学式可表示为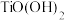 或
或 ,室温时
,室温时 。
。回答下列问题:
(1)“碱浸”时发生反应的化学方程式为
 调整到3.5左右,目的是
调整到3.5左右,目的是(2)试剂a为
(3)检验“过滤Ⅱ”所得
 已洗涤干净的方法是
已洗涤干净的方法是(4)室温下测得“滤液Ⅲ”的
 ,则此时“滤液Ⅲ”中
,则此时“滤液Ⅲ”中
 。
。(5)
 与
与 同周期,
同周期, 、
、 、
、 可形成一种具有特殊导电性的晶体(化学式为
可形成一种具有特殊导电性的晶体(化学式为 ,
, 、
、 为整数),其立方晶胞如图所示,
为整数),其立方晶胞如图所示, 与
与 最小间距大于
最小间距大于 与
与 最小间距。
最小间距。
该晶体中,1个
 周围与其最近的
周围与其最近的 的个数为
的个数为②若
 与
与 最小间距为
最小间距为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
2 . 钼酸铋作为新型半导体光催化材料,广泛应用于生产生活中。以氧化铋渣(主要成分是Bi2O3、Sb2O3、还含有Fe2O3、ZnO、Ag2O和SiO2等杂质)为原料制备钼酸铋(Bi2MoO6,其中Mo为+6价)的工艺流程如下:

回答下列问题:
(1)基态S的价电子排布式为___________ 。
(2)“浸渣”的主要成分为___________ (填化学式)。
(3)①“除锑”过程中发生反应的化学方程式为___________ ;
②该过程需要加热的原因为___________ 。
(4)已知:硫代乙酰胺(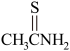 )在酸性溶液中会水解为乙酰胺(
)在酸性溶液中会水解为乙酰胺(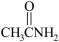 )和硫化氢;H2S的Ka1=1.0×10-7,Ka2=1.0×10-13;Ksp(Bi2S3)=2.0×10-99。
)和硫化氢;H2S的Ka1=1.0×10-7,Ka2=1.0×10-13;Ksp(Bi2S3)=2.0×10-99。
①硫化氢会进一步发生反应2Bi3+(aq)+3HS-(aq)=Bi2S3(s)+3H+(aq),此时溶液中c(HS-):c(S2-)=________ 。
②H2S常温下为气体,而H2O常温下为液体的原因为___________ 。
(5)“酸溶”时会有NO逸出,此过程中氧化剂与还原剂的物质的量之比为___________ 。
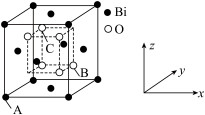
(6)Bi2O3的立方晶胞结构如图所示(O占据部分Bi的四面体空隙),以A点为原点建立分数坐标,已知A点坐标为(0,0,0),B点坐标为( ,
, ,
, ),则C点坐标为
),则C点坐标为___________ 。晶胞边长为anm,则密度为___________ g·cm-3(Bi2O3的摩尔质量为Mr,阿伏加德罗常数为NA)

回答下列问题:
(1)基态S的价电子排布式为
(2)“浸渣”的主要成分为
(3)①“除锑”过程中发生反应的化学方程式为
②该过程需要加热的原因为
(4)已知:硫代乙酰胺(
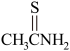 )在酸性溶液中会水解为乙酰胺(
)在酸性溶液中会水解为乙酰胺(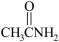 )和硫化氢;H2S的Ka1=1.0×10-7,Ka2=1.0×10-13;Ksp(Bi2S3)=2.0×10-99。
)和硫化氢;H2S的Ka1=1.0×10-7,Ka2=1.0×10-13;Ksp(Bi2S3)=2.0×10-99。①硫化氢会进一步发生反应2Bi3+(aq)+3HS-(aq)=Bi2S3(s)+3H+(aq),此时溶液中c(HS-):c(S2-)=
②H2S常温下为气体,而H2O常温下为液体的原因为
(5)“酸溶”时会有NO逸出,此过程中氧化剂与还原剂的物质的量之比为
(6)Bi2O3的立方晶胞结构如图所示(O占据部分Bi的四面体空隙),以A点为原点建立分数坐标,已知A点坐标为(0,0,0),B点坐标为(
 ,
, ,
, ),则C点坐标为
),则C点坐标为
您最近一年使用:0次
3 . 锰在冶金工业、电子工业、电池工业、农业生产等方面都有广泛应用,某软锰矿的主要成分为 、
、 、CaO)和少量的MgO、CuO,一种利用废铁屑还原浸出该软锰矿并制取金属锰的工艺流程如图所示:
、CaO)和少量的MgO、CuO,一种利用废铁屑还原浸出该软锰矿并制取金属锰的工艺流程如图所示:

已知: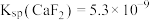 ,
,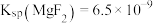 。
。
回答下列问题:
(1)废铁屑表面含有油脂,在使用前需进行处理,方法是_______ 。
(2)写出“浸出”时Fe与 反应的离子方程式:
反应的离子方程式:_______ 。
(3)“除铁”时加入 的主要作用是
的主要作用是_______ ;滤渣A的主要成分为_______ (填化学式)。
(4) “除钙镁”时,当钙离子和镁离子沉淀完全时,溶液中
_______ 。
(5)电解硫酸锰溶液(阳极为惰性电极,阴极为不锈钢合金)的装置示意图如图所示。

电解时Mn在_______ (填“阴”或“阳”)极析出,阳极的电极反应式为_______ ,阳极室的溶液可返回上述“_______ ”工序循环利用。
(6)一种锰的硅化物的晶胞结构( )如图所示:
)如图所示:

①基态Mn原子的核外电子排布式为_______ 。
②该锰的硅化物的化学式为_______ 。
 、
、 、CaO)和少量的MgO、CuO,一种利用废铁屑还原浸出该软锰矿并制取金属锰的工艺流程如图所示:
、CaO)和少量的MgO、CuO,一种利用废铁屑还原浸出该软锰矿并制取金属锰的工艺流程如图所示:
已知:
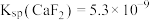 ,
,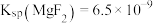 。
。回答下列问题:
(1)废铁屑表面含有油脂,在使用前需进行处理,方法是
(2)写出“浸出”时Fe与
 反应的离子方程式:
反应的离子方程式:(3)“除铁”时加入
 的主要作用是
的主要作用是(4) “除钙镁”时,当钙离子和镁离子沉淀完全时,溶液中

(5)电解硫酸锰溶液(阳极为惰性电极,阴极为不锈钢合金)的装置示意图如图所示。

电解时Mn在
(6)一种锰的硅化物的晶胞结构(
 )如图所示:
)如图所示:
①基态Mn原子的核外电子排布式为
②该锰的硅化物的化学式为
您最近一年使用:0次
2023-08-04更新
|
279次组卷
|
2卷引用:广东省河源市2022-2023学年高三下学期开学考试化学试题
21-22高三上·广东广州·期末
名校
4 . 回答下列问题:
(1)据世界权威刊物《自然》最近报道,我国科学家选择碲化锆(ZrTe2)和砷化镉(Cd3As2)为材料验证了三维量子霍尔效应,并发现了金属—绝缘体的转换。回答下列问题:
①基态锌原子的电子排布式为___ ,原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态的锌原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的锌原子,其价电子自旋磁量子数的代数和为___ 。
②Cd与Zn同族,价电子数相同,若配离子[Cd(CN)x](x-2)-的中心离子价电子数与配体提供的电子数之和为18,则x=____ 。
③碲和硫同主族,TeO 的空间构型为
的空间构型为___ ,写出一个与TeO 互为等电子体的分子
互为等电子体的分子___ 。
(2)石墨烯是一种二维碳纳米材料,具有优异的光学、力学、电学特性,在材料学、微纳加工、能源、生物医学和药物传递方面具有重要应用前景。1mol石墨烯含六元环的数目为___ ;石墨烯中部分碳原子被氧化后,其平面结构将发生改变,转化为氧化石墨烯(如图),氧化石墨烯中键角α___ (填“>”、“<”或“=”)键角β,原因是___ 。
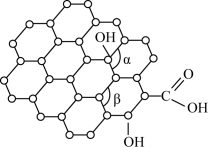
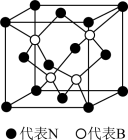
(3)立方氮化硼晶体的结构和硬度都与金刚石相似,晶胞结构如图所示,B原子填在由N原子构成的___ (填“四面体”、“八面体”或“立方体”)空隙中。若晶胞边长为apm,B原子半径为bpm,N原子半径为cpm,则该晶胞的空间利用率为____ (列出计算式),氮硼原子间的最短距离为___ pm。
(1)据世界权威刊物《自然》最近报道,我国科学家选择碲化锆(ZrTe2)和砷化镉(Cd3As2)为材料验证了三维量子霍尔效应,并发现了金属—绝缘体的转换。回答下列问题:
①基态锌原子的电子排布式为
 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态的锌原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的锌原子,其价电子自旋磁量子数的代数和为②Cd与Zn同族,价电子数相同,若配离子[Cd(CN)x](x-2)-的中心离子价电子数与配体提供的电子数之和为18,则x=
③碲和硫同主族,TeO
 的空间构型为
的空间构型为 互为等电子体的分子
互为等电子体的分子(2)石墨烯是一种二维碳纳米材料,具有优异的光学、力学、电学特性,在材料学、微纳加工、能源、生物医学和药物传递方面具有重要应用前景。1mol石墨烯含六元环的数目为

(3)立方氮化硼晶体的结构和硬度都与金刚石相似,晶胞结构如图所示,B原子填在由N原子构成的

您最近一年使用:0次
2022-01-23更新
|
612次组卷
|
4卷引用:广东名校2021-2022学年高三下学期开学测试化学试题
广东名校2021-2022学年高三下学期开学测试化学试题(已下线)广东省华师附中、实验中学、深圳中学、广雅中学四校2021-2022学年高三上学期期末联考化学试题湖南省长沙市雅礼中学2021-2022学年高三下学期月考(七)化学试题湖南省娄底市2022届高三上学期第二次模拟考试化学试题
5 . 氨酸络合剂指含有—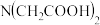 基团的有机化合物,它是一类具有广泛络合性能和强的络合能力的络合剂。
基团的有机化合物,它是一类具有广泛络合性能和强的络合能力的络合剂。
Ⅰ、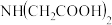 Ⅱ、
Ⅱ、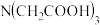 Ⅲ、
Ⅲ、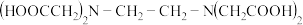
(1)基态氮原子价电子排布式为___________ 。
(2) 、
、 、
、 的沸点由高到低顺序为
的沸点由高到低顺序为___________ 。
(3)Ⅰ、Ⅱ、Ⅲ都可以与 形成络合物
形成络合物
①铜元素位于元素周期表第四周期第___________ 族。
②预测___________ (填编号“Ⅰ”、“Ⅱ”、“Ⅲ”)与 形成的络合物最稳定。
形成的络合物最稳定。
(4)下列说法正确的有___________ 。
A.在Ⅰ、Ⅱ、Ⅲ中N原子采取的都是 杂化
杂化
B.在Ⅱ中C元素的电负性最大
C.在Ⅲ中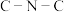 键角是
键角是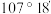
D.在Ⅲ中N元素的第一电离能最大。
E.在Ⅲ中碳氧键的键能均相等
(5)某杂志报道了一种磷化硼纳米颗粒作为高选择性 电化学还原为甲醇的非金属电催化剂。磷化硼熔点特别高,处于极高温的空气环境时也具有抗氧化作用。其晶胞结构如图所示:
电化学还原为甲醇的非金属电催化剂。磷化硼熔点特别高,处于极高温的空气环境时也具有抗氧化作用。其晶胞结构如图所示:
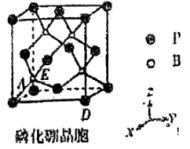
①磷化硼晶体中与硼原子距离最近且相等的硼原子数为___________ 。
②若图中A处磷原子坐标为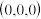 ,D处磷原子坐标为
,D处磷原子坐标为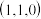 ,则E处的硼原子坐标为
,则E处的硼原子坐标为___________ 。
③已知磷化硼晶胞中A处磷原子与D处磷原子间的距离为a ,则硼原子与最近磷原子的核间距为
,则硼原子与最近磷原子的核间距为___________  。
。
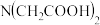 基团的有机化合物,它是一类具有广泛络合性能和强的络合能力的络合剂。
基团的有机化合物,它是一类具有广泛络合性能和强的络合能力的络合剂。Ⅰ、
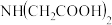 Ⅱ、
Ⅱ、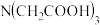 Ⅲ、
Ⅲ、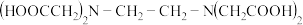
(1)基态氮原子价电子排布式为
(2)
 、
、 、
、 的沸点由高到低顺序为
的沸点由高到低顺序为(3)Ⅰ、Ⅱ、Ⅲ都可以与
 形成络合物
形成络合物①铜元素位于元素周期表第四周期第
②预测
 形成的络合物最稳定。
形成的络合物最稳定。(4)下列说法正确的有
A.在Ⅰ、Ⅱ、Ⅲ中N原子采取的都是
 杂化
杂化B.在Ⅱ中C元素的电负性最大
C.在Ⅲ中
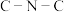 键角是
键角是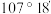
D.在Ⅲ中N元素的第一电离能最大。
E.在Ⅲ中碳氧键的键能均相等
(5)某杂志报道了一种磷化硼纳米颗粒作为高选择性
 电化学还原为甲醇的非金属电催化剂。磷化硼熔点特别高,处于极高温的空气环境时也具有抗氧化作用。其晶胞结构如图所示:
电化学还原为甲醇的非金属电催化剂。磷化硼熔点特别高,处于极高温的空气环境时也具有抗氧化作用。其晶胞结构如图所示:
①磷化硼晶体中与硼原子距离最近且相等的硼原子数为
②若图中A处磷原子坐标为
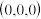 ,D处磷原子坐标为
,D处磷原子坐标为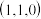 ,则E处的硼原子坐标为
,则E处的硼原子坐标为③已知磷化硼晶胞中A处磷原子与D处磷原子间的距离为a
 ,则硼原子与最近磷原子的核间距为
,则硼原子与最近磷原子的核间距为 。
。
您最近一年使用:0次
2021-08-17更新
|
190次组卷
|
2卷引用:广东省广州市四校2022届高三8月联考化学试题
6 . 晶体硅是制备太阳能电池板的主要原料,电池板中还含有硼、钛、钙等元素。回答下列问题:
(1)基态Ti原子的价层电子排布式为___ 。根据____ 规则可知硅、硼元素一些化学性质相似。
(2)NaBH4所含元素中第一电离能最小的是_______ (填元素符号)。 与NH3的VSEPR模型相似,
与NH3的VSEPR模型相似, 的键角大于NH3的键角的原因是
的键角大于NH3的键角的原因是___ ,任意写出一种 的等电子体
的等电子体___ (写粒子符号)。
(3)硅酸根有多种结构形式,一种无限长链状结构如图1所示,其化学式为_______ 。

(4)硼砂的构成为Na2[B4O5(OH)4]·8H2O,其阴离子[B4O5(OH)4]2-的结构如图2所示。B的杂化方式为___ 。硼砂中不存在___ (填标号)。
A.氢键 B.金属键 C.配位键 D.离子键
(5)钙钛矿晶体的结构如图3所示。假设把氧离子看作硬球接触模型,钛离子位于氧离子形成的正八面体中心,钙离子位于立方晶胞的体心。一个钙离子被___ 个氧离子包围。若钛离子与钙离子间最短距离为apm,则氧离子半径为___ pm。

(1)基态Ti原子的价层电子排布式为
(2)NaBH4所含元素中第一电离能最小的是
 与NH3的VSEPR模型相似,
与NH3的VSEPR模型相似, 的键角大于NH3的键角的原因是
的键角大于NH3的键角的原因是 的等电子体
的等电子体(3)硅酸根有多种结构形式,一种无限长链状结构如图1所示,其化学式为

(4)硼砂的构成为Na2[B4O5(OH)4]·8H2O,其阴离子[B4O5(OH)4]2-的结构如图2所示。B的杂化方式为
A.氢键 B.金属键 C.配位键 D.离子键
(5)钙钛矿晶体的结构如图3所示。假设把氧离子看作硬球接触模型,钛离子位于氧离子形成的正八面体中心,钙离子位于立方晶胞的体心。一个钙离子被

您最近一年使用:0次



