1 . 氮、碳、硼元素形成的化合物具有独特的结构。请回答:
(1)固态的N2O5为离子晶体(阴阳离子中所含原子个数均不超过4个),其阳离子的空间结构名称为___________ ,阴离子中氮原子的杂化方式为___________ 。
(2)比较酸性强弱:
___________  (填“>”、“<”),请说明理由
(填“>”、“<”),请说明理由___________ 。
(3)当石墨被过量的K处理后(未反应的金属被汞洗出),K+离子在石墨层间嵌入,K+层在石墨层的投影如图所示。该钾石墨晶体的化学式是___________ ,晶体类型是___________ 。不正确 的是___________。
(5)硼砂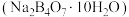 与NaOH的混合溶液中加入H2O2可以制备
与NaOH的混合溶液中加入H2O2可以制备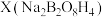 ,已知X的阴离子
,已知X的阴离子 只有一种化学环境的B原子,且B和O原子最外层都达到8电子稳定结构,写出X阴离子的结构式
只有一种化学环境的B原子,且B和O原子最外层都达到8电子稳定结构,写出X阴离子的结构式___________ 。
(1)固态的N2O5为离子晶体(阴阳离子中所含原子个数均不超过4个),其阳离子的空间结构名称为
(2)比较酸性强弱:

 (填“>”、“<”),请说明理由
(填“>”、“<”),请说明理由(3)当石墨被过量的K处理后(未反应的金属被汞洗出),K+离子在石墨层间嵌入,K+层在石墨层的投影如图所示。该钾石墨晶体的化学式是
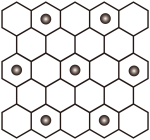
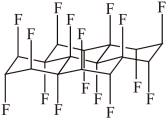
| A.与石墨相比,(CF)x导电性增强 | B.与石墨相比,(CF)x抗氧化性增强 |
| C.(CF)x中C—F的键长比C—C短 | D.1mol(CF)x中含有2x mol共价单键 |
(5)硼砂
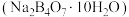 与NaOH的混合溶液中加入H2O2可以制备
与NaOH的混合溶液中加入H2O2可以制备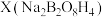 ,已知X的阴离子
,已知X的阴离子 只有一种化学环境的B原子,且B和O原子最外层都达到8电子稳定结构,写出X阴离子的结构式
只有一种化学环境的B原子,且B和O原子最外层都达到8电子稳定结构,写出X阴离子的结构式
您最近一年使用:0次
名校
2 . 图甲是的拉维斯结构,Mg以金刚石方式堆积,在八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu,图乙是沿立方格子对角面取得的截图。___________
(2)阿伏伽德罗常数值为 ,则该晶体的密度为
,则该晶体的密度为___________  (列出计算式)。
(列出计算式)。
(3)两个 原子之间的最短距离为
原子之间的最短距离为___________ , 原子围成的八面体空隙的边长为
原子围成的八面体空隙的边长为___________ 。

(2)阿伏伽德罗常数值为
 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式)。
(列出计算式)。(3)两个
 原子之间的最短距离为
原子之间的最短距离为 原子围成的八面体空隙的边长为
原子围成的八面体空隙的边长为
您最近一年使用:0次
3 . 回答下列问题。
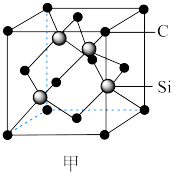
(1)金刚砂(SiC)的硬度为9.5,其晶胞结构如图甲所示,则金刚砂晶体类型为___________ ;若晶胞的边长为a pm,则金刚砂的密度表达式为___________  。
。
(2)硅的某种单质的晶胞结构如图乙所示。
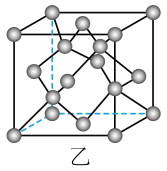
若该硅晶体的密度为ρg·cm-3,阿伏加德罗常数的值为NA,则晶体中最近的两个硅原子之间的距离为___________ cm(用代数式表示)。
(1)金刚砂(SiC)的硬度为9.5,其晶胞结构如图甲所示,则金刚砂晶体类型为
 。
。
(2)硅的某种单质的晶胞结构如图乙所示。

若该硅晶体的密度为ρg·cm-3,阿伏加德罗常数的值为NA,则晶体中最近的两个硅原子之间的距离为
您最近一年使用:0次
名校
解题方法
4 . 化学,让生活更美好。回答下列问题:
(1)乳酸亚铁 是一种常用的补铁剂。
是一种常用的补铁剂。
①基态 核外电子的空间运动状态有
核外电子的空间运动状态有__________ 种。
②乳酸分子中 键与
键与 键的数目比为
键的数目比为__________ 。
③乳酸亚铁中各元素的电负性由大到小的顺序为__________ 。
(2)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:

①该新药分子中有__________ 种不同化学环境的C原子。
②研究发现,适量硒酸钠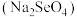 可减轻重金属铊引起的中毒。比较键角大小:
可减轻重金属铊引起的中毒。比较键角大小:
__________  (填“
(填“ ”、“
”、“ ”或“
”或“ ”),原因是
”),原因是__________ 。
(3) 广泛应用于太阳能电池领域。以
广泛应用于太阳能电池领域。以 、
、 和抗坏血酸为原料,可制备
和抗坏血酸为原料,可制备 。抗坏血酸的分子结构如图1所示,
。抗坏血酸的分子结构如图1所示, 晶胞如图2所示。
晶胞如图2所示。

①抗坏血酸的分子式是__________ , 的价层电子轨道表示式为
的价层电子轨道表示式为__________ 。
②下列说法中不正确 的是__________ 。
A.抗坏血酸分子中碳原子的轨道杂化类型为
B.抗坏血酸难溶于水,易溶于乙醇
C.抗坏血酸与足量氢气完全催化还原后的分子中有5个手性碳原子
D. 在水溶液中以
在水溶液中以 形式存在,
形式存在, 的配位原子为
的配位原子为
③ 晶胞为立方体,边长为
晶胞为立方体,边长为 ,设
,设 为阿伏加德罗常数的值,则晶胞的密度
为阿伏加德罗常数的值,则晶胞的密度
__________  。
。
(1)乳酸亚铁
 是一种常用的补铁剂。
是一种常用的补铁剂。①基态
 核外电子的空间运动状态有
核外电子的空间运动状态有②乳酸分子中
 键与
键与 键的数目比为
键的数目比为③乳酸亚铁中各元素的电负性由大到小的顺序为
(2)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:

①该新药分子中有
②研究发现,适量硒酸钠
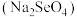 可减轻重金属铊引起的中毒。比较键角大小:
可减轻重金属铊引起的中毒。比较键角大小:
 (填“
(填“ ”、“
”、“ ”或“
”或“ ”),原因是
”),原因是(3)
 广泛应用于太阳能电池领域。以
广泛应用于太阳能电池领域。以 、
、 和抗坏血酸为原料,可制备
和抗坏血酸为原料,可制备 。抗坏血酸的分子结构如图1所示,
。抗坏血酸的分子结构如图1所示, 晶胞如图2所示。
晶胞如图2所示。
①抗坏血酸的分子式是
 的价层电子轨道表示式为
的价层电子轨道表示式为②下列说法中
A.抗坏血酸分子中碳原子的轨道杂化类型为

B.抗坏血酸难溶于水,易溶于乙醇
C.抗坏血酸与足量氢气完全催化还原后的分子中有5个手性碳原子
D.
 在水溶液中以
在水溶液中以 形式存在,
形式存在, 的配位原子为
的配位原子为
③
 晶胞为立方体,边长为
晶胞为立方体,边长为 ,设
,设 为阿伏加德罗常数的值,则晶胞的密度
为阿伏加德罗常数的值,则晶胞的密度
 。
。
您最近一年使用:0次
5 . 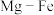 新型储氢合金的晶胞如图所示,该晶胞为立方体,晶胞棱长为a nm。
新型储氢合金的晶胞如图所示,该晶胞为立方体,晶胞棱长为a nm。

(1)基态Fe原子共有__________ 种空间运动状态的电子;基态 的价层电子排布式为
的价层电子排布式为__________ 。
(2)下列说法正确的是__________。
(3)该晶体化学式为__________ ;设阿伏加德罗常数的值为 ,则该晶胞密度为
,则该晶胞密度为__________  。(只需列出计算的表达式)
。(只需列出计算的表达式)
(4)每个Fe周围与它最近且等距的Mg有__________ 个。
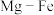 新型储氢合金的晶胞如图所示,该晶胞为立方体,晶胞棱长为a nm。
新型储氢合金的晶胞如图所示,该晶胞为立方体,晶胞棱长为a nm。
(1)基态Fe原子共有
 的价层电子排布式为
的价层电子排布式为(2)下列说法正确的是__________。
| A.该晶胞与金刚石晶胞结构相似 | B.铁原子之间最短距离为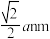 |
| C.该合金储氢过程是化学吸附 | D.储氢后材料中存在离子键、共价键和分子间作用力 |
(3)该晶体化学式为
 ,则该晶胞密度为
,则该晶胞密度为 。(只需列出计算的表达式)
。(只需列出计算的表达式)(4)每个Fe周围与它最近且等距的Mg有
您最近一年使用:0次
名校
解题方法
6 . 铜的化合物种类繁多,应用广泛。请回答:
(1)Cu在周期表中的_______ 区,当焰色试验时Cu的一个3d轨道电子会跃迁至4p轨道,写出该激发态Cu核外的电子排布式_______ 。
(2)[Cu(NH3)4]SO4·H2O是一种农业杀虫剂。
①下列相关说法正确的是_______ 。
A.该化合物中NH3的中心原子的杂化轨道类型为sp3
B.该化合物中存在的化学键有离子键、共价键、配位键和氢键
C.组成该化合物的元素N、O、S中,第一电离能最大的是N
D.根据VSEPR模型预测的 的空间结构是正四面体形
的空间结构是正四面体形
②比较键角∠H-N-H的大小:NH3_______ [Cu(NH3)]2+(填“>”或“<”),理由是_______ 。
(3)某磷青铜晶体的晶胞结构如图所示,则该晶体中与磷原子距离最近的铜原子共有_______ 个,若晶体的密度为 g/cm3,阿伏加德罗常数的值为NA,则晶胞的边长a=
g/cm3,阿伏加德罗常数的值为NA,则晶胞的边长a=_______ nm。
(1)Cu在周期表中的
(2)[Cu(NH3)4]SO4·H2O是一种农业杀虫剂。
①下列相关说法正确的是
A.该化合物中NH3的中心原子的杂化轨道类型为sp3
B.该化合物中存在的化学键有离子键、共价键、配位键和氢键
C.组成该化合物的元素N、O、S中,第一电离能最大的是N
D.根据VSEPR模型预测的
 的空间结构是正四面体形
的空间结构是正四面体形②比较键角∠H-N-H的大小:NH3
(3)某磷青铜晶体的晶胞结构如图所示,则该晶体中与磷原子距离最近的铜原子共有
 g/cm3,阿伏加德罗常数的值为NA,则晶胞的边长a=
g/cm3,阿伏加德罗常数的值为NA,则晶胞的边长a=
您最近一年使用:0次
7 . 铝是常见金属,其合金、化合物在生产生活中有重要应用。请回答:
(1)能量最低的激发态 的核外电子排布式是
的核外电子排布式是___________ 。
(2)铝能与H、C、N、F、Cl 等元素形成多种化合物
①下列说法不正确 的是___________ 。
A. 中Al原子的杂化方式是sp2
中Al原子的杂化方式是sp2
B.化学键中离子键成分的百分数: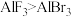
C. 分子中有6对共用电子对
分子中有6对共用电子对
D. 中所有原子或离子满足8 电子稳定结构
中所有原子或离子满足8 电子稳定结构
②常温下 AlCl3在四氯化碳中的溶解度大于MgCl2,理由是___________ 。
③三乙基铝是一种金属有机物,结构简式为Al(C2H5)3,可做高能火箭燃料,原因是___________ 。
(3)AlP 晶胞结构如下图所示:
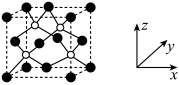
①磷化铝晶胞沿着 y轴的投影图为_________ (填选项字母)。
A. B.
B.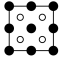 C.
C.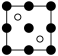 D.
D.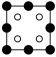
②若磷化铝的晶胞边长为 apm,NA表示阿伏加德罗常数的值,则 AlP晶体的密度为_________ g∙cm−3(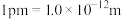 用含 NA、a 的最简代数式表示)。
用含 NA、a 的最简代数式表示)。
(1)能量最低的激发态
 的核外电子排布式是
的核外电子排布式是(2)铝能与H、C、N、F、Cl 等元素形成多种化合物
①下列说法
A.
 中Al原子的杂化方式是sp2
中Al原子的杂化方式是sp2B.化学键中离子键成分的百分数:
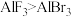
C.
 分子中有6对共用电子对
分子中有6对共用电子对D.
 中所有原子或离子满足8 电子稳定结构
中所有原子或离子满足8 电子稳定结构②常温下 AlCl3在四氯化碳中的溶解度大于MgCl2,理由是
③三乙基铝是一种金属有机物,结构简式为Al(C2H5)3,可做高能火箭燃料,原因是
(3)AlP 晶胞结构如下图所示:

①磷化铝晶胞沿着 y轴的投影图为
A.
 B.
B. C.
C. D.
D.
②若磷化铝的晶胞边长为 apm,NA表示阿伏加德罗常数的值,则 AlP晶体的密度为
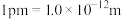 用含 NA、a 的最简代数式表示)。
用含 NA、a 的最简代数式表示)。
您最近一年使用:0次
22-23高二下·浙江·期中
解题方法
8 . 小沁老师在检查同学们的笔记时,由于错误过多而火冒三丈,把红笔扔下,请你帮助她找出剩下的笔记中需要更改的内容_______ 。

A.在上图的晶胞中,原子分数坐标参数A为 ,C为
,C为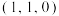 ,B为
,B为 ,则E原子的坐标为
,则E原子的坐标为
B.邻羟基苯乙醛的结构简式(虚线表示氢键):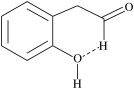
C.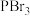 的VSEPR模型:正四面体型
的VSEPR模型:正四面体型
D.标况下 氯乙烷分子数:
氯乙烷分子数:
E.硼烷氨络合物( )的结构式:
)的结构式: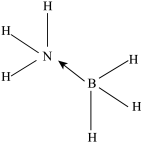

A.在上图的晶胞中,原子分数坐标参数A为
 ,C为
,C为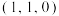 ,B为
,B为 ,则E原子的坐标为
,则E原子的坐标为
B.邻羟基苯乙醛的结构简式(虚线表示氢键):

C.
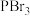 的VSEPR模型:正四面体型
的VSEPR模型:正四面体型D.标况下
 氯乙烷分子数:
氯乙烷分子数:
E.硼烷氨络合物(
 )的结构式:
)的结构式:
您最近一年使用:0次
9 . 富勒烯( )是一类完全由碳组成的中空分子,在催化、光电等很多领域都有重要作用。
)是一类完全由碳组成的中空分子,在催化、光电等很多领域都有重要作用。
Ⅰ. 以其完美的球烯受到科学家重视,其结构如图所示。60个碳原子是等同的,均为近似
以其完美的球烯受到科学家重视,其结构如图所示。60个碳原子是等同的,均为近似 杂化,但却有两种不同类型的碳碳键。其中一种为
杂化,但却有两种不同类型的碳碳键。其中一种为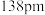 ;另一种为
;另一种为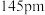 。
。
(1) 在水中溶解度
在水中溶解度_______  在甲苯中溶解度(填“>”、“<”或“≈”)
在甲苯中溶解度(填“>”、“<”或“≈”)
(2)石墨、 互为同素异形体,但相同条件下,石墨的熔点比
互为同素异形体,但相同条件下,石墨的熔点比 高得多,原因是
高得多,原因是_______ 。
Ⅱ.常态下是为紫色固体,不导电,但给富勒烯掺杂金属后(用金属原子把富勒烯分子连起来或者把金属原子放进富勒烯笼子里),其在一定条件下甚至可以成为超导体。
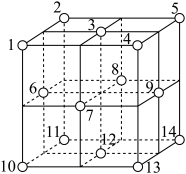
(3) 的晶胞结构如图所示、每个白球代表1个
的晶胞结构如图所示、每个白球代表1个 分子,已知一定条件下晶胞的棱长为
分子,已知一定条件下晶胞的棱长为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该条件下
,则该条件下 的摩尔体积为
的摩尔体积为_______  (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
(4) 晶体结构中存在四面体空隙(如图中1、3、6、7围成的空隙)和八面体空隙(如图中3、6、7、8、9、12围成的空隙),所有空隙中均填充一个金属M原子,可获得某条件下的超导材料、则该超导材料中,平均一个
晶体结构中存在四面体空隙(如图中1、3、6、7围成的空隙)和八面体空隙(如图中3、6、7、8、9、12围成的空隙),所有空隙中均填充一个金属M原子,可获得某条件下的超导材料、则该超导材料中,平均一个 晶胞需掺杂
晶胞需掺杂_______ 个M原子。
 )是一类完全由碳组成的中空分子,在催化、光电等很多领域都有重要作用。
)是一类完全由碳组成的中空分子,在催化、光电等很多领域都有重要作用。Ⅰ.
 以其完美的球烯受到科学家重视,其结构如图所示。60个碳原子是等同的,均为近似
以其完美的球烯受到科学家重视,其结构如图所示。60个碳原子是等同的,均为近似 杂化,但却有两种不同类型的碳碳键。其中一种为
杂化,但却有两种不同类型的碳碳键。其中一种为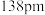 ;另一种为
;另一种为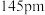 。
。(1)
 在水中溶解度
在水中溶解度 在甲苯中溶解度(填“>”、“<”或“≈”)
在甲苯中溶解度(填“>”、“<”或“≈”)(2)石墨、
 互为同素异形体,但相同条件下,石墨的熔点比
互为同素异形体,但相同条件下,石墨的熔点比 高得多,原因是
高得多,原因是Ⅱ.常态下是为紫色固体,不导电,但给富勒烯掺杂金属后(用金属原子把富勒烯分子连起来或者把金属原子放进富勒烯笼子里),其在一定条件下甚至可以成为超导体。
(3)
 的晶胞结构如图所示、每个白球代表1个
的晶胞结构如图所示、每个白球代表1个 分子,已知一定条件下晶胞的棱长为
分子,已知一定条件下晶胞的棱长为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该条件下
,则该条件下 的摩尔体积为
的摩尔体积为 (用含a、
(用含a、 的代数式表示)。
的代数式表示)。(4)
 晶体结构中存在四面体空隙(如图中1、3、6、7围成的空隙)和八面体空隙(如图中3、6、7、8、9、12围成的空隙),所有空隙中均填充一个金属M原子,可获得某条件下的超导材料、则该超导材料中,平均一个
晶体结构中存在四面体空隙(如图中1、3、6、7围成的空隙)和八面体空隙(如图中3、6、7、8、9、12围成的空隙),所有空隙中均填充一个金属M原子,可获得某条件下的超导材料、则该超导材料中,平均一个 晶胞需掺杂
晶胞需掺杂
您最近一年使用:0次
10 . 某晶体晶胞结构如图所示,●表示X , 表示Y,请回答下列问题:
表示Y,请回答下列问题:

(1)晶体中每个X周围与之等距且距离最近的Y有___________ 个,每个Y周围与之等距且距离最近的Y有___________ 个,每个晶胞中含X的个数为___________ 个,该晶体的化学式为___________ 。
(2)若该晶胞的边长为a cm,则晶体的密度为___________ g·cm-3(列出计算式即可,已知该物质的摩尔质量为M g/mol,阿伏加德罗常数为NA)。
 表示Y,请回答下列问题:
表示Y,请回答下列问题:
(1)晶体中每个X周围与之等距且距离最近的Y有
(2)若该晶胞的边长为a cm,则晶体的密度为
您最近一年使用:0次



