1 . 设 为阿伏伽德罗常数,下列说法错误的是
为阿伏伽德罗常数,下列说法错误的是
 为阿伏伽德罗常数,下列说法错误的是
为阿伏伽德罗常数,下列说法错误的是A.晶体 中 中 十二元环平均含有 十二元环平均含有 个 个 键 键 |
B. 金刚石晶体中含有 金刚石晶体中含有 个 个 键 键 |
C. 碳化硅晶胞中含有 碳化硅晶胞中含有 个C-Si键 个C-Si键 |
D.晶体硅中 六元环平均含有 六元环平均含有 个 个 键 键 |
您最近一年使用:0次
名校
解题方法
2 . 碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

| A.在石墨烯晶体中,每个C原子连接3个六元环,每个六元环占有2个C原子 |
B.金刚石晶体中,C原子采取 杂化 杂化 |
C.金刚石晶体中 形成 形成 |
| D.在金刚石晶体中,C原子所连接的最小环为六元环,每个C原子连接12个六元环 |
您最近一年使用:0次
名校
3 . “铜纳米催化剂室温催化氨硼烷产氢串联选择性还原催化3-硝基苯乙烯到3-氨基苯乙烯”在有机化学选择性加氢反应研究领域取得重要进展。
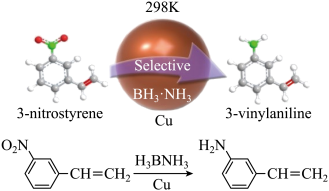
请回答下列问题:
(1)下列分别为B、C、N、Cu基态原子价电子排布图,其中正确的是_____(填标号)
(2)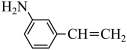 物质的沸点高于
物质的沸点高于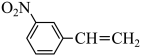 ,原因是
,原因是_____ ,硝基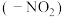 和氨基
和氨基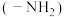 中N的杂化方式分别为
中N的杂化方式分别为_____ 。
(3)碳的第三种同素异形体——金刚石,其晶胞如图所示。已知金属钠的晶胞(体心立方堆积)沿其体对角线垂直在纸平面上的投影图如图A所示,则金刚石晶胞沿其体对角线垂直在纸平面上的投影图应该是图_____(从A~D图中选填)。

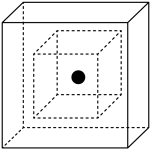
(4)SiC结构类似金刚石,则SiC为_____ 晶体。图为SiC的晶胞图,其中两个正方体中心重合、各面分别平行,其中心为Si原子(用●表示),其余Si原子位于大正方体的_____ 位置。
(5)科学研究表明, 是由
是由 、
、 、
、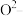 通过离子键而组成的复杂离子晶体。
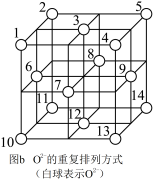
通过离子键而组成的复杂离子晶体。 的重复排列方式如图b所示,
的重复排列方式如图b所示, 中有一半的
中有一半的 填充在正四面体空隙中,另一半
填充在正四面体空隙中,另一半 和
和 地填充在正八面体空隙中,则
地填充在正八面体空隙中,则 晶体中,正四面体空隙数与
晶体中,正四面体空隙数与 数之比为
数之比为_____ ,其中有_____ %正四面体空隙填有 ,有
,有_____ %正八面体空隙没有被填充。

请回答下列问题:
(1)下列分别为B、C、N、Cu基态原子价电子排布图,其中正确的是_____(填标号)
A.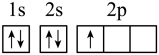 | B.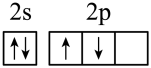 |
C.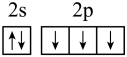 | D.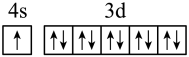 |
 物质的沸点高于
物质的沸点高于 ,原因是
,原因是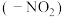 和氨基
和氨基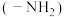 中N的杂化方式分别为
中N的杂化方式分别为(3)碳的第三种同素异形体——金刚石,其晶胞如图所示。已知金属钠的晶胞(体心立方堆积)沿其体对角线垂直在纸平面上的投影图如图A所示,则金刚石晶胞沿其体对角线垂直在纸平面上的投影图应该是图_____(从A~D图中选填)。

A.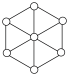 | B.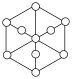 | C.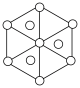 | D.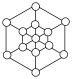 |


(5)科学研究表明,
 是由
是由 、
、 、
、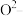 通过离子键而组成的复杂离子晶体。
通过离子键而组成的复杂离子晶体。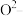 的重复排列方式如图b所示,
的重复排列方式如图b所示, 中有一半的
中有一半的 填充在正四面体空隙中,另一半
填充在正四面体空隙中,另一半 和
和 地填充在正八面体空隙中,则
地填充在正八面体空隙中,则 晶体中,正四面体空隙数与
晶体中,正四面体空隙数与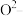 数之比为
数之比为 ,有
,有
您最近一年使用:0次
4 . 下面有关晶体的叙述中,不正确的是
A.氯化钠晶体中,每个 周围距离相等的 周围距离相等的 共有6个 共有6个 |
| B.金刚石为空间网状结构,由共价键形成的碳原子环中,最小的环上有6个碳原子 |
C.氯化铯晶体中,每个 周围紧邻8个 周围紧邻8个 |
D.干冰晶体中,每个 分子周围紧邻12个 分子周围紧邻12个 分子 分子 |
您最近一年使用:0次
2023-10-09更新
|
183次组卷
|
2卷引用:河北省沧州市泊头市第一中学2023-2024学年高二下学期4月月考化学试题
5 . 我国科学家预言的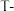 碳已被合成。
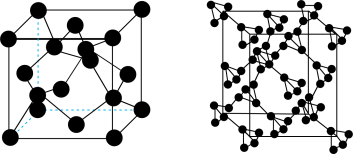
碳已被合成。 碳的晶体结构可看作将金刚石中的碳原子用由四个碳原子组成的正四面体结构单元取代所得,金刚石和
碳的晶体结构可看作将金刚石中的碳原子用由四个碳原子组成的正四面体结构单元取代所得,金刚石和 碳的晶胞如图所示。下列说法正确的是
碳的晶胞如图所示。下列说法正确的是
 碳已被合成。
碳已被合成。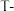 碳的晶体结构可看作将金刚石中的碳原子用由四个碳原子组成的正四面体结构单元取代所得,金刚石和
碳的晶体结构可看作将金刚石中的碳原子用由四个碳原子组成的正四面体结构单元取代所得,金刚石和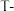 碳的晶胞如图所示。下列说法正确的是
碳的晶胞如图所示。下列说法正确的是
| A.金刚石中每个碳原子被12个最小环共用 | B.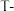 碳中最小环由24个碳原子组成 碳中最小环由24个碳原子组成 |
C.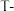 碳属于分子晶体 碳属于分子晶体 | D. 碳中键角是 碳中键角是 |
您最近一年使用:0次
2023-06-01更新
|
296次组卷
|
2卷引用:湖北省高中名校联盟2022-2023学年高二下学期5月联合测评化学试卷
名校
解题方法
6 . 下列关于SiO2和金刚石的叙述正确的是
| A.SiO2的晶体结构中,每个Si原子与2个O原子直接相连 |
| B.通常状况下,1molSiO2晶体中含有的分子数为NA(NA表示阿伏加德罗常数的值) |
| C.金刚石的网状结构中,由共价键形成的最小环上有6个碳原子 |
| D.1mol金刚石中含有4NA个C-C键(NA表示阿伏加德罗常数的值) |
您最近一年使用:0次
2023-01-13更新
|
1423次组卷
|
12卷引用:湖南省株洲市第一中学2022-2023学年高二下学期第一次月考化学试题
湖南省株洲市第一中学2022-2023学年高二下学期第一次月考化学试题湖北省宜昌英杰学校2022-2023学年高二3月月考化学试题黑龙江省哈尔滨市第四中学校2022-2023学年高二下学期4月月考化学试题2014-2015学年辽宁实验中学等五校高二下期末化学试卷(人教版2019)选择性必修2 第三章 晶体结构与性质 第二节 分子晶体与共价晶体 课时2 共价晶体四川省成都市龙泉驿区教育科学研究院2021-2022学年高二下学期期中考试化学试卷(已下线)第43练 分子晶体与共价晶体-2023年高考化学一轮复习小题多维练(全国通用)吉林省通化市梅河口市第五中学2022-2023学年高二上学期期末考试化学试题(已下线)3.2.2 共价晶体-同步学习必备知识甘肃省武威市凉州区2022-2023学年高二下学期期中考试化学试题(已下线)热点07 分子晶体与共价晶体3.2.2 共价晶体-随堂练习
名校
解题方法
7 . 碳化物衍生碳以其独特的性能被广泛应用在超级电容器、催化剂载体等方面。常用氯气刻蚀法制备。该方法通过高温氯化2小时在SiC表面制备碳涂层(已知: 的沸点是59℃,极易水解),其方法如图:
的沸点是59℃,极易水解),其方法如图:

(1)圆底烧瓶A中为氯酸钾固体,仪器a中的试剂是______________________ ,A中发生反应的化学方程式为__________________ 。
(2)仪器C中所盛物质为_______________ 。
(3)高温环境氯气与氩气混合气氛中氯气与SiC反应,将Si原子从SiC中刻蚀掉形成碳层,反应的化学方程式为__________________ ,如果温度超过1175℃,涂层上的碳结构发生如下变化:碳→骨架碳→非晶碳→石墨碳,则碳涂层硬度会______________ (填“逐渐变高”或“逐渐变低”),SiC熔点远高于 的原因是
的原因是__________________ 。
(4)装置F的作用是__________________ ,NaOH溶液中生成的盐除了NaCl外,还有__________________ 。
 的沸点是59℃,极易水解),其方法如图:
的沸点是59℃,极易水解),其方法如图:
(1)圆底烧瓶A中为氯酸钾固体,仪器a中的试剂是
(2)仪器C中所盛物质为
(3)高温环境氯气与氩气混合气氛中氯气与SiC反应,将Si原子从SiC中刻蚀掉形成碳层,反应的化学方程式为
 的原因是
的原因是(4)装置F的作用是
您最近一年使用:0次
2022-11-19更新
|
367次组卷
|
2卷引用:重庆市第八中学2023届高三上学期适应性月考卷(三)化学试题
名校
解题方法
8 . 下列说法错误的是
A.从CH4、 、 、 为正四面体结构,可推测PH 为正四面体结构,可推测PH 、 、 也为正四面体结构 也为正四面体结构 |
| B.1mol金刚石晶体中,平均含有2molC-C键 |
| C.水的沸点比硫化氢的高,是因为H2O分子间存在氢键,H2S分子间不能形成氢键 |
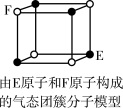
| D.某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE |
您最近一年使用:0次
2022-10-31更新
|
243次组卷
|
8卷引用:贵州省遵义市习水县一中2018-2019学年高二上学期11月考试化学试题
9 . 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
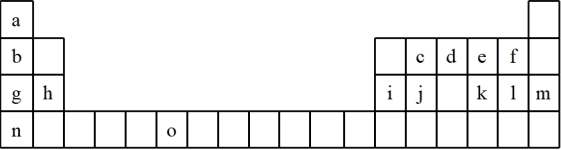
(1)请写出元素“o”的基态原子的价电子排布式_______ 。
(2)k在空气中燃烧产物的分子构型为_______ ,中心原子的杂化形式为_______ ,该分子是_______ (填“极性”或“非极性”)分子。
(3)由j原子跟c原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同。两者相比熔点更高的是(写化学式)_______ ,试从结构角度加以解释_______ 。
(4)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。

若已知i的原子半径为dcm,NA代表阿伏加德罗常数,i的相对原子质量为M,请回答:
①晶胞中i原子的配位数为_______ 。
②该晶体的密度为_______ g/cm3。

(1)请写出元素“o”的基态原子的价电子排布式
(2)k在空气中燃烧产物的分子构型为
(3)由j原子跟c原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同。两者相比熔点更高的是(写化学式)
(4)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。

若已知i的原子半径为dcm,NA代表阿伏加德罗常数,i的相对原子质量为M,请回答:
①晶胞中i原子的配位数为
②该晶体的密度为
您最近一年使用:0次
解题方法
10 . 下面排序不正确的是
A.晶体的熔点由高到低排列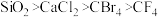 |
B.硬度由大到小:金刚石 碳化硅 碳化硅 晶体硅 晶体硅 |
C.熔点由高到低: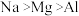 |
D.熔点由高到低: 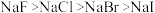 |
您最近一年使用:0次



