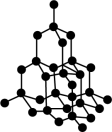
1 . 2022年12月,首架国产大飞机C919正式交付,国之重器,世界瞩目。铼(Re)是生产飞机发动机叶片必不可少的材料。X、Y、Z、Q、W是原子序数依次增大且位于不同主族的短周期元素,其中X、Y、Z三种元素可与铼元素组成一种化合物(结构如图),该化合物与X的单质反应可得到铼。Q是地壳中含量最丰富的金属元素,Z与W形成的化合物为共价晶体。下列说法正确的是
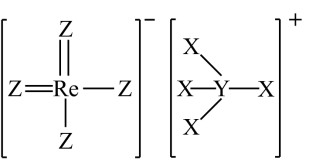
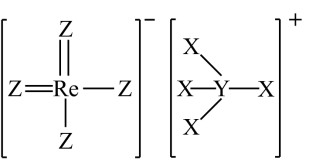
| A.电负性:Z>Y>Q>W |
| B.图中的阳离子存在配位键,但四个键的性质不同 |
| C.熔点:W晶体小于W、Y形成的晶体 |
| D.Q的氧化物可以和氨水反应 |
您最近半年使用:0次
23-24高二下·全国·单元测试
解题方法
2 . 下列变化规律正确的是
| A.NaCl、MgCl2、MgO熔点由低到高 |
| B.H2O、H2S、H2Se的分解温度及沸点都由高到低 |
| C.O2、I2、Hg、NaCl、SiO2熔点由低到高 |
| D.碳化硅、单晶硅、金刚石、石墨熔点由低到高 |
您最近半年使用:0次
3 . 中国科学家首次成功制得大面积单晶石墨炔,是碳材料科学的一大进步。
下列关于金刚石、石墨、石墨炔的说法正确的是
金刚石 |
石墨 |
石墨炔 |
| A.金刚石中最小环为六元环,通过旋转单键,六元环中六个碳可以在同一平面上 |
| B.石墨晶体中存在共价键、分子间作用力、离子键等多种类型作用力 |
| C.等质量的石墨和金刚石中碳碳σ键数目之比为3:4 |
| D.三种物质均能导电 |
您最近半年使用:0次
名校
解题方法
4 . 下列叙述中正确的是
| A.共价晶体(原子晶体)中,共价键的键能越大,熔沸点越高 |
| B.分子晶体中,分子间的作用力越大,该分子越稳定 |
| C.分子晶体中,共价键的键能越大,熔沸点越高 |
| D.共价晶体(原子晶体)中,构成晶体的微粒一定是相同的原子 |
您最近半年使用:0次
5 . 下列说法错误的是
| A.凡是共价晶体都含有共价键 | B.凡是共价晶体都有正四面体结构 |
| C.凡是共价晶体都具有三维骨架结构 | D.凡是共价晶体都具有很高的熔点 |
您最近半年使用:0次
6 . 下列关于共价晶体、分子晶体的叙述中,正确的是
| A.在干冰晶体中,1个CO2分子和6个CO2分子距离最近 |
| B.分子晶体中一定存在共价键 |
| C.HI的相对分子质量大于HF,所以HI的沸点高于HF |
| D.金刚石为共价键三维骨架结构,晶体中的最小环上有6个碳原子 |
您最近半年使用:0次
7 . 下列物质性质的比较,不正确的是
| A.微粒的半径:Al3+<Cl- | B.元素的电负性:P<S<Cl |
| C.共价晶体的硬度:晶体硅>金刚石 | D.离子晶体的熔点:NaCl>CsCl |
您最近半年使用:0次
8 . 部分晶体及分子结构如图所示,下列说法正确的是
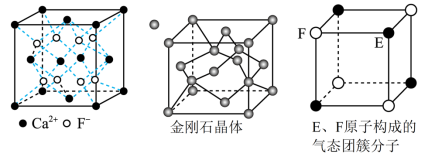

| A.CaF2晶胞中有8个F-,F-配位数是4 |
| B.金刚石晶体中每个碳原子被6个六元环共用,每个六元环最多有4个碳原子共面 |
| C.该气态团簇分子的分子式为E4F4或F4E4 |
| D.三种物质对应的晶体熔沸点最高的是CaF2 |
您最近半年使用:0次
名校
9 . 类比是预测物质性质与化学反应的重要方法,下列类比结果合理的是
A. 的沸点高于 的沸点高于 ,则单晶硅的沸点高于金刚石 ,则单晶硅的沸点高于金刚石 |
B. 分子间可以形成氢键,则 分子间可以形成氢键,则 分子间也可以形成氢键 分子间也可以形成氢键 |
| C.NaCl固体与浓硫酸共热可制HCl,则NaI固体与浓硫酸共热可制HI |
D.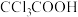 酸性强于 酸性强于 ,则 ,则 酸性强于 酸性强于 |
您最近半年使用:0次
2024-02-29更新
|
511次组卷
|
3卷引用:黑龙江省哈尔滨市第三中学校2023-2024学年高三一模化学试题
名校
解题方法
10 . VA族元素及其化合物应用广泛。 催化氧化生成
催化氧化生成 ,
, 继续被氧化为
继续被氧化为 ,将
,将 通入水中制取
通入水中制取 。工业上用白磷(
。工业上用白磷( )与
)与 反应生成
反应生成 和一种盐,该盐可与
和一种盐,该盐可与 反应制备一元弱酸
反应制备一元弱酸 。雌黄(
。雌黄( )和
)和 在盐酸中反应转化为雄黄(
在盐酸中反应转化为雄黄( )和
)和 (沸点114℃)并放出
(沸点114℃)并放出 气体。砷化镓(
气体。砷化镓( )是第三代半导体材料,熔点高,硬度大。氨硼烷(
)是第三代半导体材料,熔点高,硬度大。氨硼烷( )是最具潜力的储氢材料之一,与乙烷的相对分子质量相近,但沸点却比乙烷高得多。下列说法不正确的是
)是最具潜力的储氢材料之一,与乙烷的相对分子质量相近,但沸点却比乙烷高得多。下列说法不正确的是
 催化氧化生成
催化氧化生成 ,
, 继续被氧化为
继续被氧化为 ,将
,将 通入水中制取
通入水中制取 。工业上用白磷(
。工业上用白磷( )与
)与 反应生成
反应生成 和一种盐,该盐可与
和一种盐,该盐可与 反应制备一元弱酸
反应制备一元弱酸 。雌黄(
。雌黄( )和
)和 在盐酸中反应转化为雄黄(
在盐酸中反应转化为雄黄( )和
)和 (沸点114℃)并放出
(沸点114℃)并放出 气体。砷化镓(
气体。砷化镓( )是第三代半导体材料,熔点高,硬度大。氨硼烷(
)是第三代半导体材料,熔点高,硬度大。氨硼烷( )是最具潜力的储氢材料之一,与乙烷的相对分子质量相近,但沸点却比乙烷高得多。下列说法不正确的是
)是最具潜力的储氢材料之一,与乙烷的相对分子质量相近,但沸点却比乙烷高得多。下列说法不正确的是A. 分子间存在氢键 分子间存在氢键 | B. 是由极性键构成的极性分子 是由极性键构成的极性分子 |
C.1mol 中含有16mol共价键 中含有16mol共价键 | D.固态 和砷化镓晶体都是分子晶体 和砷化镓晶体都是分子晶体 |
您最近半年使用:0次