名校
1 . 氮化铝(AlN)是一种新型无机非金属原料,结构与金刚石相似。常温下AlN+NaOH+H2O=NaAlO2+NH3↑。某课题小组利用下图所示装置测定样品AlN的含量(杂质不反应)。下列说法中正确的是
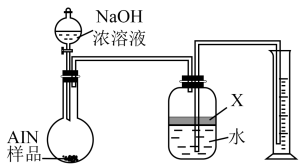

| A.氮化铝是共价晶体,晶体中N、Al原子配位数均为4 |
| B.X可以是CCl4,因为NH3不溶于CCl4而易溶于水 |
| C.若广口瓶中液体未装满,测得NH3的体积将偏大 |
D.若实验中测得样品的质量为w g,氨气的体积为a L(标况下),则样品中AlN的质量分数为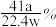 |
您最近一年使用:0次
解题方法
2 . X、Y、Z为三种元素,X能与氢形成气态XH4,其中X的质量分数为75%;且X与Y能形成XY2型化合物。Y的原子核内质子数和中子数相等,在Y的氢化物中,Y的质量分数为88.9%。Z的最高价氧化物的水化物是酸性最强的酸。
(1)X的单质叫做______ ,它属于______ 晶体。
(2)Y的氢化物属于______ 晶体,它的电子式是______ 。
(3)Z元素位于周期表的第______ 周期______ 族,它的氢化物是______ 性分子。
(4)X与Z形成的化合物可用电子式表示为______ ,其分子的空间构型是______ 体,属于______ 性分子,它的晶体属于______ 晶体。
(1)X的单质叫做
(2)Y的氢化物属于
(3)Z元素位于周期表的第
(4)X与Z形成的化合物可用电子式表示为
您最近一年使用:0次
3 . 已知:A、B、C、D、E、F六种元素核电荷数依次增大,属元素周期表中前四周期的元素。其中A原子核外有三个未成对电子;B和E可形成离子化合物B2E,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F原子核外最外层电子数与B相同,其余各层均充满。请根据以上信息,回答下列问题:
⑴A、B、C、D的第一电离能由小到大的顺序为________ (用元素符号表示)。
⑵E与D的同族短周期元素可形成一种化合物X,X是常见的有机溶剂,X分子的空间构型是________ 。
⑶F原子的核外电子排布式是____________ ,F的高价离子与A的简单氢化物形成的配离子的化学式为________ 。
⑷A、F形成某种化合物的晶胞结构如图所示,则其化学式为________ (黑色球表示F原子)。

⑸A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料,其晶体中所含的化学键类型为________ 。
⑴A、B、C、D的第一电离能由小到大的顺序为
⑵E与D的同族短周期元素可形成一种化合物X,X是常见的有机溶剂,X分子的空间构型是
⑶F原子的核外电子排布式是
⑷A、F形成某种化合物的晶胞结构如图所示,则其化学式为

⑸A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料,其晶体中所含的化学键类型为
您最近一年使用:0次
名校
解题方法
4 . 已知A、B、C、D、E、F六种元素的原子序数依次增大,其中A元素的原子半径在短周期元素中最小,B原子核外电子有6种不同的运动状态;D原子L层上有2对成对电子。E元素在地壳中含量居第二位,F与E位于同一周期,且是该周期元素中电负性最大的元素。根据以上信息回答下列问题:
(1)E元素可分别与D元素、F元素形成两种常见化合物,这两种化合物的熔沸点高低顺序为__ (用化学式表示),原因是___ 。
(2)C的氢化物比下周期同族元素的氢化物沸点还要高,其原因是__ 。
(3)1molB2A2分子中含σ键的数目是__ 。
(4)图(Ⅰ)是B元素的单质晶体的一个晶胞,该晶胞中含有__ 个原子,若设晶胞的棱长为acm,阿伏加德罗常数的值为NA则该晶体的密度表达式为__ 。
(5)E单质存在与金刚石结构类似的晶体,晶体中原子之间以__ 相结合,其晶胞中共有8个原子,其中在面心位置贡献__ 个原子。
(6)BD2在高温高压下所形成的晶体其晶胞如图(Ⅱ)所示。该晶体的类型属于__ (填“分子”、“原子”、“离子”或“金属”)晶体,该晶体中B原子轨道的杂化类型为__ 。

(1)E元素可分别与D元素、F元素形成两种常见化合物,这两种化合物的熔沸点高低顺序为
(2)C的氢化物比下周期同族元素的氢化物沸点还要高,其原因是
(3)1molB2A2分子中含σ键的数目是
(4)图(Ⅰ)是B元素的单质晶体的一个晶胞,该晶胞中含有
(5)E单质存在与金刚石结构类似的晶体,晶体中原子之间以
(6)BD2在高温高压下所形成的晶体其晶胞如图(Ⅱ)所示。该晶体的类型属于

您最近一年使用:0次
5 . X是核外电子数最少的元素,Y是地壳中含量最丰富的元素,Z在地壳中的含量仅次于Y,W可以形成自然界中最硬的原子晶体。下列叙述错误的是( )
| A.WX4是沼气的主要成分 | B.固态X2Y是分子晶体 |
| C.W可以形成原子晶体 | D.玛瑙、水晶和玻璃的成分都是ZY2 |
您最近一年使用:0次
6 . 已知X、Y、Z、R都是周期表中前四周期的元素,它们的核电荷数依次增大。X是空气中含量最高的元素,Z基态原子核外K、L、M三层电子数之比为1∶4∶2,R基态原子的3d原子轨道上的电子数是4 s原子轨道上的4倍,Y基态原子的最外层电子数等于Z、R基态原子的最外层电子数之和。(答题时,X、Y、Z、R用所对应的元素符号表示)
(1)X、Y、Z的第一电离能由小到大的顺序为_____ ,写出一种与ZY44-互为等电子体的分子的化学式:_____ 。

(2)R3+基态核外电子排布式为______ 。
(3)化合物Z3X4熔点高达1900℃以上,硬度很大。该物质的晶体类型是_____ 。
(4)Y、Z形成的某晶体的晶胞结构如右图所示,则该化合物的化学式为_____ 。
(5)R2+与过量的氨水形成的配离子的化学式为[R(NH3)6]2+,1 mol [R(NH3)6]2+中含有σ键的数目为______ 。
(1)X、Y、Z的第一电离能由小到大的顺序为

(2)R3+基态核外电子排布式为
(3)化合物Z3X4熔点高达1900℃以上,硬度很大。该物质的晶体类型是
(4)Y、Z形成的某晶体的晶胞结构如右图所示,则该化合物的化学式为
(5)R2+与过量的氨水形成的配离子的化学式为[R(NH3)6]2+,1 mol [R(NH3)6]2+中含有σ键的数目为
您最近一年使用:0次
名校
7 . X是核外电子数最少的元素,Y是地壳中含量最丰富的元素,Z在地壳中的含量仅次于Y,W可以形成自然界中最硬的原子晶体。下列叙述错误的是( )
| A.WX4是沼气的主要成分 | B.固态X2Y是分子晶体 |
| C.ZW是原子晶体 | D.玛瑙、水晶和玻璃的成分都是ZY2 |
您最近一年使用:0次
2018-12-24更新
|
228次组卷
|
5卷引用:云南省元江哈尼族彝族傣族自治县一中2018-2019学年高二上学期12月考试化学试题
2014·陕西西安·一模
8 . 短周期原子序数依次增大的主族元素R、T、Q、W、Y具有如下信息:
① R、Y原子的最外层电子数与电子层数相同;
② Q是地壳中含量最高的元素,R与T的核电荷数之和等于Q的核电荷数;
③ W与R同主族。下列说法正确的是
① R、Y原子的最外层电子数与电子层数相同;
② Q是地壳中含量最高的元素,R与T的核电荷数之和等于Q的核电荷数;
③ W与R同主族。下列说法正确的是
| A.元素Q与W形成的两种常见化合物中含有相同比例的阴、阳离子,属于同种晶体类型 |
| B.元素T、Q、W、Y的原子半径大小为:T<Q<Y<W |
| C.Q与Y组成的常见物质是一种两性物质,结构中含有共价键 |
| D.由Y和T组成的物质YT是原子晶体,在电子和陶瓷工业上有广泛应用,可以直接由单质Y和T在低温下合成 |
您最近一年使用:0次
10-11高三上·云南昆明·阶段练习
解题方法
9 . 已知A、B、C、D、E为原子序数依次增大的五种短周期元素。其中A与D、B与E同主族,C元素的最外层电子数是内层电子数的3倍,D元素在地壳中的含量仅次于氧,D的单质是良好的半导体材料,E元素的最高正价与最低负价的代数和为2。请回答:
(1)E元素的氢化物是 分子(填“极性”或“非极性”),电子式是 。
(2)A、B、C三种元素形成的氢化物的熔点由高到低的顺序是 。(用化学式表示)
(3)B、D、E三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是 ___ 。(用化学式表示)
(4)工业上用A单质制备D单质的化学方程式是 ,D和C形成的固体物质属于 晶体。
(1)E元素的氢化物是 分子(填“极性”或“非极性”),电子式是 。
(2)A、B、C三种元素形成的氢化物的熔点由高到低的顺序是 。(用化学式表示)
(3)B、D、E三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是 ___ 。(用化学式表示)
(4)工业上用A单质制备D单质的化学方程式是 ,D和C形成的固体物质属于 晶体。
您最近一年使用:0次
10 . 已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A与B同周期、A与D同族,A原子核外有两个未成对电子,B元素的第一电离能比同周期相邻两种元素都大,C原子在同周期原子中半径最大(稀有气体除外);E与C位于不同周期,E原子核外最外层电子数与C相同,其余各层电子均充满。请根据以上信息回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)
(1)E原子核外电子排布式是_____________ 。
(2)B的最高价含氧酸根的空间构型为__________________ 。
(3)A、B、D三种元素电负性由大到小排列顺序为____________ 。
(4)D单质比化合物DA的熔点____ (填“高”或“低”),理由是_______________ 。
(5)已知A、C和地壳中含量最多的元素按1∶1∶2的原子个数比可形成某离子化合物,该化合物能使酸性高锰酸钾溶液褪色,写出发生反应的离子方程式___________________________ 。
(1)E原子核外电子排布式是
(2)B的最高价含氧酸根的空间构型为
(3)A、B、D三种元素电负性由大到小排列顺序为
(4)D单质比化合物DA的熔点
(5)已知A、C和地壳中含量最多的元素按1∶1∶2的原子个数比可形成某离子化合物,该化合物能使酸性高锰酸钾溶液褪色,写出发生反应的离子方程式
您最近一年使用:0次
2016-12-09更新
|
172次组卷
|
2卷引用:2015届四川省资阳市高三第三次模拟考试理综化学试卷



