1 . 回答下列问题:
(1)某化学社团为证实Ba(OH)2溶液和H2SO4溶液的反应是离子反应,设计了如下实验。
已知:溶液的导电性由溶液中离子的浓度及离子电荷数决定,可通过观察实验现象,判断溶液中离子浓度的变化,从而证明反应是离子反应。实验装置如图所示:
(2)写出下列情况发生反应的离子方程式:向NaHSO4液中逐滴加入Ba(OH)2溶液至溶液显中性___________ 。
(3)某化工厂排出的废水呈酸性,且其中含大量的Na+、Cu2+、Cl-、 ,为除去废水样品中的Cu2+和
,为除去废水样品中的Cu2+和 ,最终得到中性溶液,设计的方案流程如下图:
,最终得到中性溶液,设计的方案流程如下图:___________ (用离子符号表示)。
②上述流程中,试剂c为___________ (写化学式)。
(1)某化学社团为证实Ba(OH)2溶液和H2SO4溶液的反应是离子反应,设计了如下实验。
已知:溶液的导电性由溶液中离子的浓度及离子电荷数决定,可通过观察实验现象,判断溶液中离子浓度的变化,从而证明反应是离子反应。实验装置如图所示:
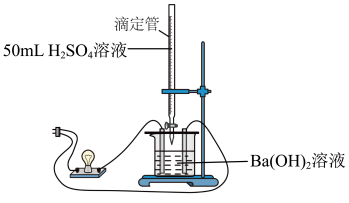
| 实验步骤 | 实验现象 | 实验结论 |
| 连接好装置,向烧杯中加入一定浓度的Ba(OH)2溶液,逐滴滴加H2SO4溶液直至过量,边滴边振荡 | Ba(OH)2溶液和H2SO4溶液的反应是离子反应 |
(2)写出下列情况发生反应的离子方程式:向NaHSO4液中逐滴加入Ba(OH)2溶液至溶液显中性
(3)某化工厂排出的废水呈酸性,且其中含大量的Na+、Cu2+、Cl-、
 ,为除去废水样品中的Cu2+和
,为除去废水样品中的Cu2+和 ,最终得到中性溶液,设计的方案流程如下图:
,最终得到中性溶液,设计的方案流程如下图: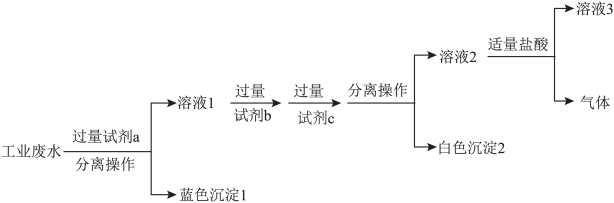
②上述流程中,试剂c为
您最近半年使用:0次
2 . 某学习小组欲从含有 、乙醇和氨水的实验室废液中分离乙醇并制备硫酸铜铵
、乙醇和氨水的实验室废液中分离乙醇并制备硫酸铜铵 晶体,设计方案如下,下列说法
晶体,设计方案如下,下列说法不正确 的是
 、乙醇和氨水的实验室废液中分离乙醇并制备硫酸铜铵
、乙醇和氨水的实验室废液中分离乙醇并制备硫酸铜铵 晶体,设计方案如下,下列说法
晶体,设计方案如下,下列说法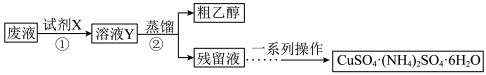
A.试剂X是硫酸,其中发生的反应之一: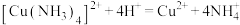 |
| B.步骤②蒸馏实验可用水浴加热 |
| C.若得到的粗乙醇中乙醇的含量明显偏低,可能是蒸馏时加热温度偏低 |
D.将残留液加热浓缩、冷却结晶可得到硫酸铜铵 晶体 晶体 |
您最近半年使用:0次
2024-05-01更新
|
294次组卷
|
3卷引用:2024届浙江省温州市高三下学期第二次适应性考试(二模)化学试题
名校
3 . 下列有关物质的分离或鉴别说法正确的是
| A.重结晶法提纯苯甲酸要用的仪器有:漏斗,烧杯,冷凝管 |
| B.分液操作时应先将下层液体从分液漏斗下口放出后再将上层液体继续放出 |
| C.酒精不能萃取水中的溶质,但是能萃取苯中的溶质 |
| D.原子光谱上的特征谱线,可用于元素鉴定 |
您最近半年使用:0次
2024-04-29更新
|
188次组卷
|
2卷引用:浙江省三锋联盟2023-2024学年高二下学期4月期中考试化学试题
名校
4 . 下列图示的实验装置,不能实现相应实验目的的是
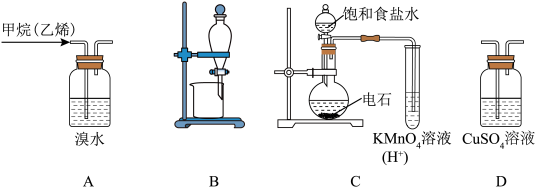
| A.图A:用溴水除去甲烷中的乙烯 |
| B.图B:分离苯和水的混合物 |
| C.图C:检验电石与饱和食盐水的产物乙炔 |
| D.图D:除去乙炔中的硫化氢 |
您最近半年使用:0次
2024-04-29更新
|
175次组卷
|
2卷引用:浙江省三锋联盟2023-2024学年高二下学期4月期中考试化学试题
5 . 为除去粗盐中的 、
、 、
、 、
、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量),有关说法正确的是
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量),有关说法正确的是
 、
、 、
、 、
、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量),有关说法正确的是
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量),有关说法正确的是
| A.步骤①:根据粗盐的质量和溶解度来确定烧杯和量筒的规格 |
B.步骤②~④: 、 、 和 和 的滴加“顺序”和“量”不可调整 的滴加“顺序”和“量”不可调整 |
C.步骤⑥:用玻璃棒搅拌滤液,直到没有气泡冒出,且 试纸检验滤液呈碱性 试纸检验滤液呈碱性 |
| D.步骤①~⑦:需要的实验用品有分液漏斗、蒸发皿、玻璃棒、陶土网和胶头滴管 |
您最近半年使用:0次
2024-04-29更新
|
233次组卷
|
2卷引用:浙江省丽水湖州衢州三地市2024届高三下学期4月教学质量检测化学试题
名校
解题方法
6 . 用 氧化甲苯制备苯甲酸。实验方法:将甲苯和
氧化甲苯制备苯甲酸。实验方法:将甲苯和 溶液在100℃反应一段时间后停止反应,过滤,将含有苯甲酸钾
溶液在100℃反应一段时间后停止反应,过滤,将含有苯甲酸钾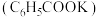 和甲苯的滤液按如下流程分离出苯甲酸和回收未反应的甲苯。
和甲苯的滤液按如下流程分离出苯甲酸和回收未反应的甲苯。
 氧化甲苯制备苯甲酸。实验方法:将甲苯和
氧化甲苯制备苯甲酸。实验方法:将甲苯和 溶液在100℃反应一段时间后停止反应,过滤,将含有苯甲酸钾
溶液在100℃反应一段时间后停止反应,过滤,将含有苯甲酸钾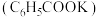 和甲苯的滤液按如下流程分离出苯甲酸和回收未反应的甲苯。
和甲苯的滤液按如下流程分离出苯甲酸和回收未反应的甲苯。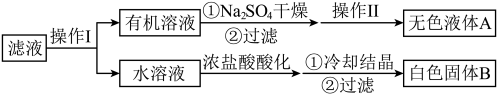
| A.操作I是分液,操作II是蒸馏 |
| B.无色液体A是甲苯,白色固体是B苯甲酸 |
| C.为了得到更多的白色固体B,冷却结晶时温度越低越好 |
D.浓盐酸的作用是:   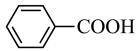  |
您最近半年使用:0次
名校
解题方法
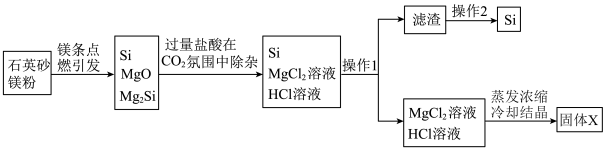
7 . 近日,清华大学等重点高校为解决中国“芯”——半导体芯片,成立了“芯片学院”。某小组拟在实验室制造硅,其流程如图:
除杂原理: ,
,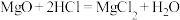
下列说法中正确的是

除杂原理:
 ,
,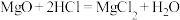
下列说法中正确的是
| A.操作1所需玻璃仪器仅为烧杯、漏斗 |
| B.操作2为重结晶 |
C.固体X为 ,可用于电解制Mg ,可用于电解制Mg |
D.点燃石英砂和镁粉的混合物发生的副反应为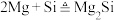 |
您最近半年使用:0次
名校
解题方法
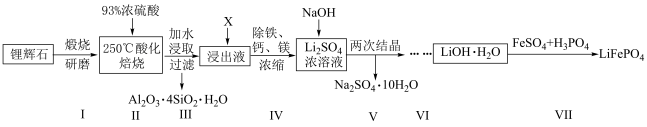
8 . 某课题组以锂辉石(主要成分为 ,还含有铁、钙、镁等元素)为原料,按下列流程制备
,还含有铁、钙、镁等元素)为原料,按下列流程制备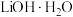 ,并制备锂离子电池正极材料
,并制备锂离子电池正极材料 。
。 不溶于水,能溶于强酸;
不溶于水,能溶于强酸;
② 晶体和
晶体和 晶体的溶解度随温度变化的曲线如图所示:
晶体的溶解度随温度变化的曲线如图所示:
(1)下列操作或描述不正确的是__________。
(2)步骤Ⅴ通过两次结晶,可得到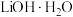 溶液和
溶液和 。需要用到下列操作:
。需要用到下列操作:
a.过滤; b.趁热过滤; c.冷却至0℃; d.用烧杯承接滤液;
e.在40℃时蒸发溶剂至溶液出现少量固体,停止加热;
f.在100℃时蒸发溶剂至溶液体积减小约原来一半,有固体析出,停止加热。
写出“两次结晶”的正确操作顺序_______ :____→____→d→____→____→____。
(3)在步骤Ⅶ,若将 和
和 的混合液滴加到
的混合液滴加到 溶液中,获得的产品纯度较低,请给出可能的原因:
溶液中,获得的产品纯度较低,请给出可能的原因:__________ 。
(4) 标准溶液浓度的测定:准确称取一定质量的硼砂
标准溶液浓度的测定:准确称取一定质量的硼砂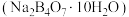 溶于水配成溶液,以如图装置测定
溶于水配成溶液,以如图装置测定 溶液的浓度。已知硼砂与
溶液的浓度。已知硼砂与 发生反应:
发生反应: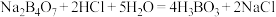 ,则锥形瓶内装入的溶液为
,则锥形瓶内装入的溶液为__________ ;若已知滴定终点pH为5.27,采用甲基橙作指示剂会导致 溶液浓度测定结果
溶液浓度测定结果__________ (填“偏高”、“偏低”或“无影响”)。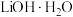 的质量分数(杂质主要为
的质量分数(杂质主要为 ,其他杂质不参与反应),取a g样品溶解,以酚酞为指示剂,用浓度为
,其他杂质不参与反应),取a g样品溶解,以酚酞为指示剂,用浓度为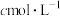 的标准
的标准 溶液滴定至溶液刚好褪色,消耗
溶液滴定至溶液刚好褪色,消耗 ,再加入甲基橙,继续用以上标准
,再加入甲基橙,继续用以上标准 溶液滴定至溶液刚好变色,又消耗
溶液滴定至溶液刚好变色,又消耗 。则样品中
。则样品中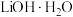 的质量分数为
的质量分数为__________ 。(已知: 溶液pH在8左右,且溶液的pH随浓度变化不大)
溶液pH在8左右,且溶液的pH随浓度变化不大)
 ,还含有铁、钙、镁等元素)为原料,按下列流程制备
,还含有铁、钙、镁等元素)为原料,按下列流程制备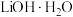 ,并制备锂离子电池正极材料
,并制备锂离子电池正极材料 。
。
 不溶于水,能溶于强酸;
不溶于水,能溶于强酸;②
 晶体和
晶体和 晶体的溶解度随温度变化的曲线如图所示:
晶体的溶解度随温度变化的曲线如图所示: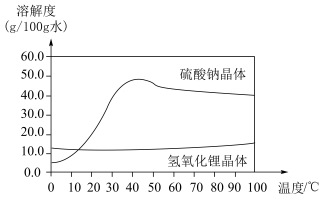
(1)下列操作或描述不正确的是__________。
A.步骤Ⅰ矿石研磨,可提高酸化焙烧效率,促进 的溶解 的溶解 |
B.步骤Ⅱ若减少浓硫酸用量,会导致 在步骤Ⅲ水解产生胶体吸附 在步骤Ⅲ水解产生胶体吸附 ,降低 ,降低 的浸出率 的浸出率 |
| C.模拟上述流程,步骤Ⅰ、Ⅲ所用的仪器有蒸发皿、烧杯、玻璃棒、耐酸过滤器及热源 |
D.步骤Ⅳ中加入的X可以是先加入 调节pH以除去 调节pH以除去 ,再加入 ,再加入 除尽 除尽 和 和 |
(2)步骤Ⅴ通过两次结晶,可得到
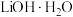 溶液和
溶液和 。需要用到下列操作:
。需要用到下列操作:a.过滤; b.趁热过滤; c.冷却至0℃; d.用烧杯承接滤液;
e.在40℃时蒸发溶剂至溶液出现少量固体,停止加热;
f.在100℃时蒸发溶剂至溶液体积减小约原来一半,有固体析出,停止加热。
写出“两次结晶”的正确操作顺序
(3)在步骤Ⅶ,若将
 和
和 的混合液滴加到
的混合液滴加到 溶液中,获得的产品纯度较低,请给出可能的原因:
溶液中,获得的产品纯度较低,请给出可能的原因:(4)
 标准溶液浓度的测定:准确称取一定质量的硼砂
标准溶液浓度的测定:准确称取一定质量的硼砂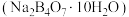 溶于水配成溶液,以如图装置测定
溶于水配成溶液,以如图装置测定 溶液的浓度。已知硼砂与
溶液的浓度。已知硼砂与 发生反应:
发生反应: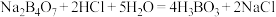 ,则锥形瓶内装入的溶液为
,则锥形瓶内装入的溶液为 溶液浓度测定结果
溶液浓度测定结果
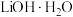 的质量分数(杂质主要为
的质量分数(杂质主要为 ,其他杂质不参与反应),取a g样品溶解,以酚酞为指示剂,用浓度为
,其他杂质不参与反应),取a g样品溶解,以酚酞为指示剂,用浓度为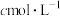 的标准
的标准 溶液滴定至溶液刚好褪色,消耗
溶液滴定至溶液刚好褪色,消耗 ,再加入甲基橙,继续用以上标准
,再加入甲基橙,继续用以上标准 溶液滴定至溶液刚好变色,又消耗
溶液滴定至溶液刚好变色,又消耗 。则样品中
。则样品中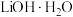 的质量分数为
的质量分数为 溶液pH在8左右,且溶液的pH随浓度变化不大)
溶液pH在8左右,且溶液的pH随浓度变化不大)
您最近半年使用:0次
名校
解题方法
9 . 下列实验装置使用不正确 的是
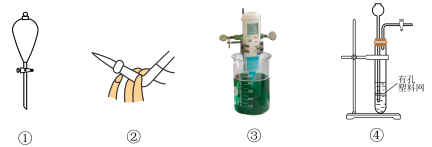
| A.图①装置可用于分离溴苯和水的混合物,且溴苯从下口放出 |
| B.可用图②方法排出碱式滴定管下端的气泡 |
| C.图③装置是用pH计测定溶液pH值,使用前pH计需洗涤和校正 |
| D.图④装置用于电石与水制取乙炔 |
您最近半年使用:0次
解题方法
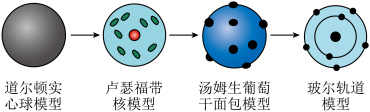
10 . 下列说法不正确的是
| A.侯德榜是我国著名化工专家,发明了侯氏制碱法 |
| B.舍勒发现了一种黄绿色气体,戴维确认该气体为氯气 |
| C.屠呦呦——从青蒿中提取青蒿素 |
| D.原子结构模型演变历史可以表示为如图 |
您最近半年使用:0次



