名校
解题方法
1 . 砷的化合物可用于半导体领域,如我国“天宫”空间站的核心舱“天和号”就是采用砷化镓薄膜电池来供电。一种从酸性高浓度含砷废水[砷主要以亚砷酸( )形式存在]中回收砷的工艺流程如下:
)形式存在]中回收砷的工艺流程如下:
Ⅱ.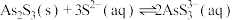
Ⅲ.砷酸( )在酸性条件下有强氧化性
)在酸性条件下有强氧化性
Ⅳ.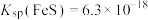 ,
,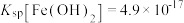
请回答:
(1)从含砷废水到滤液Ⅰ,浓度明显减小的阳离子为__________ (用离子符号表示)。
(2)下列说法正确的是__________。
(3)“沉砷”过程中 是否可用过量的
是否可用过量的 替换
替换__________ (填“是”或“否”);请从平衡移动的角度解释原因__________ 。
(4)砷酸“还原”过程中发生的化学方程式为__________ 。还原后溶液需检验是否仍剩余砷酸,设计检验实验方案__________ 。
 )形式存在]中回收砷的工艺流程如下:
)形式存在]中回收砷的工艺流程如下:

Ⅱ.
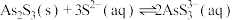
Ⅲ.砷酸(
 )在酸性条件下有强氧化性
)在酸性条件下有强氧化性Ⅳ.
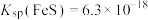 ,
,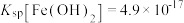
请回答:
(1)从含砷废水到滤液Ⅰ,浓度明显减小的阳离子为
(2)下列说法正确的是__________。
A.沉砷时产生的废气可用 溶液吸收处理 溶液吸收处理 |
B.酸化的目的是增加 价砷的氧化性 价砷的氧化性 |
C. 浸取后所得滤渣的主要成分是 浸取后所得滤渣的主要成分是 ,不含 ,不含 |
D.酸性: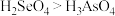 |
(3)“沉砷”过程中
 是否可用过量的
是否可用过量的 替换
替换(4)砷酸“还原”过程中发生的化学方程式为
您最近一年使用:0次
2 . 某实验小组为制备1-氯-2-甲基丙烷(沸点69℃),将2-甲基-1-丙醇和 溶于
溶于 中,加热回流(伴有
中,加热回流(伴有 气体产生)。反应完全后倒入冰水中分解残余的
气体产生)。反应完全后倒入冰水中分解残余的 ,分液收集
,分液收集 层,再用无水
层,再用无水 干燥,过滤、蒸馏后得到目标产物。上述过程中涉及的部分装置(夹持及加热装置略)如下图,下列说法
干燥,过滤、蒸馏后得到目标产物。上述过程中涉及的部分装置(夹持及加热装置略)如下图,下列说法不正确 的是
 溶于
溶于 中,加热回流(伴有
中,加热回流(伴有 气体产生)。反应完全后倒入冰水中分解残余的
气体产生)。反应完全后倒入冰水中分解残余的 ,分液收集
,分液收集 层,再用无水
层,再用无水 干燥,过滤、蒸馏后得到目标产物。上述过程中涉及的部分装置(夹持及加热装置略)如下图,下列说法
干燥,过滤、蒸馏后得到目标产物。上述过程中涉及的部分装置(夹持及加热装置略)如下图,下列说法
| A.装置①在加热回流时,需加入沸石或碎瓷片 |
B.装置②与装置①的冷凝管上端相连,因 气体极易溶于水,需将尾气处理装置设计成防倒吸 气体极易溶于水,需将尾气处理装置设计成防倒吸 |
| C.装置③在分液前无法区分水层与有机层时,可向分液漏斗中滴水,若上层无水滴通过轨迹,则上层为水层 |
D. 沸点为39.8℃,为增强冷凝效果,可使用装置④的蒸馏装置,对圆底烧瓶进行控制温度的温水浴加热 沸点为39.8℃,为增强冷凝效果,可使用装置④的蒸馏装置,对圆底烧瓶进行控制温度的温水浴加热 |
您最近一年使用:0次
名校
解题方法
3 . 为除去括号内少量的杂质,所用的试剂或方法正确的是
| A.Fe粉(Cu粉):盐酸,过滤 |
B. :氧气,点燃 :氧气,点燃 |
C.除去KCl溶液中的少量 :加入适量NaOH溶液,过滤 :加入适量NaOH溶液,过滤 |
D. :饱和碳酸氢钠溶液,洗气 :饱和碳酸氢钠溶液,洗气 |
您最近一年使用:0次
2024-03-20更新
|
350次组卷
|
3卷引用:浙江省杭州市长河高级中学2023-2024学年高一上学期期末考试化学试题
浙江省杭州市长河高级中学2023-2024学年高一上学期期末考试化学试题浙江省宁波市九校2023-2024学年高一上学期1月期末化学试题(已下线)专题01 硫及其化合物(考点清单)(讲+练)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)
2024高三下·全国·专题练习
4 . Cu元素在生命活动中占有举足轻重的地位,缺铜会造成贫血、记忆力减退、反应迟钝、运动失常等。设计如下实验制备有机补铜剂顺式甘氨酸合铜水合物并测定其组成。
查阅资料:
①制备反应为:
②该反应同时生成顺式产物(天蓝色针状)和反式产物(蓝紫色鳞片状),其反应进程如图所示:

制备有机补铜剂顺式甘氨酸合铜水合物实验过程为:


回答下列问题:
(1)步骤Ⅱ中控制反应温度为70℃的原因是___________ ,可采用的加热方式为___________ 。
(2)下列有关说法正确的是___________。
(3)用间接碘量法测定产物中Cu(Ⅱ)的质量分数。
已知:2Cu2++4I-=I2+2CuI↓ I2+2S2O =S4O
=S4O +2I-
+2I-
请选择以下正确的操作排序:
取2.0g所制备的产品,用稀硫酸溶解配成100mL溶液→a→___________ ,重复操作3次,消耗Na2S2O3标准液平均值为amL。
a.取25mL该溶液转移入锥形瓶
b.立即用酸式滴定管中0.01 molL-1Na2S2O3标准液快速进行滴定
c.立即用碱式滴定管中0.01 mol L-1Na2S2O3标准液快速进行滴定
d.当溶液变为浅黄色时,加入1mL淀粉溶液
e.加入蒸馏水和过量的KI溶液,得到棕黄色溶液
f.继续滴定至溶液蓝色恰好褪去
g.继续滴定至溶液由无色变为蓝色
根据实验数据,所得晶体中Cu(Ⅱ)质量分数为___________ ,若要提高产品的纯度,所用的实验方法名称是___________ 。
查阅资料:
①制备反应为:

②该反应同时生成顺式产物(天蓝色针状)和反式产物(蓝紫色鳞片状),其反应进程如图所示:

制备有机补铜剂顺式甘氨酸合铜水合物实验过程为:


回答下列问题:
(1)步骤Ⅱ中控制反应温度为70℃的原因是
(2)下列有关说法正确的是___________。
| A.CuSO4和NaOH快速生成的Cu(OH)2絮状沉淀易裹挟杂质,故不采用CuSO4和NaOH直接反应制备Cu(OH)2 |
| B.步骤Ⅲ中趁热过滤是为了防止杂质析出 |
| C.步骤Ⅳ加入95%的乙醇可以得到纯度更高的产品,说明顺式甘氨酸的极性大于反式甘氨酸 |
| D.步骤Ⅴ用25%酒精和丙酮分别洗涤晶体的目的是:25%酒精用于除去可溶性杂质(剩余反应物),丙酮用于除去晶体中残余的水 |
(3)用间接碘量法测定产物中Cu(Ⅱ)的质量分数。
已知:2Cu2++4I-=I2+2CuI↓ I2+2S2O
 =S4O
=S4O +2I-
+2I-请选择以下正确的操作排序:
取2.0g所制备的产品,用稀硫酸溶解配成100mL溶液→a→
a.取25mL该溶液转移入锥形瓶
b.立即用酸式滴定管中0.01 molL-1Na2S2O3标准液快速进行滴定
c.立即用碱式滴定管中0.01 mol L-1Na2S2O3标准液快速进行滴定
d.当溶液变为浅黄色时,加入1mL淀粉溶液
e.加入蒸馏水和过量的KI溶液,得到棕黄色溶液
f.继续滴定至溶液蓝色恰好褪去
g.继续滴定至溶液由无色变为蓝色
根据实验数据,所得晶体中Cu(Ⅱ)质量分数为
您最近一年使用:0次
名校
解题方法
5 . 下列有关物质的除杂所选试剂或方法不正确 的是
A.除去 固体中少量 固体中少量 :直接加热 :直接加热 |
B.除去 溶液中少量 溶液中少量 :过量铁粉,过滤 :过量铁粉,过滤 |
C.除去 气体中少量 气体中少量 :饱和食盐水、浓硫酸,洗气 :饱和食盐水、浓硫酸,洗气 |
D.除去 气体中少量 气体中少量 :过量 :过量 ,点燃 ,点燃 |
您最近一年使用:0次
2024-03-15更新
|
173次组卷
|
2卷引用:浙江省浙南名校2023-2024学年高一下学期开学化学试题
6 . 过滤操作过程中,不会 用到的仪器是
| A.烧杯 | B.烧瓶 | C.漏斗 | D.玻璃棒 |
您最近一年使用:0次
7 . 下列装置或操作能达到实验目的的是
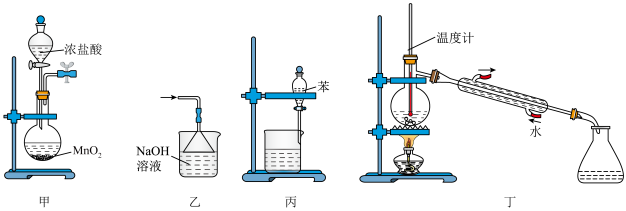

| A.用甲装置制取氯气 | B.用乙装置除去氯气中的HCl气体 |
| C.用丙装置分离苯和水 | D.用丁装置模拟海水淡化 |
您最近一年使用:0次
8 . 下列关于实验安全与事故的处理正确的是
| A.浓硫酸不慎沾到皮肤上,应立即用氢氧化钠溶液中和 |
| B.做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸 |
| C.所有用剩的药品都不能放回原瓶 |
| D.金属钠着火用泡沫灭火器灭火 |
您最近一年使用:0次
9 . 除去括号内杂质所用试剂和方法错误 的是
| A.CO2(HCl)——饱和碳酸氢钠溶液,洗气 |
| B.FeCl3溶液(FeCl2)——加入足量的铁粉,过滤 |
| C.Cl2(HCl)——饱和食盐水,洗气 |
| D.Cu(Fe)——溶于足量盐酸,过滤 |
您最近一年使用:0次
名校
解题方法
10 . 加热条件下,硅单质和 反应生成
反应生成 是粗硅提纯的重要步骤,某小组欲用以下装置完成上述转化(夹持装置略去)。
是粗硅提纯的重要步骤,某小组欲用以下装置完成上述转化(夹持装置略去)。

已知: 的沸点为33.0℃,易溶于有机溶剂,能与水剧烈反应,在空气中易被氧化,
的沸点为33.0℃,易溶于有机溶剂,能与水剧烈反应,在空气中易被氧化, 的沸点为76.8℃。
的沸点为76.8℃。
请回答下列问题:
(1)装置A中浓硫酸体现出的性质是______ 。
(2)g管的作用是______ 。
(3)从装置 所得的液体混合物分离得到
所得的液体混合物分离得到 的实验操作方法是
的实验操作方法是______ 。
(4)以上各个装置的组装顺序为
______ (部分装置可重复使用)。
(5) 在潮湿的空气中被氧化生成一种氧化物和一种无氧酸,该反应的化学方程式为
在潮湿的空气中被氧化生成一种氧化物和一种无氧酸,该反应的化学方程式为______ 。
 反应生成
反应生成 是粗硅提纯的重要步骤,某小组欲用以下装置完成上述转化(夹持装置略去)。
是粗硅提纯的重要步骤,某小组欲用以下装置完成上述转化(夹持装置略去)。
已知:
 的沸点为33.0℃,易溶于有机溶剂,能与水剧烈反应,在空气中易被氧化,
的沸点为33.0℃,易溶于有机溶剂,能与水剧烈反应,在空气中易被氧化, 的沸点为76.8℃。
的沸点为76.8℃。请回答下列问题:
(1)装置A中浓硫酸体现出的性质是
(2)g管的作用是
(3)从装置
 所得的液体混合物分离得到
所得的液体混合物分离得到 的实验操作方法是
的实验操作方法是(4)以上各个装置的组装顺序为

(5)
 在潮湿的空气中被氧化生成一种氧化物和一种无氧酸,该反应的化学方程式为
在潮湿的空气中被氧化生成一种氧化物和一种无氧酸,该反应的化学方程式为
您最近一年使用:0次



