解题方法
1 . 按要求填空
(1)向CuCl2溶液中滴加NaOH溶液,现象:_________ ,离子方程式:_____ ,
(2)向NaHCO3溶液中滴加稀硫酸,现象:_____ ,离子方程式:_______ ;
(3)铜粉(铁粉):除杂,括号内为杂质,所加试剂_____ ,离子方程式;_____ 。
(4)FeSO4 (CuSO4):除杂,括号内为杂质,所加试剂________ ,离子方程式__________ 。
(1)向CuCl2溶液中滴加NaOH溶液,现象:
(2)向NaHCO3溶液中滴加稀硫酸,现象:
(3)铜粉(铁粉):除杂,括号内为杂质,所加试剂
(4)FeSO4 (CuSO4):除杂,括号内为杂质,所加试剂
您最近一年使用:0次
2021-01-09更新
|
1981次组卷
|
5卷引用:河北省沧州市部分学校2021-2022学年高一下学期开年摸底考试联考化学试题
名校
2 . 二硫化钼(MoS2,难溶于水)具有良好的光、电性能,可由钼精矿(主要含MoS2,还含NiS、CaMoO4等)为原料经过如下过程制得。
(1)“浸取”。向钼精矿中加入NaOH溶液,再加入NaClO溶液,充分反应后的溶液中含有Na2MoO4、Na2SO4、NiSO4、NaCl。
①写出浸取时MoS2发生反应的离子方程式:_______ 。
②浸取后的滤渣中含CaMoO4。若浸取时向溶液中加入Na2CO3溶液,可提高浸出液中Mo元素的含量,原因是_______ 。
③浸取时,Mo元素的浸出率与时间的变化如图1所示。已知生成物对反应无影响,则反应3~4min时,Mo元素的浸出率迅速上升的原因是_______ 。

(2)“制硫代钼酸铵[(NH4)2MoS4,摩尔质量260g•mol-1]”。向浸出液中加入NH4NO3和HNO3,析出(NH4)2Mo4O13,将(NH4)2Mo4O13溶于水,向其中加入(NH4)2S溶液,可得(NH4)2MoS4,写出生成(NH4)2MoS4反应的化学方程式:________ 。
(3)“制MoS2”。(NH4)2MoS4可通过如下两种方法制取MoS2:
方法一:将(NH4)2MoS4在一定条件下加热,可分解得到MoS2、NH3、H2S和硫单质。其中NH3、H2S和硫单质的物质的量之比为8:4:1。
方法二:将(NH4)2MoS4在空气中加热可得MoS2,加热时所得剩余固体的质量与原始固体质量的比值与温度的关系如图2所示。
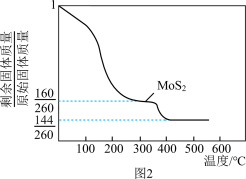
①方法一中,所得硫单质的分子式为_______ 。
②方法二中,500℃可得到Mo的一种氧化物,该氧化物的化学式为_______ 。
(1)“浸取”。向钼精矿中加入NaOH溶液,再加入NaClO溶液,充分反应后的溶液中含有Na2MoO4、Na2SO4、NiSO4、NaCl。
①写出浸取时MoS2发生反应的离子方程式:
②浸取后的滤渣中含CaMoO4。若浸取时向溶液中加入Na2CO3溶液,可提高浸出液中Mo元素的含量,原因是
③浸取时,Mo元素的浸出率与时间的变化如图1所示。已知生成物对反应无影响,则反应3~4min时,Mo元素的浸出率迅速上升的原因是

(2)“制硫代钼酸铵[(NH4)2MoS4,摩尔质量260g•mol-1]”。向浸出液中加入NH4NO3和HNO3,析出(NH4)2Mo4O13,将(NH4)2Mo4O13溶于水,向其中加入(NH4)2S溶液,可得(NH4)2MoS4,写出生成(NH4)2MoS4反应的化学方程式:
(3)“制MoS2”。(NH4)2MoS4可通过如下两种方法制取MoS2:
方法一:将(NH4)2MoS4在一定条件下加热,可分解得到MoS2、NH3、H2S和硫单质。其中NH3、H2S和硫单质的物质的量之比为8:4:1。
方法二:将(NH4)2MoS4在空气中加热可得MoS2,加热时所得剩余固体的质量与原始固体质量的比值与温度的关系如图2所示。

①方法一中,所得硫单质的分子式为
②方法二中,500℃可得到Mo的一种氧化物,该氧化物的化学式为
您最近一年使用:0次
2023-05-29更新
|
500次组卷
|
3卷引用:江苏省常州高级中学2023-2024学年高三上学期开学考试化学试题
3 . 海洋是一个巨大的宝藏,海水淡化是重要的化学研究课题。
(1)蒸馏法获取淡水,历史悠久,操作简单,图中符合模拟蒸馏海水的装置是___ (填序号)。
a.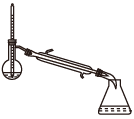 b.
b.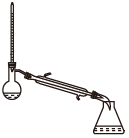
c.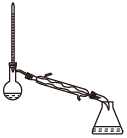 d.
d.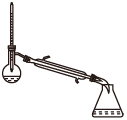
蒸馏前,应向烧瓶中加入沸石或碎瓷片,目的是___ ,冷凝水一般不采用“上进下出”,其原因是____ 。
(2)电渗析法的技术原理如图(两端为惰性电极,阳膜只允许阳离子通过,阴膜只允许阴离子通过):
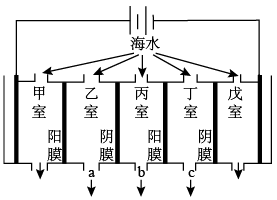
某地海水中主要含Na+、K+、Ca2+、Mg2+、Cl-、HCO 、SO
、SO 等,则淡化过程中,甲室的电极反应式为
等,则淡化过程中,甲室的电极反应式为___ ,产生水垢最多的是___ 室,淡水的出口为____ (填“a”、“b”或“c”)。
(3)离子交换法获取淡水模拟图如图:

经过阳离子交换树脂后水中阳离子数目____ (填“增加”“不变”或“减少”),阴离子交换树脂中发生了离子反应,其离子方程式为___ 。
(1)蒸馏法获取淡水,历史悠久,操作简单,图中符合模拟蒸馏海水的装置是
a.
 b.
b.
c.
 d.
d.
蒸馏前,应向烧瓶中加入沸石或碎瓷片,目的是
(2)电渗析法的技术原理如图(两端为惰性电极,阳膜只允许阳离子通过,阴膜只允许阴离子通过):

某地海水中主要含Na+、K+、Ca2+、Mg2+、Cl-、HCO
 、SO
、SO 等,则淡化过程中,甲室的电极反应式为
等,则淡化过程中,甲室的电极反应式为(3)离子交换法获取淡水模拟图如图:

经过阳离子交换树脂后水中阳离子数目
您最近一年使用:0次
2021-09-06更新
|
1253次组卷
|
5卷引用:安徽省A10联盟2022届高三上学期摸底考试化学试题
安徽省A10联盟2022届高三上学期摸底考试化学试题(已下线)3.3.1 粗盐提纯 从海水中提取溴-2021-2022学年高一化学课后培优练(苏教版2019必修第一册)(已下线)专题35 物质的检验、分离和提纯(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练(已下线)第八章 化学与可持续发展(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)(已下线)第八章 化学与可持续发展【单元测试B卷】
名校
4 . 含钠化合物在工业生产和日常生活中应用广泛,请回答下列有关问题:
(1)钠元素的碱性氧化物的化学式为___________ ,钠另一种氧化物是一种淡黄色固体,写出其用于呼吸面具供氧剂的一个化学方程式:___________ 。
(2) 是一种强碱,若实验室用
是一种强碱,若实验室用 浓溶液配制
浓溶液配制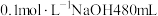 ,需量取密度为
,需量取密度为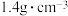 质量分数为
质量分数为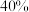 的
的 溶液
溶液___________  ,该实验所需的玻璃仪器除玻璃棒、量筒、胶头滴管之外,还有
,该实验所需的玻璃仪器除玻璃棒、量筒、胶头滴管之外,还有___________ ,当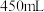 所配溶液与标准状况下
所配溶液与标准状况下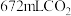 恰好反应时,发生反应的离子方程式为
恰好反应时,发生反应的离子方程式为___________ 。
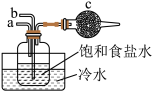
(3)如图是实验室模拟“侯氏制碱法”制取 的部分装置。下列说正确的是___________(填序号)
的部分装置。下列说正确的是___________(填序号)
(4)粗盐常含有少量 、
、 、
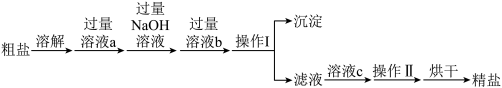
、 以及泥沙等杂质,实验室中可用如下流程提纯
以及泥沙等杂质,实验室中可用如下流程提纯 ,下列说法中正确的是___________(填序号)
,下列说法中正确的是___________(填序号)
(1)钠元素的碱性氧化物的化学式为
(2)
 是一种强碱,若实验室用
是一种强碱,若实验室用 浓溶液配制
浓溶液配制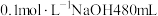 ,需量取密度为
,需量取密度为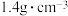 质量分数为
质量分数为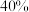 的
的 溶液
溶液 ,该实验所需的玻璃仪器除玻璃棒、量筒、胶头滴管之外,还有
,该实验所需的玻璃仪器除玻璃棒、量筒、胶头滴管之外,还有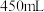 所配溶液与标准状况下
所配溶液与标准状况下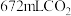 恰好反应时,发生反应的离子方程式为
恰好反应时,发生反应的离子方程式为(3)如图是实验室模拟“侯氏制碱法”制取
 的部分装置。下列说正确的是___________(填序号)
的部分装置。下列说正确的是___________(填序号)
A.a先通入 ,然后b通入 ,然后b通入 ,c中放碱石灰 ,c中放碱石灰 |
B.b先通入 ,然后a通入 ,然后a通入 ,c中放碱石灰 ,c中放碱石灰 |
C.a先通入 ,然后b通入 ,然后b通入 ,c中放蘸稀硫酸的脱脂棉 ,c中放蘸稀硫酸的脱脂棉 |
D.b先通入 ,然后a通入 ,然后a通入 ,c中放蘸稀硫酸的脱脂棉 ,c中放蘸稀硫酸的脱脂棉 |
 、
、 、
、 以及泥沙等杂质,实验室中可用如下流程提纯
以及泥沙等杂质,实验室中可用如下流程提纯 ,下列说法中正确的是___________(填序号)
,下列说法中正确的是___________(填序号)
A.溶液a和 可用一种试剂来代替 可用一种试剂来代替 |
| B.溶液a和溶液b的添加顺序可以互换 |
| C.操作Ⅱ为蒸发结晶,蒸发过程中当蒸发皿中有大量晶体析出时停止加热 |
| D.粗盐提纯的整个操作过程中共有两处需要使用玻璃棒 |
您最近一年使用:0次
2023-02-12更新
|
392次组卷
|
3卷引用:山东省德州市2022-2023学年高一下学期开学考试化学试题
名校
解题方法
5 . 现有 NaCl、Na2SO4和 NaNO3 的混合物,选择适当的试剂除去杂质,从而得到纯净的NaNO3晶体,相应的实验流程如图所示。

(1)写出实验流程中下列物质的化学式:试剂 X___________ ,沉淀 A_________ 。
(2)上述实验流程中①②③步均要进行的实验操作是______________ (填操作名称),该过程中玻璃棒的作用是___________ 。
(3)上述实验流程中加入过量 Na2CO3 溶液的目的是_____________ 。
(4)按此实验方案得到的溶液3中肯定含有_________________ (填化学式)杂质。为了解决这个问题,可以向溶液3中加入适量的_________________ (填化学式)。

(1)写出实验流程中下列物质的化学式:试剂 X
(2)上述实验流程中①②③步均要进行的实验操作是
(3)上述实验流程中加入过量 Na2CO3 溶液的目的是
(4)按此实验方案得到的溶液3中肯定含有
您最近一年使用:0次
2020-06-12更新
|
1360次组卷
|
8卷引用:河北省沧州市盐山中学2023-2024学年高一下学期开学化学试题
河北省沧州市盐山中学2023-2024学年高一下学期开学化学试题江苏省江都中学2019-2020学年度高一期中考试化学试题(已下线)第二章 化学物质及其变化(基础过关)-2020-2021学年高一化学单元测试定心卷(人教版必修1)(已下线)第一章 物质及其变化(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版2019必修第一册)安徽省六安市新安中学2022届高三上学期第二次月考化学试题(已下线)【苏州新东方】13 吴江区 高级中学江苏省宿迁市泗阳县实验高级中学2022-2023学年高一上学期第一次调研测试化学试题(已下线)第一章 化学物质及其变化 第3练 离子反应的应用
名校
6 . 我国是世界产盐大国,海盐、湖盐和井盐的总产量居世界第二位。某同学进行粗盐的提纯并配制溶液、检验纯度实验。
(一)粗盐的提纯
(1)粗盐中含有泥沙、Ca2+、Mg2+、SO 杂质,请选择合适的操作补全实验流程。
杂质,请选择合适的操作补全实验流程。_______
将粗盐溶解→加入NaOH溶液→___________→___________→___________→___________→结晶得到精盐
加入稀盐酸 B.加入稀硫酸 C.过滤 D.加入BaCl2溶液 E.加入Na2CO3溶液
(2)以上流程中加酸的目的是(用离子方程式表示)___________
(二)一定浓度溶液的配制:用制得的精盐配制100 mL 1.00 mol/L NaCl溶液
(3)实验中用到的玻璃仪器,除了烧杯、量筒、胶头滴管外,还需要___________
(4)定容时的操作:当液面离容量瓶刻度线1~2cm时,___________ ,再将容量瓶塞盖好,反复上下颠倒,摇匀。
(5)下列操作会使配得的NaCl溶液浓度偏低的是___________。
(三)纯度测定
取25.00mL所配溶液于锥形瓶中,加入几滴K2CrO4溶液(指示反应终点),在不断摇动下,滴加1.00mol/L AgNO3溶液反应。平行测试3次,平均消耗AgNO3溶液23.50mL。
(6)制得的NaCl的纯度是___________ 。
(一)粗盐的提纯
(1)粗盐中含有泥沙、Ca2+、Mg2+、SO
 杂质,请选择合适的操作补全实验流程。
杂质,请选择合适的操作补全实验流程。将粗盐溶解→加入NaOH溶液→___________→___________→___________→___________→结晶得到精盐
加入稀盐酸 B.加入稀硫酸 C.过滤 D.加入BaCl2溶液 E.加入Na2CO3溶液
(2)以上流程中加酸的目的是(用离子方程式表示)
(二)一定浓度溶液的配制:用制得的精盐配制100 mL 1.00 mol/L NaCl溶液
(3)实验中用到的玻璃仪器,除了烧杯、量筒、胶头滴管外,还需要
(4)定容时的操作:当液面离容量瓶刻度线1~2cm时,
(5)下列操作会使配得的NaCl溶液浓度偏低的是___________。
| A.没有进行洗涤操作 |
| B.定容时俯视容量瓶的刻度线 |
| C.摇匀后发现液面低于容量瓶刻度线,再滴加蒸馏水至刻度线 |
| D.转移洗涤液时洒到容量瓶外,继续用该未清洗的容量瓶重新配制 |
(三)纯度测定
取25.00mL所配溶液于锥形瓶中,加入几滴K2CrO4溶液(指示反应终点),在不断摇动下,滴加1.00mol/L AgNO3溶液反应。平行测试3次,平均消耗AgNO3溶液23.50mL。
(6)制得的NaCl的纯度是
您最近一年使用:0次
2023-11-17更新
|
173次组卷
|
5卷引用:北京市首都师范大学附属中学2023-2024学年高一下学期开学化学试题
7 . 航天员王亚平在“天宫课堂”中介绍了空间站中的生活,在轨演示了水球变气球等一系列炫酷又好玩的实验。
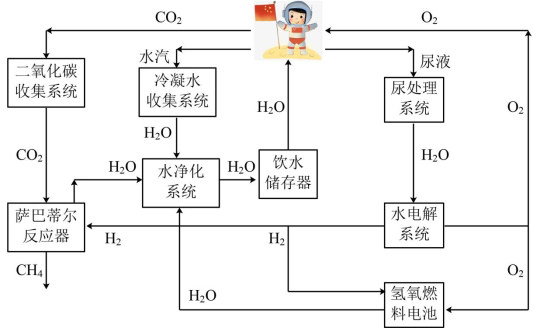
I.“天宫”中水和氧气的最大化利用是保障生活的重要措施。如图是空间站常用资源再利用模拟图。
(1)“尿处理子系统”采用蒸馏方法对其中成分进行分离。此方法是根据尿液中各成分的____ 不同进行分离的。
(2)“水电解系统”中产生氧气的电极应接电池的____ 极(填“正”或“负”)。发生反应的化学方程式为____ 。
(3)在水净化系统中,用臭氧(O3)消毒,臭氧在一定条件下转化为氧气的化学方程式为____ 。
(4)在一定条件下,“萨巴蒂尔反应器”可以除去CO2,该反应的化学方程式为____ 。
II.王亚平将蓝色颜料注入水球中,整个水球变成蓝色,将泡腾片放入水球中,产生大量气泡向四面八方扩散,充满整个水球。气体并不溢出,使水球越来越大。
(5)泡腾片在水中发生了如下反应:H3C6H5O7+3NaHCO3=Na3C6H5O7+3H2O+3____ (补全化学方程式)。
(6)如果在空间站失重状态下收集制得的氧气,可以选用下列装置中的____ (填序号)。
I.“天宫”中水和氧气的最大化利用是保障生活的重要措施。如图是空间站常用资源再利用模拟图。

(1)“尿处理子系统”采用蒸馏方法对其中成分进行分离。此方法是根据尿液中各成分的
(2)“水电解系统”中产生氧气的电极应接电池的
(3)在水净化系统中,用臭氧(O3)消毒,臭氧在一定条件下转化为氧气的化学方程式为
(4)在一定条件下,“萨巴蒂尔反应器”可以除去CO2,该反应的化学方程式为
II.王亚平将蓝色颜料注入水球中,整个水球变成蓝色,将泡腾片放入水球中,产生大量气泡向四面八方扩散,充满整个水球。气体并不溢出,使水球越来越大。
(5)泡腾片在水中发生了如下反应:H3C6H5O7+3NaHCO3=Na3C6H5O7+3H2O+3
(6)如果在空间站失重状态下收集制得的氧气,可以选用下列装置中的
A. | B. | C.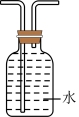 | D. |
您最近一年使用:0次
2022-08-22更新
|
375次组卷
|
3卷引用:福建省龙岩第一中学2022-2023学年高一上学期开学考试化学试题
真题
名校
8 . 用含有A1203、SiO2和少量FeO·xFe2O3的铝灰制备A12(SO4)3·18H2O。,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
(1)H2SO4溶解A12O3的离子方程式是_______________ 1;
(2)KMnO4-氧化Fe2+的离子方程式补充完整:______
 1MnO
1MnO +
+ Fe2++
Fe2++ ______=
______= Mn2++
Mn2++ Fe3++
Fe3++ ______
______
(3)已知:
生成氢氧化物沉淀的pH
注:金属离子的起始浓度为0.1mol·L-1
根据表中数据解释步骤Ⅱ的目的:._________________ ;
(4)已知:一定条件下,MnO 可与Mn2+反应生成MnO2,
可与Mn2+反应生成MnO2,
①向Ⅲ的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是_____________ ;
②Ⅳ中加入MnSO4的目的是:______________ ;
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
(1)H2SO4溶解A12O3的离子方程式是
(2)KMnO4-氧化Fe2+的离子方程式补充完整:
 1MnO
1MnO +
+ Fe2++
Fe2++ ______=
______= Mn2++
Mn2++ Fe3++
Fe3++ ______
______(3)已知:
生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
根据表中数据解释步骤Ⅱ的目的:.
(4)已知:一定条件下,MnO
 可与Mn2+反应生成MnO2,
可与Mn2+反应生成MnO2,①向Ⅲ的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是
②Ⅳ中加入MnSO4的目的是:
您最近一年使用:0次
2019-01-30更新
|
1889次组卷
|
4卷引用:吉林省长春外国语学校2020-2021学年高一下学期期初考试化学试题
吉林省长春外国语学校2020-2021学年高一下学期期初考试化学试题2013年全国普通高等学校招生统一考试理科综合能力测试化学(北京卷)(已下线)2014届高考化学二轮复习四川配套训练 第10讲金属元素化合物练习卷河南省范县第一中学2021-2022学年高一上学期第三次月考检测化学试题
9 . Ⅰ.“价类”二维图是学习元素及其化合物的重要工具.如图所示是铁及其化合物的“价类”二维图。__________ 、__________ ;Z在空气中转化为W的化学方程式为__________ 。
(2)含重铬酸根离子 的工业废水有毒,必须经过处理达标后才能排放。工业上常用绿矾
的工业废水有毒,必须经过处理达标后才能排放。工业上常用绿矾 作处理剂,发生反应的离子方程式为
作处理剂,发生反应的离子方程式为 ,则该反应中还原性:
,则该反应中还原性:
______ (填“>”或“<”) 。该反应中,每生成
。该反应中,每生成 ,消耗
,消耗 的质量为
的质量为__________ g。
Ⅱ.硫酸亚铁晶体 在医药上作补血剂。某课外小组取10片补血剂总质量w g,通过一系列反应转变为
在医药上作补血剂。某课外小组取10片补血剂总质量w g,通过一系列反应转变为 来测定该补血剂中铁元素的含量。实验步骤如下:
来测定该补血剂中铁元素的含量。实验步骤如下:
(3)某同学发现部分补血剂药片表面发黄,怀疑该补铁剂已经变质,遂取少量步骤①的滤液,滴加__________ 后,溶液变为红色,证实了怀疑。
(4)步骤②反应的离子方程式为__________ ,下列物质中可以用来代替该步骤中的 是
是__________ (填序号)。
① 溶液 ②氯水 ③稀盐酸 ④碳酸钠
溶液 ②氯水 ③稀盐酸 ④碳酸钠
(5)服用维生素C可使食物中的 转化为
转化为 ,从而实现科学补铁,在这个过程中体现出维生素C的
,从而实现科学补铁,在这个过程中体现出维生素C的__________ 性。假设实验中的损耗忽略不计,则该补血剂含铁元素的质量分数为__________ 。

(2)含重铬酸根离子
 的工业废水有毒,必须经过处理达标后才能排放。工业上常用绿矾
的工业废水有毒,必须经过处理达标后才能排放。工业上常用绿矾 作处理剂,发生反应的离子方程式为
作处理剂,发生反应的离子方程式为 ,则该反应中还原性:
,则该反应中还原性:
 。该反应中,每生成
。该反应中,每生成 ,消耗
,消耗 的质量为
的质量为Ⅱ.硫酸亚铁晶体
 在医药上作补血剂。某课外小组取10片补血剂总质量w g,通过一系列反应转变为
在医药上作补血剂。某课外小组取10片补血剂总质量w g,通过一系列反应转变为 来测定该补血剂中铁元素的含量。实验步骤如下:
来测定该补血剂中铁元素的含量。实验步骤如下:
(3)某同学发现部分补血剂药片表面发黄,怀疑该补铁剂已经变质,遂取少量步骤①的滤液,滴加
(4)步骤②反应的离子方程式为
 是
是①
 溶液 ②氯水 ③稀盐酸 ④碳酸钠
溶液 ②氯水 ③稀盐酸 ④碳酸钠(5)服用维生素C可使食物中的
 转化为
转化为 ,从而实现科学补铁,在这个过程中体现出维生素C的
,从而实现科学补铁,在这个过程中体现出维生素C的
您最近一年使用:0次
2024-01-24更新
|
143次组卷
|
2卷引用:四川省广元市川师大万达中学2023-2024学年高一下学期入学考试化学试题
名校
10 . 自古至今,铁及其化合物在人类生产生活中的使用发挥了巨大的作用。
(1)四大发明之一的司南是由天然磁石制成的,其主要成分是___________ (填化学式) 。
(2)由于Fe(OH)2易被氧化,所以制备时常隔绝空气制备,写出Fe(OH)2露置在空气中被氧化的化学方程式___________ 。
(3)某工业废渣wg (主要含二氧化硅、氧化铁、氧化镁)中提取氧化铁的工业流程如图(部分操作和条件略):
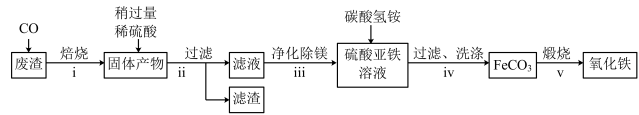
提示:二氧化硅不溶于稀硫酸。
①验证硫酸亚铁溶液中是否存在Fe3+的常用的试剂是___________ (填化学式)。
②步骤Ⅴ中,发生反应的化学方程式为___________ 。
③若提取过程中铁元素的损耗忽略不计,最终获得n g的氧化铁。则废渣中铁元素的质量分数为___________ 。
(1)四大发明之一的司南是由天然磁石制成的,其主要成分是
(2)由于Fe(OH)2易被氧化,所以制备时常隔绝空气制备,写出Fe(OH)2露置在空气中被氧化的化学方程式
(3)某工业废渣wg (主要含二氧化硅、氧化铁、氧化镁)中提取氧化铁的工业流程如图(部分操作和条件略):

提示:二氧化硅不溶于稀硫酸。
①验证硫酸亚铁溶液中是否存在Fe3+的常用的试剂是
②步骤Ⅴ中,发生反应的化学方程式为
③若提取过程中铁元素的损耗忽略不计,最终获得n g的氧化铁。则废渣中铁元素的质量分数为
您最近一年使用:0次
2023-07-10更新
|
306次组卷
|
2卷引用:江西省宁冈中学2023-2024学年高二上学期开学考试化学试题



