1 . 钴基变形高温合金是指含钴40%~70%的铸造合金,具有较好的抗氧化和抗热腐蚀性。制备某钴基变形高温合金的废料中主要含有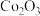 ,还含有少量
,还含有少量 、
、 及铝、镁、钙等金属元素的氧化物。用该废料采用酸溶法回收
及铝、镁、钙等金属元素的氧化物。用该废料采用酸溶法回收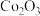 的工业流程如图所示。
的工业流程如图所示。 、
、 、
、 、
、 、
、 、
、 等。
等。
②部分阳离子以氢氧化物形式开始沉淀和沉淀完全(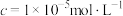 )时的pH见下表。
)时的pH见下表。
(1)“溶浸”前,通常需要将合金废料粉碎,这样做的目的是___________ 。“溶浸”时加入 的作用是
的作用是___________ 。
(2)“滤液1”中加入 溶液的作用是
溶液的作用是___________ (用离子方程式表示)。得到“滤渣2”时需要加 溶液调节溶液的
溶液调节溶液的 范围是
范围是___________ 。
(3)已知:25℃时, 、
、 。向“滤液2”中加入
。向“滤液2”中加入 溶液的目的是将溶液中的
溶液的目的是将溶液中的 与
与 转化为氮化物沉淀。如果“滤液2”中的
转化为氮化物沉淀。如果“滤液2”中的 ,则开始滴加
,则开始滴加 溶液时,首先析出的沉淀是
溶液时,首先析出的沉淀是___________ (填化学式),已知当加入过量 溶液后,所得滤液中
溶液后,所得滤液中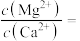
___________ 。
(4) 在空气中充分煅烧,除得到产品外,还生成了
在空气中充分煅烧,除得到产品外,还生成了 ,写出该反应的化学方程式:
,写出该反应的化学方程式:___________ 。
(5)若将草酸铵溶液换为碳酸氢钠溶液,可将 转化为
转化为 沉淀,反应的离子方程式为
沉淀,反应的离子方程式为___________ 。
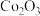 ,还含有少量
,还含有少量 、
、 及铝、镁、钙等金属元素的氧化物。用该废料采用酸溶法回收
及铝、镁、钙等金属元素的氧化物。用该废料采用酸溶法回收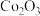 的工业流程如图所示。
的工业流程如图所示。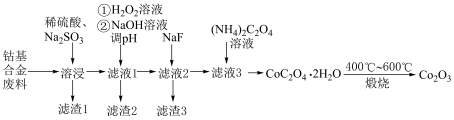
 、
、 、
、 、
、 、
、 、
、 等。
等。②部分阳离子以氢氧化物形式开始沉淀和沉淀完全(
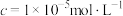 )时的pH见下表。
)时的pH见下表。| 沉淀物 |  |  |  |  |  |
| 开始沉淀时的pH | 6.6 | 7.6 | 2.7 | 3.4 | 9.2 |
| 沉淀完全时的pH | 9.2 | 9.6 | 3.2 | 4.7 | 11.1 |
(1)“溶浸”前,通常需要将合金废料粉碎,这样做的目的是
 的作用是
的作用是(2)“滤液1”中加入
 溶液的作用是
溶液的作用是 溶液调节溶液的
溶液调节溶液的 范围是
范围是(3)已知:25℃时,
 、
、 。向“滤液2”中加入
。向“滤液2”中加入 溶液的目的是将溶液中的
溶液的目的是将溶液中的 与
与 转化为氮化物沉淀。如果“滤液2”中的
转化为氮化物沉淀。如果“滤液2”中的 ,则开始滴加
,则开始滴加 溶液时,首先析出的沉淀是
溶液时,首先析出的沉淀是 溶液后,所得滤液中
溶液后,所得滤液中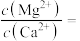
(4)
 在空气中充分煅烧,除得到产品外,还生成了
在空气中充分煅烧,除得到产品外,还生成了 ,写出该反应的化学方程式:
,写出该反应的化学方程式:(5)若将草酸铵溶液换为碳酸氢钠溶液,可将
 转化为
转化为 沉淀,反应的离子方程式为
沉淀,反应的离子方程式为
您最近一年使用:0次
解题方法
2 . 铍是航天航空、火箭导弹和原子能工业不可替代的材料,有“超级金属”之称。某厂以硅铍石(主要含有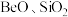 ,还有少量
,还有少量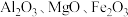 )为原料提取铍,具体流程如图。
)为原料提取铍,具体流程如图。 为两性氢氧化物,在强碱溶液中以
为两性氢氧化物,在强碱溶液中以 的形式存在;
的形式存在;
②氯化铍在熔融态时较难电离;
③ 为离子化合物,熔点为
为离子化合物,熔点为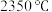 ,等物质的量的
,等物质的量的 和
和 的固体混合物在
的固体混合物在 即可熔化;
即可熔化;
④不同金属离子在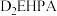 中的溶解性如表所示:
中的溶解性如表所示:
(1)“滤渣”的主要成分为_______ (填化学式)。
(2)“萃取分液”除去的离子主要是_______ 。若铍的萃取按如下反应式进行: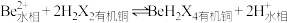 ,则“反萃取”时要加入足量
,则“反萃取”时要加入足量 溶液,发生的主要反应的化学方程式为
溶液,发生的主要反应的化学方程式为_______ 。
(3)“煮沸”时,发生反应的离子方程式为_______ 。
(4)写出高温条件下“转化”的化学方程式:_______ 。
(5)“电解”制铍时,加入与 等物质的量的
等物质的量的 的作用是
的作用是_______ ,不用电解 的方法制金属铍的原因是
的方法制金属铍的原因是_______ 。
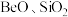 ,还有少量
,还有少量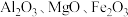 )为原料提取铍,具体流程如图。
)为原料提取铍,具体流程如图。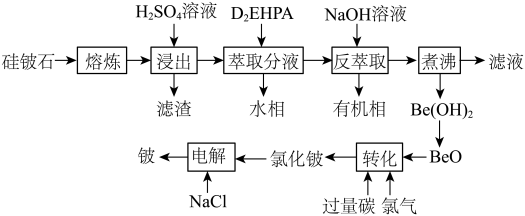
 为两性氢氧化物,在强碱溶液中以
为两性氢氧化物,在强碱溶液中以 的形式存在;
的形式存在;②氯化铍在熔融态时较难电离;
③
 为离子化合物,熔点为
为离子化合物,熔点为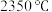 ,等物质的量的
,等物质的量的 和
和 的固体混合物在
的固体混合物在 即可熔化;
即可熔化;④不同金属离子在
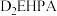 中的溶解性如表所示:
中的溶解性如表所示:金属离子 |
|
|
|
|
| 易溶 | 难溶 | 微溶 | 微溶 |
(1)“滤渣”的主要成分为
(2)“萃取分液”除去的离子主要是
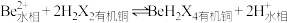 ,则“反萃取”时要加入足量
,则“反萃取”时要加入足量 溶液,发生的主要反应的化学方程式为
溶液,发生的主要反应的化学方程式为(3)“煮沸”时,发生反应的离子方程式为
(4)写出高温条件下“转化”的化学方程式:
(5)“电解”制铍时,加入与
 等物质的量的
等物质的量的 的作用是
的作用是 的方法制金属铍的原因是
的方法制金属铍的原因是
您最近一年使用:0次
解题方法
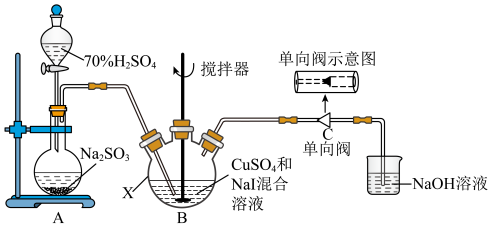
3 . 碘化亚铜(CuI)可用作有机合成催化剂,是一种白色粉末,不溶于水,在空气中相对稳定。实验室制备碘化亚铜的装置如图(部分夹持及加热装置已略去):
I.取50.0g 、80.0gNaI于仪器X中,加入适量蒸馏水溶解,搅拌,得到黄色沉淀;
、80.0gNaI于仪器X中,加入适量蒸馏水溶解,搅拌,得到黄色沉淀;
Ⅱ.打开分液漏斗,将A中产生的 通向B中的黄色沉淀,充分反应后得到白色沉淀;
通向B中的黄色沉淀,充分反应后得到白色沉淀;
Ⅲ.将分离出的白色沉淀经过“系列操作”得到19.1g产品;
Ⅳ.测定产品中CuI的纯度。
回答下列问题:
(1)在使用分液漏斗组装发生装置之前,必需进行的操作是___________ 。仪器X的名称是___________ 。
(2)已知步骤I中的黄色沉淀含CuI和一种单质,制备CuI的化学方程式为___________ 。
(3)步骤Ⅱ通入 的主要目的是
的主要目的是___________ 。写出通入 所发生的离子反应方程式
所发生的离子反应方程式___________ 。
(4)下图中能起到与单向阀C相同作用的是___________ (填字母)。(下图容器中未标注的液体均为氢氧化钠溶液) 浓度在一定范围内的关系如图。取0.1mgCuI粗产品,经预处理,将其中Cu元素全部转化为
浓度在一定范围内的关系如图。取0.1mgCuI粗产品,经预处理,将其中Cu元素全部转化为 并定容至1L。取样1mL测得荧光强度比值为10.7,则产品中CuI的纯度为
并定容至1L。取样1mL测得荧光强度比值为10.7,则产品中CuI的纯度为___________ %,据此推算CuI的产率接近于___________ (填字母)。
I.取50.0g
 、80.0gNaI于仪器X中,加入适量蒸馏水溶解,搅拌,得到黄色沉淀;
、80.0gNaI于仪器X中,加入适量蒸馏水溶解,搅拌,得到黄色沉淀;Ⅱ.打开分液漏斗,将A中产生的
 通向B中的黄色沉淀,充分反应后得到白色沉淀;
通向B中的黄色沉淀,充分反应后得到白色沉淀;Ⅲ.将分离出的白色沉淀经过“系列操作”得到19.1g产品;
Ⅳ.测定产品中CuI的纯度。
回答下列问题:
(1)在使用分液漏斗组装发生装置之前,必需进行的操作是
(2)已知步骤I中的黄色沉淀含CuI和一种单质,制备CuI的化学方程式为
(3)步骤Ⅱ通入
 的主要目的是
的主要目的是 所发生的离子反应方程式
所发生的离子反应方程式(4)下图中能起到与单向阀C相同作用的是

 浓度在一定范围内的关系如图。取0.1mgCuI粗产品,经预处理,将其中Cu元素全部转化为
浓度在一定范围内的关系如图。取0.1mgCuI粗产品,经预处理,将其中Cu元素全部转化为 并定容至1L。取样1mL测得荧光强度比值为10.7,则产品中CuI的纯度为
并定容至1L。取样1mL测得荧光强度比值为10.7,则产品中CuI的纯度为
您最近一年使用:0次
名校
解题方法
4 . 四氯化碳( )主要用作优良的溶剂、灭火剂、制冷剂、萃取剂等。某化学小组模拟工业原理,用二硫化碳与氯气反应制取四氯化碳,所用实验各部分装置如下图所示(部分夹持仪器、加热装置已省略)。
)主要用作优良的溶剂、灭火剂、制冷剂、萃取剂等。某化学小组模拟工业原理,用二硫化碳与氯气反应制取四氯化碳,所用实验各部分装置如下图所示(部分夹持仪器、加热装置已省略)。
① 与溴水反应生成硫酸和氢溴酸等,可用溴水吸收
与溴水反应生成硫酸和氢溴酸等,可用溴水吸收 ;
;
② 与
与 在铁作催化剂的条件下,在装置C中(85~95℃)反应可生成四氯化碳;
在铁作催化剂的条件下,在装置C中(85~95℃)反应可生成四氯化碳;
③硫单质的沸点445℃, 的沸点46.5℃,
的沸点46.5℃, 沸点76.8℃、密度1.6
沸点76.8℃、密度1.6 。
。
回答下列问题:
(1)装置A中仪器a的名称是___________ ,用浓盐酸与 反应制取
反应制取 ,发生反应的离子方程式为
,发生反应的离子方程式为____________ (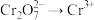 )。
)。
(2)装置的连接顺序为___________ 。
A→_______→________→_______→_____→E。
(3)为使冷凝效果较好,应选用的冷凝管为_______ (填编号);装置C中冷凝管的作用是____________ ,冷水从_________ 口通入。 、
、 ,此时装置F的作用为
,此时装置F的作用为_________________ 。
(5)反应一段时间后,装置C中出现淡黄色固体,写出装置C中发生反应的化学方程式:_________ 。
(6)装置C中反应结束后,先过滤除去固体_________ (填名称),再经过_________ (填操作名称)可得到 。
。
 )主要用作优良的溶剂、灭火剂、制冷剂、萃取剂等。某化学小组模拟工业原理,用二硫化碳与氯气反应制取四氯化碳,所用实验各部分装置如下图所示(部分夹持仪器、加热装置已省略)。
)主要用作优良的溶剂、灭火剂、制冷剂、萃取剂等。某化学小组模拟工业原理,用二硫化碳与氯气反应制取四氯化碳,所用实验各部分装置如下图所示(部分夹持仪器、加热装置已省略)。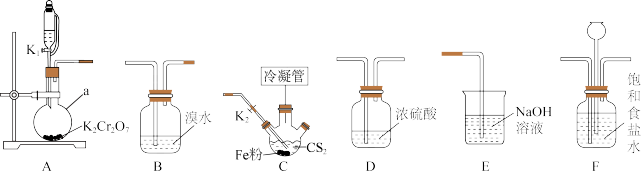
①
 与溴水反应生成硫酸和氢溴酸等,可用溴水吸收
与溴水反应生成硫酸和氢溴酸等,可用溴水吸收 ;
;②
 与
与 在铁作催化剂的条件下,在装置C中(85~95℃)反应可生成四氯化碳;
在铁作催化剂的条件下,在装置C中(85~95℃)反应可生成四氯化碳;③硫单质的沸点445℃,
 的沸点46.5℃,
的沸点46.5℃, 沸点76.8℃、密度1.6
沸点76.8℃、密度1.6 。
。回答下列问题:
(1)装置A中仪器a的名称是
 反应制取
反应制取 ,发生反应的离子方程式为
,发生反应的离子方程式为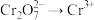 )。
)。(2)装置的连接顺序为
A→_______→________→_______→_____→E。
(3)为使冷凝效果较好,应选用的冷凝管为

 、
、 ,此时装置F的作用为
,此时装置F的作用为(5)反应一段时间后,装置C中出现淡黄色固体,写出装置C中发生反应的化学方程式:
(6)装置C中反应结束后,先过滤除去固体
 。
。
您最近一年使用:0次
7日内更新
|
48次组卷
|
2卷引用:2024届陕西省铜川市王益中学高三下学期模拟预测理综试题-高中化学
解题方法
5 . BeO广泛用于电子、半导体和光学领域。工业上以绿柱石(主要成分为 ,还含有少量铁元素)和方解石(主要成分为
,还含有少量铁元素)和方解石(主要成分为 )为原料制备BeO的流程如图所示:
)为原料制备BeO的流程如图所示: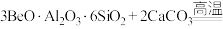
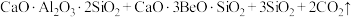 ;
;
②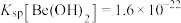 。
。
(1)“滤渣1”的主要成分为___________ (填化学式)。
(2)被浸物料和浸出试剂的流动方向相同时称为“顺流浸出”,相反则为“逆流浸出”,该流程采用“逆流浸出”的优点是___________ 。
(3)“结晶”过程中,铝会以铝铵矾[ ]的形式析出,写出该反应的离子方程式:
]的形式析出,写出该反应的离子方程式:___________ 。
(4)“转化”时加入 的作用是
的作用是___________ 。
(5)“调pH”除铁,利用平衡移动原理解释“调pH”过程中加入 可得到“滤渣2”的原因:
可得到“滤渣2”的原因:___________ 。
(6)“滤液”的主要成分为___________ (填化学式),可以返回___________ 工序循环使用。
(7)常温下,“沉淀”过程中加入 调节pH=5,溶液中的铍离子是否沉淀完全
调节pH=5,溶液中的铍离子是否沉淀完全___________ [列式计算,溶液中c(Mn+)≤1×10-5mol/L时,可认为该离子沉淀完全]。
 ,还含有少量铁元素)和方解石(主要成分为
,还含有少量铁元素)和方解石(主要成分为 )为原料制备BeO的流程如图所示:
)为原料制备BeO的流程如图所示:
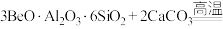
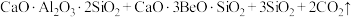 ;
;②
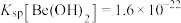 。
。(1)“滤渣1”的主要成分为
(2)被浸物料和浸出试剂的流动方向相同时称为“顺流浸出”,相反则为“逆流浸出”,该流程采用“逆流浸出”的优点是
(3)“结晶”过程中,铝会以铝铵矾[
 ]的形式析出,写出该反应的离子方程式:
]的形式析出,写出该反应的离子方程式:(4)“转化”时加入
 的作用是
的作用是(5)“调pH”除铁,利用平衡移动原理解释“调pH”过程中加入
 可得到“滤渣2”的原因:
可得到“滤渣2”的原因:(6)“滤液”的主要成分为
(7)常温下,“沉淀”过程中加入
 调节pH=5,溶液中的铍离子是否沉淀完全
调节pH=5,溶液中的铍离子是否沉淀完全
您最近一年使用:0次
解题方法
6 . 检验新鲜芹菜中铁元素的实验操作有:(1)剪碎芹菜,研磨;(2)加入蒸馏水,搅拌,过滤;(3)取少量滤液,滴加稀 ;(4)滴加几滴KSCN溶液,振荡,观察。下列仪器在实验时必须用到的有
;(4)滴加几滴KSCN溶液,振荡,观察。下列仪器在实验时必须用到的有
 ;(4)滴加几滴KSCN溶液,振荡,观察。下列仪器在实验时必须用到的有
;(4)滴加几滴KSCN溶液,振荡,观察。下列仪器在实验时必须用到的有
| A.②⑤⑥⑦⑧⑨ | B.③⑥⑦⑧⑨⑩ |
| C.①②③⑥⑨⑩ | D.①④⑤⑥⑦⑧ |
您最近一年使用:0次
名校
解题方法
7 . 一硝基甲苯是一种重要的工业原料,某实验小组用如图所示装置制备一硝基甲苯(包括对硝基甲苯和邻硝基甲苯)。
实验步骤:
①浓硫酸与浓硝酸按体积比1:3配制混合溶液(即混酸)共40mL;
②在三颈烧瓶中加入15mL甲苯(易挥发),按图所示装置装好药品和其它仪器;
③向三颈烧瓶中加入混酸,并不断搅拌(磁力搅拌器已略去);
④控制温度约为50℃,反应大约10min至三颈烧瓶底部有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯,经提纯最终得到对硝基甲苯和邻硝基甲苯共15g。
(1)仪器A的作用为______ ,下口为______ (填“进水”或“出水”)口。
(2)实验前混酸该如何配制____________ ;实验过程中常采用的控温方法是______ 。
(3)甲苯与混酸反应生成邻硝基甲苯的化学方程式为______ 。
(4)若实验后在三颈烧瓶中收集到的产物较少,可能的原因是______ 。
(5)分离产物的方案如下:______ ,操作Ⅵ的名称为______ 。
②操作Ⅲ中加入5%NaOH溶液的目的是______ ,操作Ⅴ中加入无水 的目的是
的目的是______ 。
实验步骤:
①浓硫酸与浓硝酸按体积比1:3配制混合溶液(即混酸)共40mL;
②在三颈烧瓶中加入15mL甲苯(易挥发),按图所示装置装好药品和其它仪器;
③向三颈烧瓶中加入混酸,并不断搅拌(磁力搅拌器已略去);
④控制温度约为50℃,反应大约10min至三颈烧瓶底部有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯,经提纯最终得到对硝基甲苯和邻硝基甲苯共15g。

有机物 | 密度( | 沸点(℃) | 溶解性 |
甲苯 | 0.866 | 110.6 | 不溶于水 |
对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
(1)仪器A的作用为
(2)实验前混酸该如何配制
(3)甲苯与混酸反应生成邻硝基甲苯的化学方程式为
(4)若实验后在三颈烧瓶中收集到的产物较少,可能的原因是
(5)分离产物的方案如下:
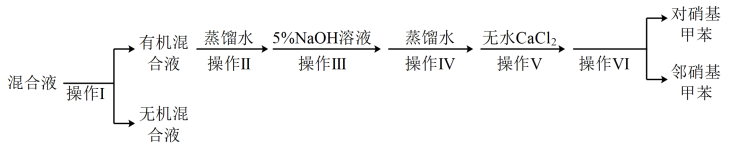
②操作Ⅲ中加入5%NaOH溶液的目的是
 的目的是
的目的是
您最近一年使用:0次
解题方法
8 . 高砷烟尘(主要成分有 、PbO、
、PbO、 、ZnO、
、ZnO、 等)属于危险固体废弃物,对高砷烟尘进行综合处理回收
等)属于危险固体废弃物,对高砷烟尘进行综合处理回收 和金属铟的工业流程如下:
和金属铟的工业流程如下: 或
或 形式存在,氧化性环境中主要存在
形式存在,氧化性环境中主要存在 ;
;
② 在90℃~95℃易分解为
在90℃~95℃易分解为 ,
, 难溶于水;
难溶于水;
③ 。
。
回答下列问题:
(1)“高压酸浸”时,As的浸出率随硫酸浓度的增大而变化的曲线如图所示,硫酸浓度超过 时,As的浸出率随硫酸浓度增大而略微减小的原因可能为
时,As的浸出率随硫酸浓度增大而略微减小的原因可能为________ ,滤渣的主要成分为________ (填化学式)。 ,发生反应的离子方程式为
,发生反应的离子方程式为________ 。已知 在水溶液中电离的总反应式为
在水溶液中电离的总反应式为
 ,
, 。当“硫化”操作后溶液中
。当“硫化”操作后溶液中 ,则此时溶液的
,则此时溶液的
________ 。
(3)“还原”后溶液酸性增强,主要原因是________ (用离子方程式表示)。
(4)“结晶”操作为________ 、过滤、洗涤、干燥。
(5)“萃余液”中含有的金属阳离子为________ (填离子符号),将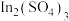 溶液电解得到金属钢,阴极的电极反应式为
溶液电解得到金属钢,阴极的电极反应式为________ 。
 、PbO、
、PbO、 、ZnO、
、ZnO、 等)属于危险固体废弃物,对高砷烟尘进行综合处理回收
等)属于危险固体废弃物,对高砷烟尘进行综合处理回收 和金属铟的工业流程如下:
和金属铟的工业流程如下:
 或
或 形式存在,氧化性环境中主要存在
形式存在,氧化性环境中主要存在 ;
;②
 在90℃~95℃易分解为
在90℃~95℃易分解为 ,
, 难溶于水;
难溶于水;③
 。
。回答下列问题:
(1)“高压酸浸”时,As的浸出率随硫酸浓度的增大而变化的曲线如图所示,硫酸浓度超过
 时,As的浸出率随硫酸浓度增大而略微减小的原因可能为
时,As的浸出率随硫酸浓度增大而略微减小的原因可能为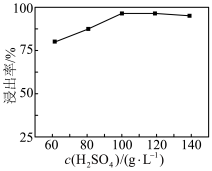
 ,发生反应的离子方程式为
,发生反应的离子方程式为 在水溶液中电离的总反应式为
在水溶液中电离的总反应式为
 ,
, 。当“硫化”操作后溶液中
。当“硫化”操作后溶液中 ,则此时溶液的
,则此时溶液的
(3)“还原”后溶液酸性增强,主要原因是
(4)“结晶”操作为
(5)“萃余液”中含有的金属阳离子为
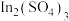 溶液电解得到金属钢,阴极的电极反应式为
溶液电解得到金属钢,阴极的电极反应式为
您最近一年使用:0次
2024-06-01更新
|
74次组卷
|
2卷引用:2024届陕西省安康市安康市高新中学,安康中学高新分校高三下学期模拟预测理综试题-高中化学
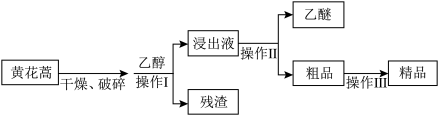
9 . 我国科学家屠呦呦因成功提取青蒿素而获得2015年诺贝尔医学奖。青蒿素是烃的含氧衍生物,为无色针状晶体,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157℃,热稳定性差,青素是高效的抗疟药。已知:乙醚沸点为35℃,与水不互溶,从黄花蒿中提取青蒿素的方法是乙醚浸取法,主要工艺流程为:
(1)先对黄花蒿进行干燥破碎后再加入乙醚的目的是______ 。
(2)操作Ⅰ的名称是______ ,操作Ⅱ的名称是______ ,既可以回收乙醚,又可以使提取液浓缩结晶,再经过滤可得到青蒿素粗品。操作Ⅲ的主要过程可能包括______ (填序号)。
a.加水溶解,蒸发浓缩、冷却结晶
b.加95%的乙醇,浓缩、结晶、过滤
c.加入乙醚进行萃取分液
(3)用如图实验装置测定青蒿素实验式的方法如下:将一定质量的青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。______ ,装置D的作用是______ 。
②装置E、F中盛放的物质是分别是______ 。
a.碱石灰、无水氯化钙 b.浓硫酸、碱石灰 c.无水氯化钙、碱石灰
③某同学认为上述装置存在不足之处,请你指出该问题并提出改进的措施:______ 。
(4)科学家在青蒿素的研究中进一步发现,一定条件下可把青蒿素转化为双氢青蒿素______ 。
a.通过元素分析与质谱法可确定其分子式
b.青蒿素是芳香族化合物
c.青蒿素分子中含有过氧键、酯基和醚键
d.古有“青蒿一握,以水二升溃,绞取汁”,利用的是萃取原理
②双氢青蒿素比青蒿素水溶性更好,因而疗效更好。从结构与性质关系角度推测主要原因是______ 。
(1)先对黄花蒿进行干燥破碎后再加入乙醚的目的是
(2)操作Ⅰ的名称是
a.加水溶解,蒸发浓缩、冷却结晶
b.加95%的乙醇,浓缩、结晶、过滤
c.加入乙醚进行萃取分液
(3)用如图实验装置测定青蒿素实验式的方法如下:将一定质量的青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
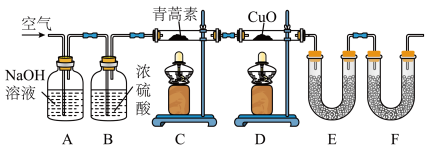
②装置E、F中盛放的物质是分别是
a.碱石灰、无水氯化钙 b.浓硫酸、碱石灰 c.无水氯化钙、碱石灰
③某同学认为上述装置存在不足之处,请你指出该问题并提出改进的措施:
(4)科学家在青蒿素的研究中进一步发现,一定条件下可把青蒿素转化为双氢青蒿素
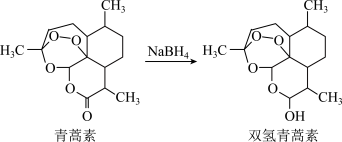
a.通过元素分析与质谱法可确定其分子式
b.青蒿素是芳香族化合物
c.青蒿素分子中含有过氧键、酯基和醚键
d.古有“青蒿一握,以水二升溃,绞取汁”,利用的是萃取原理
②双氢青蒿素比青蒿素水溶性更好,因而疗效更好。从结构与性质关系角度推测主要原因是
您最近一年使用:0次
解题方法
10 . 下列仪器在相应实验中选用合理的是

| A.蒸馏海水:①②③⑤ |
| B.实验室分离碘单质和氯化钠的混合物:③⑦ |
C.用碳酸钠和稀硫酸制备 :⑥ :⑥ |
D.用酸性高锰酸钾标准溶液测定溶液中 含量:④⑤ 含量:④⑤ |
您最近一年使用:0次
2024-06-01更新
|
35次组卷
|
2卷引用:2024届陕西省安康市安康市高新中学,安康中学高新分校高三下学期模拟预测理综试题-高中化学





