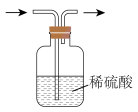
1 . 下列实验装置或操作能达到实验目的的是
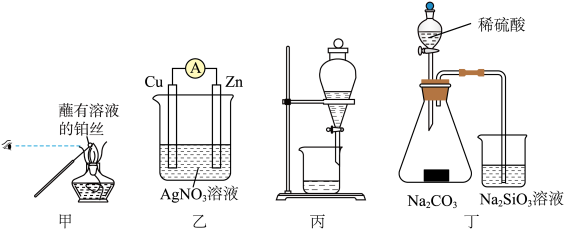
A.图甲:检验某溶液中是否含有 |
B.图乙:将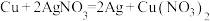 设计成原电池 设计成原电池 |
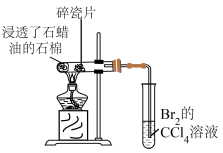
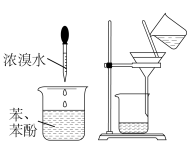
| C.图丙:用乙醇萃取碘水中的碘 |
D.图丁:验证非金属性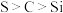 |
您最近一年使用:0次
2 . 某V2O5失活催化剂是重要的含钒二次资源。从酸浸处理之后的浸出液中提取钒的一种工艺流程如图。下列说法错误的是
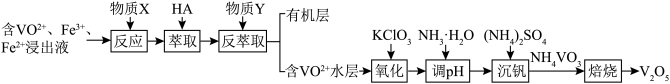
| A.物质X为高锰酸钾溶液 |
| B.反萃取时,物质Y可以选用硫酸 |
| C.氧化过程中,氧化产物与还原产物的物质的量之比为6:1 |
D.调pH时,发生反应:VO +2NH3•H2O +2NH3•H2O VO VO +2NH +2NH +H2O +H2O |
您最近一年使用:0次
3 . 一种高硫锰矿的主要成分为MnCO3和MnS,主要杂质为FeS、SiO2、CaCO3、Al2O3、MgO等,研究人员设计了如图流程,制备Mn3O4。
②Ksp(MgF2)=6.4×10-9、Ksp(CaF2)=4.0×10-11.
(1)“焙烧”的主要目的是___________ 。
(2)“酸浸”过程中,___________ (填“能”或“不能”)用盐酸替换硫酸。
(3)“氧化1”时,试剂a为MnO2,并控制溶液的pH=3,此时发生反应的离子方程式为___________ 。
(4)若省略“氧化”步骤直接进行“中和除杂”,则造成的影响是___________ 。
(5)“净化除杂”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Mg2+)=1.0×10-5mol•L-1,则滤液中c(Ca2+)为___________ mol•L-1.
(6)“氧化2”过程中,在MnSO4溶液中滴入一定浓度的氮水,加压通入空气反应7小时制备Mn3O4,此时发生反应的离子方程式为___________ 。
(7)锰的一种氧化物晶胞结构如图所示:___________ ,该晶胞的密度为___________ g•cm-3(列出计算式,设NA为阿伏加德罗常数的值,晶胞底面边长为apm,高为bpm)。

| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ |
| 开始沉定的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 |
(1)“焙烧”的主要目的是
(2)“酸浸”过程中,
(3)“氧化1”时,试剂a为MnO2,并控制溶液的pH=3,此时发生反应的离子方程式为
(4)若省略“氧化”步骤直接进行“中和除杂”,则造成的影响是
(5)“净化除杂”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Mg2+)=1.0×10-5mol•L-1,则滤液中c(Ca2+)为
(6)“氧化2”过程中,在MnSO4溶液中滴入一定浓度的氮水,加压通入空气反应7小时制备Mn3O4,此时发生反应的离子方程式为
(7)锰的一种氧化物晶胞结构如图所示:

您最近一年使用:0次
4 .  易溶于水,溶液呈中性,可用于制作替代氟利昂的绿色制冷剂,利用高浓度
易溶于水,溶液呈中性,可用于制作替代氟利昂的绿色制冷剂,利用高浓度 粗溶液合成
粗溶液合成 工艺流程如下。下列说法正确的是
工艺流程如下。下列说法正确的是
 易溶于水,溶液呈中性,可用于制作替代氟利昂的绿色制冷剂,利用高浓度
易溶于水,溶液呈中性,可用于制作替代氟利昂的绿色制冷剂,利用高浓度 粗溶液合成
粗溶液合成 工艺流程如下。下列说法正确的是
工艺流程如下。下列说法正确的是
| A.“还原”过程应加入过量BaS |
| B.“滤渣”中两种物质的物质的量相近 |
C. 晶体中存在4原子7电子构成的大 晶体中存在4原子7电子构成的大 键 键 |
D.“浓缩”过程需在 气流中进行 气流中进行 |
您最近一年使用:0次
名校
解题方法
5 . 从废旧镍钴锰三元锂电池正极材料[主要含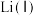 、
、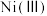 、
、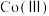 、
、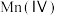 等金属的氧化物]中回收钴的一种流程如下:
等金属的氧化物]中回收钴的一种流程如下: 的形式存在。下列说法正确的是
的形式存在。下列说法正确的是
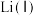 、
、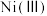 、
、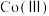 、
、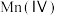 等金属的氧化物]中回收钴的一种流程如下:
等金属的氧化物]中回收钴的一种流程如下: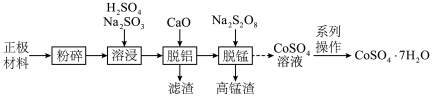
 的形式存在。下列说法正确的是
的形式存在。下列说法正确的是A.“溶浸”中 被还原 被还原 |
B.“脱铝”得到的滤渣成分是 |
C.“脱锰”的离子方程式为: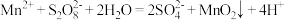 |
| D.“系列操作”含蒸发结晶、洗涤、干燥 |
您最近一年使用:0次
6 . 某研究小组拟在实验室以废铁屑(含有少量炭和 杂质)为原料制备无水
杂质)为原料制备无水 ,设计如下流程(已知
,设计如下流程(已知 易水解):
易水解):不正确 的是
 杂质)为原料制备无水
杂质)为原料制备无水 ,设计如下流程(已知
,设计如下流程(已知 易水解):
易水解):
| A.试剂X可选用硫酸 |
B.“氧化”时: |
| C.操作①②均需用到漏斗、烧杯、玻璃棒 |
| D.“脱水”时可能会产生亚铁盐 |
您最近一年使用:0次
名校
7 . 利用某钒废渣(主要成分为 以及铁、铝、硅的氧化物)制备
以及铁、铝、硅的氧化物)制备 的工艺流程如图。
的工艺流程如图。 溶于酸后以
溶于酸后以 的形式存在;过量
的形式存在;过量 可氧化
可氧化 ;
;
Ⅱ. (有机层)
(有机层)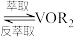 (有机层)
(有机层) ;
;
Ⅲ.溶液中 与
与 可相互转化:
可相互转化: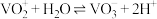 。
。
下列说法错误的是
 以及铁、铝、硅的氧化物)制备
以及铁、铝、硅的氧化物)制备 的工艺流程如图。
的工艺流程如图。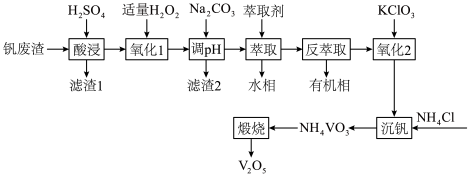
 溶于酸后以
溶于酸后以 的形式存在;过量
的形式存在;过量 可氧化
可氧化 ;
;Ⅱ.
 (有机层)
(有机层)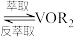 (有机层)
(有机层) ;
;Ⅲ.溶液中
 与
与 可相互转化:
可相互转化: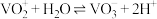 。
。下列说法错误的是
| A.“氧化1”中,不适宜用升温的方式加快转化速率 |
B.“滤渣2”的成分为 |
| C.有机萃取剂可循环使用 |
D.“沉钒”时还需通 调节溶液的酸碱性 调节溶液的酸碱性 |
您最近一年使用:0次
7日内更新
|
475次组卷
|
4卷引用:福建省福州市八县市一中2024届高三下学期模拟联考化学试题
福建省福州市八县市一中2024届高三下学期模拟联考化学试题2024届湖南省湖南大学附属中学高三下学期二模 化学试题 (已下线)江苏省姜堰中学、如东中学、前黄中学三校2023-2024学年高三下学期联考化学试题江苏省部分学校2024届高三下学期高考模拟化学试题
名校
8 . 二氧化铈( )具有较强的氧化性,是一种应用非常广泛的稀土氧化物。以氟碳铈矿(主要含
)具有较强的氧化性,是一种应用非常广泛的稀土氧化物。以氟碳铈矿(主要含 、
、 等)为原料制备
等)为原料制备 的一种工艺流程如图所示。
的一种工艺流程如图所示。
(1)“氧化焙烧”后,Ce元素转化为 和
和 ,写出氧化焙烧的化学方程式
,写出氧化焙烧的化学方程式_______ 。
(2)“酸浸”时,铈的浸出率与温度、 的关系如图所示,应选择的最适宜的条件为
的关系如图所示,应选择的最适宜的条件为_______ (填标号)。不能用盐酸代替硫酸进行酸浸,理由是_______ 。 B.75℃、
B.75℃、 C.85℃、
C.85℃、 D.100℃、
D.100℃、
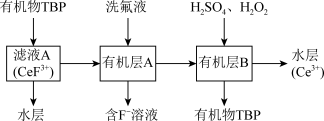
(3)“系列操作”包含以下几个过程: 不能溶于有机物TBP,
不能溶于有机物TBP, 能溶于有机物TBP,且存在反应
能溶于有机物TBP,且存在反应 。
。
“系列操作”在_______ (填仪器名称)中完成,“有机层B”中发生反应的离子方程式为_______ 。
(4)“调pH”中,要使 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制pH大于
为沉淀完全),应控制pH大于_______ (已知:25℃时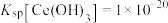 )。
)。
(5)“氧化”中,氧化剂与还原剂的物质的量之比为_______ 。
(6) 具有良好的储氧放氧能力,晶胞如图所示,是汽车尾气净化催化剂的关键成分。
具有良好的储氧放氧能力,晶胞如图所示,是汽车尾气净化催化剂的关键成分。 中位于晶粒表面的
中位于晶粒表面的 具有催化作用。已知
具有催化作用。已知 晶胞边长为
晶胞边长为 ,在边长为
,在边长为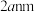 的立方体晶粒中位于表面的
的立方体晶粒中位于表面的 最多有
最多有_______ 个。
②在尾气消除过程中 与
与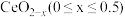 相互转化。
相互转化。 中的Ce为
中的Ce为 、
、 价,测定x的值可判断它们的比例。现取
价,测定x的值可判断它们的比例。现取 固体1.6560g,加入足量硫酸和
固体1.6560g,加入足量硫酸和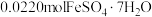 充分溶解,使
充分溶解,使 ⁺全部被还原成
⁺全部被还原成 ,再用
,再用 的酸性
的酸性 标准溶液滴定至终点,重复操作三次,平均消耗标准溶液40.00mL(已知氧化性:
标准溶液滴定至终点,重复操作三次,平均消耗标准溶液40.00mL(已知氧化性: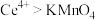 ),则x的值为
),则x的值为_______ ,则此时氧空位率为_______ 。
 )具有较强的氧化性,是一种应用非常广泛的稀土氧化物。以氟碳铈矿(主要含
)具有较强的氧化性,是一种应用非常广泛的稀土氧化物。以氟碳铈矿(主要含 、
、 等)为原料制备
等)为原料制备 的一种工艺流程如图所示。
的一种工艺流程如图所示。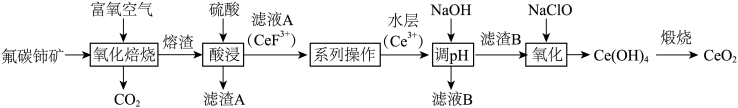
(1)“氧化焙烧”后,Ce元素转化为
 和
和 ,写出氧化焙烧的化学方程式
,写出氧化焙烧的化学方程式(2)“酸浸”时,铈的浸出率与温度、
 的关系如图所示,应选择的最适宜的条件为
的关系如图所示,应选择的最适宜的条件为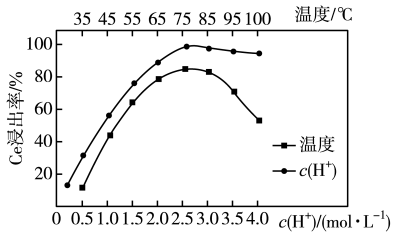
 B.75℃、
B.75℃、 C.85℃、
C.85℃、 D.100℃、
D.100℃、
(3)“系列操作”包含以下几个过程:
 不能溶于有机物TBP,
不能溶于有机物TBP, 能溶于有机物TBP,且存在反应
能溶于有机物TBP,且存在反应 。
。“系列操作”在
(4)“调pH”中,要使
 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制pH大于
为沉淀完全),应控制pH大于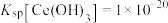 )。
)。(5)“氧化”中,氧化剂与还原剂的物质的量之比为
(6)
 具有良好的储氧放氧能力,晶胞如图所示,是汽车尾气净化催化剂的关键成分。
具有良好的储氧放氧能力,晶胞如图所示,是汽车尾气净化催化剂的关键成分。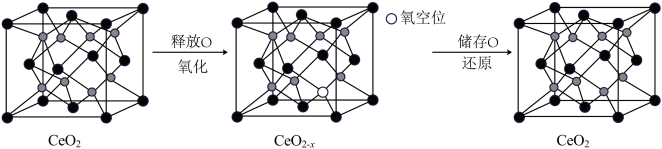
 中位于晶粒表面的
中位于晶粒表面的 具有催化作用。已知
具有催化作用。已知 晶胞边长为
晶胞边长为 ,在边长为
,在边长为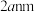 的立方体晶粒中位于表面的
的立方体晶粒中位于表面的 最多有
最多有②在尾气消除过程中
 与
与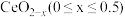 相互转化。
相互转化。 中的Ce为
中的Ce为 、
、 价,测定x的值可判断它们的比例。现取
价,测定x的值可判断它们的比例。现取 固体1.6560g,加入足量硫酸和
固体1.6560g,加入足量硫酸和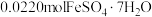 充分溶解,使
充分溶解,使 ⁺全部被还原成
⁺全部被还原成 ,再用
,再用 的酸性
的酸性 标准溶液滴定至终点,重复操作三次,平均消耗标准溶液40.00mL(已知氧化性:
标准溶液滴定至终点,重复操作三次,平均消耗标准溶液40.00mL(已知氧化性: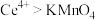 ),则x的值为
),则x的值为
您最近一年使用:0次
解题方法
9 . 二氧化钛化学稳定性好,无污染,可应用于锂电池负极材料。某含钛高炉渣(主要成分为CaTi2O5,含少量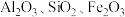 等杂质)制备二氧化钛工艺如下:
等杂质)制备二氧化钛工艺如下:___________ 。
(2)“焙烧”过程生成偏钛酸钠 的化学方程式为
的化学方程式为___________ 。
(3)“滤液1”中Si、Al分别以___________ (填离子符号)存在。
(4)“滤渣1”的主要成分为___________ 。
(5)“还原”工序需要在低温下进行的原因是___________ 。
(6)“水解”步骤 转化为偏钛酸
转化为偏钛酸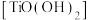 沉淀,反应的离子方程式为
沉淀,反应的离子方程式为___________ 。
(7)将80g二氧化钛和40g焦炭混合,在真空高温条件下制备碳化钛(TiC)的化学方程式为___________ ,若该过程固体失重率达到35%,则碳化钛的产率为___________ 。
(8)锐钛矿型TiO2晶胞结构如图,该晶胞中氧的配位数为___________ ;已知该晶体密度为 ,则阿伏加德罗常数为
,则阿伏加德罗常数为___________ mol⁻¹(用含ρ、a、b的代数式表示)。
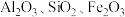 等杂质)制备二氧化钛工艺如下:
等杂质)制备二氧化钛工艺如下:
(2)“焙烧”过程生成偏钛酸钠
 的化学方程式为
的化学方程式为(3)“滤液1”中Si、Al分别以
(4)“滤渣1”的主要成分为
(5)“还原”工序需要在低温下进行的原因是
(6)“水解”步骤
 转化为偏钛酸
转化为偏钛酸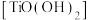 沉淀,反应的离子方程式为
沉淀,反应的离子方程式为(7)将80g二氧化钛和40g焦炭混合,在真空高温条件下制备碳化钛(TiC)的化学方程式为
(8)锐钛矿型TiO2晶胞结构如图,该晶胞中氧的配位数为
 ,则阿伏加德罗常数为
,则阿伏加德罗常数为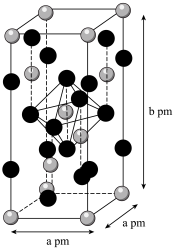
您最近一年使用:0次
解题方法
10 . 下列实验能达到目的的是
| A | B |
|
|
除去 中的 中的 | 证明生成乙烯 |
| C | D |
|
|
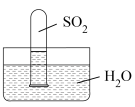
证明 能与水反应 能与水反应 | 除去苯中的苯酚 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次