名校
解题方法
1 . 高纯度钛及其合金在微电子、原子能、航天航空等高科技领域有重要的用途,某化学小组在实验室通过下列装置测定海绵钛(含杂质)纯度。已知 为深红棕色晶体,沸点
为深红棕色晶体,沸点 、易水解,高温时可与氧气发生反应。
、易水解,高温时可与氧气发生反应。
实验步骤:①按图甲所示连接好装置,向仪器内通入氮气,待气体充满整个装置后,将电热炉Ⅰ的温度调整为 ,对装置和海绵钛进行脱气处理。
,对装置和海绵钛进行脱气处理。
②将图乙中的 管与
管与 管进行连接,停止通入氮气,并将系统压强降低至
管进行连接,停止通入氮气,并将系统压强降低至 以下,调节电热炉Ⅱ温度至
以下,调节电热炉Ⅱ温度至 ,反应持续一定时间。
,反应持续一定时间。
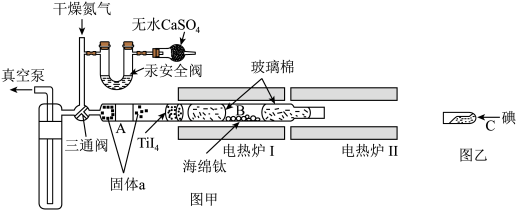
(1)汞安全阀的作用为_____________________________________________ ,盛放无水 的仪器名称为
的仪器名称为_____________________ 。
(2)对装置和海绵钛进行脱气处理的目的为_______________________ 。
(3)装置B中玻璃棉的作用为__________________________ 。
(4)固体 的成分为
的成分为_____________ ,在装置 中收集固体
中收集固体 的目的为
的目的为_____________________________________ 。
(5)通入氮气和对系统进行减压操作时,三通阀的孔路位置示意图分别为_________________ 、_________________ 。

(6)已知管B中放入海绵钛的质量为4.50g,充分反应后收集到的TiI4为43.96g,则海绵钛的纯度为_________ (保留到小数点后2位)。
 为深红棕色晶体,沸点
为深红棕色晶体,沸点 、易水解,高温时可与氧气发生反应。
、易水解,高温时可与氧气发生反应。实验步骤:①按图甲所示连接好装置,向仪器内通入氮气,待气体充满整个装置后,将电热炉Ⅰ的温度调整为
 ,对装置和海绵钛进行脱气处理。
,对装置和海绵钛进行脱气处理。②将图乙中的
 管与
管与 管进行连接,停止通入氮气,并将系统压强降低至
管进行连接,停止通入氮气,并将系统压强降低至 以下,调节电热炉Ⅱ温度至
以下,调节电热炉Ⅱ温度至 ,反应持续一定时间。
,反应持续一定时间。
(1)汞安全阀的作用为
 的仪器名称为
的仪器名称为(2)对装置和海绵钛进行脱气处理的目的为
(3)装置B中玻璃棉的作用为
(4)固体
 的成分为
的成分为 中收集固体
中收集固体 的目的为
的目的为(5)通入氮气和对系统进行减压操作时,三通阀的孔路位置示意图分别为

(6)已知管B中放入海绵钛的质量为4.50g,充分反应后收集到的TiI4为43.96g,则海绵钛的纯度为
您最近半年使用:0次
2024-02-26更新
|
168次组卷
|
2卷引用:河北省秦皇岛市昌黎县开学联考2023-2024学年高三下学期开学化学试题
名校
2 . 化学是一门以实验为基础的科学。下列实验操作与目的不正确的是
| 选项 | 实验操作 | 目的 |
| A | 铁粉与水蒸气反应中将生成的气体通入肥皂水中,并点燃肥皂泡 | 检验反应产生氢气 |
| B | 配制 溶液时加入适量铁粉 溶液时加入适量铁粉 | 防止 被氧化 被氧化 |
| C | 蒸馏水加热至沸腾后滴加几滴饱和 溶液,继续煮沸至液体呈红褐色 溶液,继续煮沸至液体呈红褐色 | 制备 胶体 胶体 |
| D | 实验结束,将剩余 固体放回原试剂瓶 固体放回原试剂瓶 | 节约试剂 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2022-01-24更新
|
223次组卷
|
2卷引用:广东省肇庆市2021-2022学年高一上学期期末教学质量检测化学试题
3 . 危险化学品的外包装上常印有警示性标志。下列化学药品名称与警示性标志对应不正确的是
 |  |  |  |
| A. 浓硫酸 | B. 汽油 | C. 酒精 | D. 氯酸钾 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2021-04-24更新
|
89次组卷
|
6卷引用:【全国百强校】陕西省长安区第一中学2018-2019学年高一上学期第一次月考化学试题
名校
解题方法
4 . 过氧乙酸( )是一种常用的消毒剂,易溶于水、易挥发、见光或受热易分解,其制备愿理为:
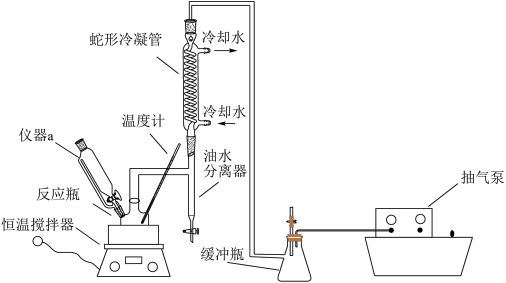
)是一种常用的消毒剂,易溶于水、易挥发、见光或受热易分解,其制备愿理为: ,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水,以提高产率,为减少反应瓶中乙丁酯的损耗,反应开始前,在油水分离器中加满乙酸丁酯,实验装置如下图。
,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水,以提高产率,为减少反应瓶中乙丁酯的损耗,反应开始前,在油水分离器中加满乙酸丁酯,实验装置如下图。
(1)过氧乙酸保存与使用时应注意____ (填标号)。
A.避光 B.低温 C.配制消毒液时应带上橡胶手套 D.储存于密闭的金属容器
(2)仪器a的名称是___ ,在本实验中与使用普通分液漏斗相比的优点是__ ,其中盛放的试剂为__ (填“乙酸”或“双氧水”)
(3)反应体系采用减压的目的是___ 。
(4)过氧乙酸(含有少量 杂质)的含量测定流程如下图。
杂质)的含量测定流程如下图。

①判断 恰好除尽的实验现象是
恰好除尽的实验现象是____ 。
②过氧乙酸被 还原,还原产物之一为乙酸,其离子方程式为
还原,还原产物之一为乙酸,其离子方程式为_____ 。
③若样品体积为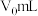 ,加入
,加入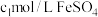 溶液
溶液 ,消耗
,消耗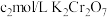 溶液
溶液 ,则过氧乙酸含量为
,则过氧乙酸含量为_____  。
。
(5)判断下列情况对过氧乙酸含量测定结果的影响(填“偏高”、“偏低”或“无影响”)。
①若滴定前无气泡,滴定终点时出现气泡,会使测定结果_____ 。
②若 标准液部分变质,会使测定结果
标准液部分变质,会使测定结果_______ 。
 )是一种常用的消毒剂,易溶于水、易挥发、见光或受热易分解,其制备愿理为:
)是一种常用的消毒剂,易溶于水、易挥发、见光或受热易分解,其制备愿理为: ,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水,以提高产率,为减少反应瓶中乙丁酯的损耗,反应开始前,在油水分离器中加满乙酸丁酯,实验装置如下图。
,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水,以提高产率,为减少反应瓶中乙丁酯的损耗,反应开始前,在油水分离器中加满乙酸丁酯,实验装置如下图。
(1)过氧乙酸保存与使用时应注意
A.避光 B.低温 C.配制消毒液时应带上橡胶手套 D.储存于密闭的金属容器
(2)仪器a的名称是
(3)反应体系采用减压的目的是
(4)过氧乙酸(含有少量
 杂质)的含量测定流程如下图。
杂质)的含量测定流程如下图。
①判断
 恰好除尽的实验现象是
恰好除尽的实验现象是②过氧乙酸被
 还原,还原产物之一为乙酸,其离子方程式为
还原,还原产物之一为乙酸,其离子方程式为③若样品体积为
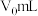 ,加入
,加入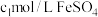 溶液
溶液 ,消耗
,消耗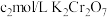 溶液
溶液 ,则过氧乙酸含量为
,则过氧乙酸含量为 。
。(5)判断下列情况对过氧乙酸含量测定结果的影响(填“偏高”、“偏低”或“无影响”)。
①若滴定前无气泡,滴定终点时出现气泡,会使测定结果
②若
 标准液部分变质,会使测定结果
标准液部分变质,会使测定结果
您最近半年使用:0次
名校
解题方法
5 . 运用化学链燃烧技术有利于提高燃料利用率。化学链燃烧技术的基本原理是借助载氧剂(如Fe2O3、FeO等)将燃料与空气直接接触的传统燃烧反应分解为几个气固反应,燃料与空气无须接触,由载氧剂将空气中的氧气传递给燃料。回答下列问题:
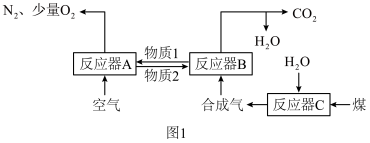
以Fe2O3作载氧剂的化学链燃烧循环转化反应的部分热化学方程式如下,循环转化的原理如图1所示。
①C(s)+H2O(g)═CO(g)+H2(g)△H1=akJ•mol﹣1
②CO(g)+H2(g)+O2(g)═CO2(g)+H2O(g)△H2=bkJ•mol﹣1
(1)写出图1中总反应的热化学方程式:_____
(2)空气经反应器A后得到的尾气_____ (填“能”或“不能”)直接用作工业合成氨的原料气,原因是_____ 。
Ⅱ.用FeO作载氧剂,部分反应的lgKp[K是用平衡分压(平衡分压=总压×物质的量分数)代替平衡浓度]与温度的关系如图2所示。
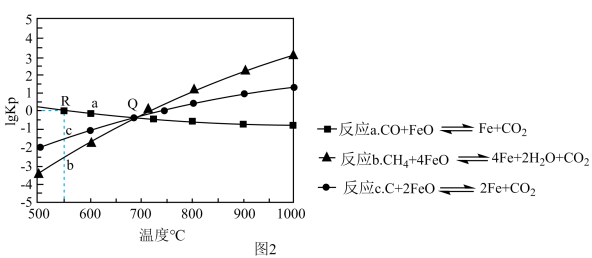
(3)图2涉及的反应中,属于吸热反应的是反应_____ (填字母)。
(4)R点对应温度下,向某恒容密闭容器中通入1mol CO,并加入足量的FeO,只发生反应CO(g)+FeO(s)⇌Fe(s)+CO2(g),则CO的平衡转化率为_____ 。
Ⅲ.在T℃下,向某恒容密闭容器中加入1mol CH4(g)和4mol FeO(s)进行反应:CH4(g)+4FeO(s)⇌4Fe(s)+2H2O(g)+CO2(g)。反应起始时压强为p0,反应进行至10min时达到平衡状态,测得此时容器的气体压强是起始压强的2倍。
(5)T℃下,该反应的Kp=_____ 。
(6)若起始时向该容器中加入1mol CH4(g),4mol FeO(s),1mol H2O(g),0.5mol CO2(g),此时反应向_____ (填“正反应”或“逆反应”)方向进行。
(7)其他条件不变,若将该容器改为恒压密闭容器,则此时CH4(g)的平衡转化率_____ (填“增大”“减小”或“不变”)。

以Fe2O3作载氧剂的化学链燃烧循环转化反应的部分热化学方程式如下,循环转化的原理如图1所示。
①C(s)+H2O(g)═CO(g)+H2(g)△H1=akJ•mol﹣1
②CO(g)+H2(g)+O2(g)═CO2(g)+H2O(g)△H2=bkJ•mol﹣1
(1)写出图1中总反应的热化学方程式:
(2)空气经反应器A后得到的尾气
Ⅱ.用FeO作载氧剂,部分反应的lgKp[K是用平衡分压(平衡分压=总压×物质的量分数)代替平衡浓度]与温度的关系如图2所示。

(3)图2涉及的反应中,属于吸热反应的是反应
(4)R点对应温度下,向某恒容密闭容器中通入1mol CO,并加入足量的FeO,只发生反应CO(g)+FeO(s)⇌Fe(s)+CO2(g),则CO的平衡转化率为
Ⅲ.在T℃下,向某恒容密闭容器中加入1mol CH4(g)和4mol FeO(s)进行反应:CH4(g)+4FeO(s)⇌4Fe(s)+2H2O(g)+CO2(g)。反应起始时压强为p0,反应进行至10min时达到平衡状态,测得此时容器的气体压强是起始压强的2倍。
(5)T℃下,该反应的Kp=
(6)若起始时向该容器中加入1mol CH4(g),4mol FeO(s),1mol H2O(g),0.5mol CO2(g),此时反应向
(7)其他条件不变,若将该容器改为恒压密闭容器,则此时CH4(g)的平衡转化率
您最近半年使用:0次
2020-07-23更新
|
292次组卷
|
5卷引用:云南省昆明市第一中学2020届高三上学期12月月考理综试卷化学试题
解题方法
6 . 二氧化氯(ClO2)是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
(1)根据文献资料,用NaClO3和双氧水在酸性条件下可制得ClO2。某小组按照文献中制备ClO2的方法设计了如图所示的实验装置用于制备ClO2。

①通入氮气的主要作用有2个,一是可以起到搅拌作用,二是____________ 。
②装置B的作用是____________ 。
③装置A用于生成ClO2气体,其中H2O2的作用是____________ 。
(2)测定装置C中ClO2溶液的浓度:取10.00mLC中溶液于锥形瓶中,加入足量H2SO4酸化的KI溶液(ClO2还原为Cl-),然后加入____________ 作指示剂,用0.1000mol·L-1的Na2S2O3标准液滴定锥形瓶中的溶液(I2+2 =2I-+
=2I-+ ),消耗标准溶液的体积为20.00mL。滴定终点的现象是
),消耗标准溶液的体积为20.00mL。滴定终点的现象是____________ ,C中ClO2溶液的浓度是____________ mol·L-1。
(3)ClO2可将废水中的CN-氧化成CO2和N2,其离子方程式为____________ 。
(1)根据文献资料,用NaClO3和双氧水在酸性条件下可制得ClO2。某小组按照文献中制备ClO2的方法设计了如图所示的实验装置用于制备ClO2。

①通入氮气的主要作用有2个,一是可以起到搅拌作用,二是
②装置B的作用是
③装置A用于生成ClO2气体,其中H2O2的作用是
(2)测定装置C中ClO2溶液的浓度:取10.00mLC中溶液于锥形瓶中,加入足量H2SO4酸化的KI溶液(ClO2还原为Cl-),然后加入
 =2I-+
=2I-+ ),消耗标准溶液的体积为20.00mL。滴定终点的现象是
),消耗标准溶液的体积为20.00mL。滴定终点的现象是(3)ClO2可将废水中的CN-氧化成CO2和N2,其离子方程式为
您最近半年使用:0次
解题方法
7 . 环戊二烯基铁[ Fe(C5H5)2]是一种有机过渡金属化合物,常温下为橙黄色粉末,难溶于水,易溶于有机溶剂,温度超过100 °C能够升华,实验室制备环戊二烯基铁的装置和步骤如下:

实验步骤:
步骤1:在三颈烧瓶中加入10mL乙二醇二甲醚(作溶剂)和4. 5 g研细的 KOH 粉末,通入氮气并开启磁力搅拌器 ,然后加入1. 5mL环戊二烯(过量);
步骤2:将1.5g FeCl2•4H2O溶于5 mL二甲基亚砜中 ,并转入滴液漏斗中,将步骤1中的混合物猛烈搅拌10 min,打开滴液漏斗将氯化亚铁的二甲基亚砜溶液在45 min钟左右滴完;
步骤3:关闭滴液漏斗,在氮气保护下继续搅拌30 min;
步骤4:将反应后的混合液倒入100 m L烧杯内,加入少量盐酸除去剩余的KOH,再加入20mL 水,继续搅拌悬浊液15min,抽滤产物,并用水洗涤产物3~4次,最后将产物铺在面皿上,置于真空干燥器内干燥。回答下列问题:
(1)仪器a的作用是___________________ 。
(2)制备过程中若不通入氮气,会降低环戊二烯基铁的产率,试分析其中的原因:__________ 。
(3)硅油的主要作用是______ 。
(4)步骤4中分离环戊二烯基铁也可采用如下方法,请将分离步骤补充完整:向反应后的混合液加入10 mL乙醚(ρ= 0.71g• cm-3) 充分搅拌,然后转入_____ (填仪器名称)中,依次用盐酸、水各洗涤两次,待液体分层后_____________ (填完整操作过程),将含有二环戊二烯基合铁的溶液在通风橱中蒸发得到二环戊二烯基合铁粗产品。
(5)可采用如图所示的简易装置分离提纯环戊二烯基铁。将颗粒状环戊二烯基铁放入蒸发皿中并小火加热,环戊二烯基铁在扎有小孔的滤纸上凝结,该分离提纯方法的名称是_______________ ,装置棉花的作用是___________ 。

(6)若最终制得环戊二烯基铁质量为 0.16g,则产率为_____ %(保留一位小数)。

实验步骤:
步骤1:在三颈烧瓶中加入10mL乙二醇二甲醚(作溶剂)和4. 5 g研细的 KOH 粉末,通入氮气并开启磁力搅拌器 ,然后加入1. 5mL环戊二烯(过量);
步骤2:将1.5g FeCl2•4H2O溶于5 mL二甲基亚砜中 ,并转入滴液漏斗中,将步骤1中的混合物猛烈搅拌10 min,打开滴液漏斗将氯化亚铁的二甲基亚砜溶液在45 min钟左右滴完;
步骤3:关闭滴液漏斗,在氮气保护下继续搅拌30 min;
步骤4:将反应后的混合液倒入100 m L烧杯内,加入少量盐酸除去剩余的KOH,再加入20mL 水,继续搅拌悬浊液15min,抽滤产物,并用水洗涤产物3~4次,最后将产物铺在面皿上,置于真空干燥器内干燥。回答下列问题:
(1)仪器a的作用是
(2)制备过程中若不通入氮气,会降低环戊二烯基铁的产率,试分析其中的原因:
(3)硅油的主要作用是
(4)步骤4中分离环戊二烯基铁也可采用如下方法,请将分离步骤补充完整:向反应后的混合液加入10 mL乙醚(ρ= 0.71g• cm-3) 充分搅拌,然后转入
(5)可采用如图所示的简易装置分离提纯环戊二烯基铁。将颗粒状环戊二烯基铁放入蒸发皿中并小火加热,环戊二烯基铁在扎有小孔的滤纸上凝结,该分离提纯方法的名称是

(6)若最终制得环戊二烯基铁质量为 0.16g,则产率为
您最近半年使用:0次
8 . 正丁醚可作许多有机物的溶剂及萃取剂 ,常用于电子级清洗剂及用于有机合成 。实验室用正丁醇与浓H2SO4反应制取,实验装置如右图,加热与夹持装置略去。反应原理与有关数据:
反应原理: 2C4H9OH C4H9OC4H9+H2O
C4H9OC4H9+H2O
副反应:C4H9OH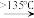 C2H5CH=CH2+H2O
C2H5CH=CH2+H2O

实验步骤如下:
①在二口烧瓶中加入0.34mol正丁醇和4.5mL浓H2SO4,再加两小粒沸石,摇匀。
②加热搅拌,温度上升至100~ll0℃开始反应。随着反应的进行,反应中产生的水经冷凝后收集在水分离器的下层,上层有机物至水分离器支管时,即可返回烧瓶。加热至反应完成。
③将反应液冷却,依次用水、50%硫酸洗涤、水洗涤,再用无水氯化钙干燥,过滤,蒸馏,得正丁醚的质量为Wg。
请回答:
(1)制备正丁醚的反应类型是____________ ,仪器a的名称是_________ 。
(2)步骤①中药品的添加顺序是,先加______ (填“正丁醇”或“浓H2SO4”),沸石的作用是___________________ 。
(3)步骤②中为减少副反应,加热温度应不超过_________ ℃为宜。使用水分离器不断分离出水的目的是________ 。如何判断反应已经完成?当_____ 时,表明反应完成,即可停止实验。
(4)步骤③中用50%硫酸洗涤的目的是为了除去______________ 。本实验中,正丁醚的产率为_____ (列出含W的表达式即可)。
反应原理: 2C4H9OH
 C4H9OC4H9+H2O
C4H9OC4H9+H2O副反应:C4H9OH
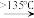 C2H5CH=CH2+H2O
C2H5CH=CH2+H2O
| 物质 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | ||
| 水 | 50%硫酸 | 其它 | ||||
| 正丁醇 | 74 | -89.8 | 117.7 | 微溶 | 易溶 | 二者互溶 |
| 正丁醚 | 130 | -98 | 142.4 | 不溶 | 微溶 | |
实验步骤如下:
①在二口烧瓶中加入0.34mol正丁醇和4.5mL浓H2SO4,再加两小粒沸石,摇匀。
②加热搅拌,温度上升至100~ll0℃开始反应。随着反应的进行,反应中产生的水经冷凝后收集在水分离器的下层,上层有机物至水分离器支管时,即可返回烧瓶。加热至反应完成。
③将反应液冷却,依次用水、50%硫酸洗涤、水洗涤,再用无水氯化钙干燥,过滤,蒸馏,得正丁醚的质量为Wg。
请回答:
(1)制备正丁醚的反应类型是
(2)步骤①中药品的添加顺序是,先加
(3)步骤②中为减少副反应,加热温度应不超过
(4)步骤③中用50%硫酸洗涤的目的是为了除去
您最近半年使用:0次
名校
解题方法
9 . 铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某废旧铍铜元件(含25%BeO、71%CuS、少量 FeS和 SiO2)中回收铍和铜两种金属的工艺流程如图:
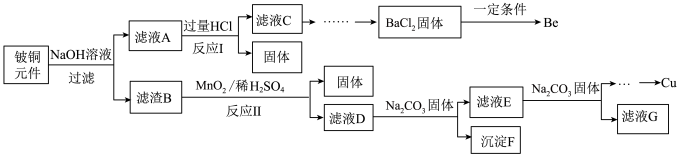
已知:
Ⅰ.铍、铝元素化学性质相似;
Ⅱ.常温下部分难溶物的溶度积常数如表:
(1)滤液A的成分除 NaOH、Na2BeO2外,还有________ (填化学式),写出反应I中Na2BeO2,与过量盐酸反应的化学方程式:_________________ 。
(2)从滤液C 中提纯纯BeCl2,最合理的实验步骤顺序为_________ (填字母)
a.加入过量的氨水 b.通入过量 CO2 c.加入过量NaOH溶液 d.加入适量HCl e.洗涤 f.过滤
(3)MnO2能将金属硫化物中的硫元素氧化为硫单质,写出反应Ⅱ中CuS发生反应的离子方程式:__________ 。若用浓HNO3溶解金属硫化物,缺点是________ (任写一条)
(4)滤液D中c(Cu2+)= 2.2 mol∙L-1、c(Fe3+) = 8.0×10 -3mol∙L-1、c(Mn2+)= 0.01mol∙L-1,逐滴加入 Na2CO3溶液调节pH 可将其转变成氢氧化物依次分离,首先沉淀的是______ (填离子符号)。为使铜离子开始沉淀,常温下应调节溶液的pH____ 4。

已知:
Ⅰ.铍、铝元素化学性质相似;
Ⅱ.常温下部分难溶物的溶度积常数如表:
| 难溶物 | Cu(OH)2 | Fe(OH)3 | Mn(OH)2 |
| Ksp | 2.2×10-20 | 4.0×10-38 | 2.1×10-13 |
(1)滤液A的成分除 NaOH、Na2BeO2外,还有
(2)从滤液C 中提纯纯BeCl2,最合理的实验步骤顺序为
a.加入过量的氨水 b.通入过量 CO2 c.加入过量NaOH溶液 d.加入适量HCl e.洗涤 f.过滤
(3)MnO2能将金属硫化物中的硫元素氧化为硫单质,写出反应Ⅱ中CuS发生反应的离子方程式:
(4)滤液D中c(Cu2+)= 2.2 mol∙L-1、c(Fe3+) = 8.0×10 -3mol∙L-1、c(Mn2+)= 0.01mol∙L-1,逐滴加入 Na2CO3溶液调节pH 可将其转变成氢氧化物依次分离,首先沉淀的是
您最近半年使用:0次
解题方法
10 . (1)古代的“药金”外观与金相似,常被误认为是金子。其冶炼方法如下:将碳酸锌、赤铜(Cu2O)、木炭按一定比例混合加热到800℃,即得金光闪闪的“药金”。
①“药金”的主要成分是__ (填化学式)。
②有关冶炼的化学方程式是__ 。
(2)某地出产的孔雀石的主要成分是Cu2(OH)2CO3。
①试写出该孔雀石在加热条件下分解的化学方程式:__ 。
②试以①中所得金属氧化物为原料,分别采用湿法冶炼和高温冶炼的方法制取金属铜。供选择的试剂有木炭、铁屑、生石灰、稀硫酸,不得另选其他试剂。写出两种方法制取金属铜的化学方程式。
a.湿法冶炼:__ 、__ (可不填满,也可补充,下同)。
b.高温冶炼:__ 。
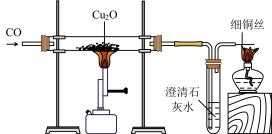
(3)利用一氧化碳还原赤铜矿(Cu2O)冶炼铜。实验室可用如图所示装置进行实验,当硬质玻璃管中的反应结束时,应进行的实验操作是___ 。
(4)利用辉铜矿(Cu2S)冶炼铜的原理如下:
Ⅰ.取一定质量的Cu2S在空气中高温焙烧,完全反应后生成一种铜的氧化物和二氧化硫;
Ⅱ.再取上述一半质量的Cu2S,与Ⅰ中生成的铜的氧化物混合均匀,隔绝空气高温煅烧,恰好完全反应,生成铜和二氧化硫。结合质量守恒定律,推断这种铜的氧化物的化学式为__ 。
①“药金”的主要成分是
②有关冶炼的化学方程式是
(2)某地出产的孔雀石的主要成分是Cu2(OH)2CO3。
①试写出该孔雀石在加热条件下分解的化学方程式:
②试以①中所得金属氧化物为原料,分别采用湿法冶炼和高温冶炼的方法制取金属铜。供选择的试剂有木炭、铁屑、生石灰、稀硫酸,不得另选其他试剂。写出两种方法制取金属铜的化学方程式。
a.湿法冶炼:
b.高温冶炼:
(3)利用一氧化碳还原赤铜矿(Cu2O)冶炼铜。实验室可用如图所示装置进行实验,当硬质玻璃管中的反应结束时,应进行的实验操作是

(4)利用辉铜矿(Cu2S)冶炼铜的原理如下:
Ⅰ.取一定质量的Cu2S在空气中高温焙烧,完全反应后生成一种铜的氧化物和二氧化硫;
Ⅱ.再取上述一半质量的Cu2S,与Ⅰ中生成的铜的氧化物混合均匀,隔绝空气高温煅烧,恰好完全反应,生成铜和二氧化硫。结合质量守恒定律,推断这种铜的氧化物的化学式为
您最近半年使用:0次



