1 . 某同学设计实验探究工业制乙烯的原理和乙烯主要的化学性质,实验装置如图所示。
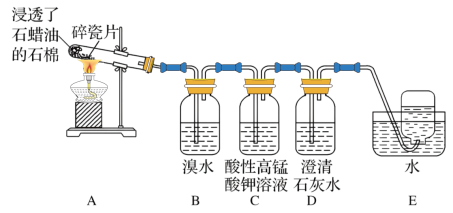
(1)B装置中的实验现象是_______ 。写出对应的化学反应方程式_______ 。
(2)C装置中的实验现象是_______ ,其中发生反应的反应类型是_______ 。
(3)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置_______ (填序号)中的实验现象可判断该资料是否真实。
(4)通过题述实验探究可知,检验甲烷和乙烯的方法是_______ (填序号,下同);除去甲烷中乙烯的方法是_______ 。
A.气体通入水中 B.气体通过装溴水的洗气瓶
C.气体通过装酸性高锰酸钾溶液的洗气瓶 D.气体通过氢氧化钠溶液
(5)燃烧乙烯,实验现象是_______ 。

(1)B装置中的实验现象是
(2)C装置中的实验现象是
(3)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置
(4)通过题述实验探究可知,检验甲烷和乙烯的方法是
A.气体通入水中 B.气体通过装溴水的洗气瓶
C.气体通过装酸性高锰酸钾溶液的洗气瓶 D.气体通过氢氧化钠溶液
(5)燃烧乙烯,实验现象是
您最近一年使用:0次
2022-09-23更新
|
360次组卷
|
2卷引用:重庆市2022-2023学年高三下学期2月月考化学试题
名校
解题方法
2 . 工业上由粗锰粉(主要杂质为Fe、Ni、Pb等金属单质)制备高纯碳酸锰。其主要工艺流程如下:

下列有关说法不正确 的是

下列有关说法
| A.可以通过搅拌的方式提高“酸浸”时粗锰粉的浸取率 |
B.向酸浸后的滤液中加入 ,反应的离子方程式为: ,反应的离子方程式为: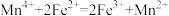 |
C.除铁时加入的物质X可以为 ,使 ,使 转化为 转化为 沉淀而除去 沉淀而除去 |
D.取除铁后的滤液,加入几滴KSCN溶液,无明显现象证明 已除尽 已除尽 |
您最近一年使用:0次
2022-01-23更新
|
217次组卷
|
3卷引用:重庆市缙云教育联盟2021-2022学年高二下学期4月质量检测化学试题
解题方法
3 . 某同学设计实验以探究元素性质的递变规律,实验装置如图所示:
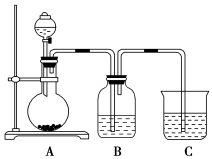
实验Ⅰ:探究同主族元素C和Si非金属性递变规律。
已知A装置的烧瓶里装有大理石,分液漏斗里装有盐酸,B装置中装有饱和碳酸氢钠溶液,C装置中装有足量Na2SiO3溶液,试回答:
(1) 中反应的离子方程式为
中反应的离子方程式为_______ ,B装置的作用是_______ ;
(2)C中发生反应的化学方程式为_______ 可观察到的现象是_______ ;
(3)根据实验现象推知,碳酸、盐酸、硅酸的酸性强弱顺序为_______ ,能否由此得出碳、氯、硅三种元素非金属性的强弱_______  填“能”或“否”
填“能”或“否” 并说明理由
并说明理由_______ 。
实验Ⅱ:探究同周期元素S和Cl的非金属性强弱。已知常温下高锰酸钾与浓盐酸混合可产生氯气,B装置中装有Na2S溶液,试回答:
(4) 装置分液漏斗中所装试剂为
装置分液漏斗中所装试剂为_______ ,B中可观察到的现象是_______ ;
(5)C装置的作用是_______ ,写出C中发生反应的离子方程式_______ 。
(6)验结论:氧化性:_______ ,非金属性:_______ 。

实验Ⅰ:探究同主族元素C和Si非金属性递变规律。
已知A装置的烧瓶里装有大理石,分液漏斗里装有盐酸,B装置中装有饱和碳酸氢钠溶液,C装置中装有足量Na2SiO3溶液,试回答:
(1)
 中反应的离子方程式为
中反应的离子方程式为(2)C中发生反应的化学方程式为
(3)根据实验现象推知,碳酸、盐酸、硅酸的酸性强弱顺序为
 填“能”或“否”
填“能”或“否” 并说明理由
并说明理由实验Ⅱ:探究同周期元素S和Cl的非金属性强弱。已知常温下高锰酸钾与浓盐酸混合可产生氯气,B装置中装有Na2S溶液,试回答:
(4)
 装置分液漏斗中所装试剂为
装置分液漏斗中所装试剂为(5)C装置的作用是
(6)验结论:氧化性:
您最近一年使用:0次
4 . 鱼浮灵是一种化学增氧剂,主要成分为过氧碳酸钠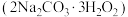 ,有
,有 和
和 的双重性质,50℃开始分解,在异丙醇中溶解度较低。实验室用
的双重性质,50℃开始分解,在异丙醇中溶解度较低。实验室用 与稳定剂的混合液(稳定剂不参与制备反应)和
与稳定剂的混合液(稳定剂不参与制备反应)和 化合制备过氧碳酸钠,制备装置如图。
化合制备过氧碳酸钠,制备装置如图。_______ ,仪器A中冷凝水的进口是_______ (填“a”或“b”)。
(2)烧瓶中发生主要反应的方程式为_______ 。
(3)下列物质可做该反应的稳定剂的是_______。
(4)实验时反应温度应控制在15~20℃,可采取的措施是_______ 。
(5)反应结束后,为了获得干燥的过氧碳酸钠固体,可在反应液中加入适量的_______ ,再进行静置、抽滤、洗涤、_______ 。
(6)取4g过氧碳酸钠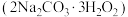 产品配成100mL溶液,取25.00mL溶液于锥形瓶,加入足量稀硫酸,用
产品配成100mL溶液,取25.00mL溶液于锥形瓶,加入足量稀硫酸,用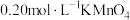 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液15.00mL。滴定的化学反应方程式
溶液15.00mL。滴定的化学反应方程式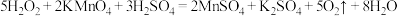 ,该过氧碳酸钠的产品纯度为
,该过氧碳酸钠的产品纯度为_______ 。
(7)为了探究过氧碳酸钠在溶液中的增氧机理,在相同时间测得体系的pH和溶解氧的含量如下表,结合以上数据分析“鱼浮灵”溶于水后在水产养殖中速效增氧的原理_______ 。
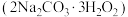 ,有
,有 和
和 的双重性质,50℃开始分解,在异丙醇中溶解度较低。实验室用
的双重性质,50℃开始分解,在异丙醇中溶解度较低。实验室用 与稳定剂的混合液(稳定剂不参与制备反应)和
与稳定剂的混合液(稳定剂不参与制备反应)和 化合制备过氧碳酸钠,制备装置如图。
化合制备过氧碳酸钠,制备装置如图。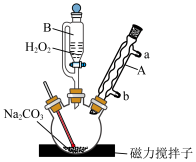
(2)烧瓶中发生主要反应的方程式为
(3)下列物质可做该反应的稳定剂的是_______。
A. | B. | C. | D. |
(4)实验时反应温度应控制在15~20℃,可采取的措施是
(5)反应结束后,为了获得干燥的过氧碳酸钠固体,可在反应液中加入适量的
(6)取4g过氧碳酸钠
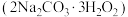 产品配成100mL溶液,取25.00mL溶液于锥形瓶,加入足量稀硫酸,用
产品配成100mL溶液,取25.00mL溶液于锥形瓶,加入足量稀硫酸,用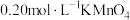 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液15.00mL。滴定的化学反应方程式
溶液15.00mL。滴定的化学反应方程式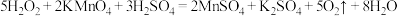 ,该过氧碳酸钠的产品纯度为
,该过氧碳酸钠的产品纯度为(7)为了探究过氧碳酸钠在溶液中的增氧机理,在相同时间测得体系的pH和溶解氧的含量如下表,结合以上数据分析“鱼浮灵”溶于水后在水产养殖中速效增氧的原理
| 试剂 |  |  | 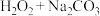 | 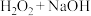 | 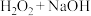 |
| pH | 6.0 | 15.97 | 8.14 | 8.15 | 9.26 |
| 溶解氧 | 6.44 | 6.48 | 9.11 | 9.12 | 10.97 |
您最近一年使用:0次
2022高三·全国·专题练习
5 . 研究小组以无水甲苯为溶剂,PCl5(易水解)和NaN3为反应物制备纳米球状红磷。该红磷可提高钠离子电池的性能。
(1)甲苯干燥和收集的回流装置如图1所示(夹持及加热装置略)。以二苯甲酮为指示剂,无水时体系呈蓝色。_____ 中。
②冷凝水的进口是______ (填“a”或“b”)。
③用Na干燥甲苯的原理是_____ (用化学方程式表示)。
④回流过程中,除水时打开的活塞是_____ ;体系变蓝后,改变开关状态收集甲苯。
(2)纳米球状红磷的制备装置如图2所示(搅拌和加热装置略)。_____ 。用Ar气赶走空气的目的是_____ 。
②经冷却、离心分离和洗涤得到产品,洗涤时先后使用乙醇和水,依次洗去的物质是_____ 和_____ 。
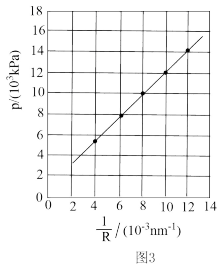
③所得纳米球状红磷的平均半径R与B装置中气体产物的压强p的关系如图3所示。欲控制合成R=125nm的红磷,气体产物的压强为_____ kPa,需NaN3的物质的量为______ mol(保留3位小数)。已知:p=a×n,其中a=2.5×105kPa•mol-1,n为气体产物的物质的量。
(1)甲苯干燥和收集的回流装置如图1所示(夹持及加热装置略)。以二苯甲酮为指示剂,无水时体系呈蓝色。

②冷凝水的进口是
③用Na干燥甲苯的原理是
④回流过程中,除水时打开的活塞是
(2)纳米球状红磷的制备装置如图2所示(搅拌和加热装置略)。
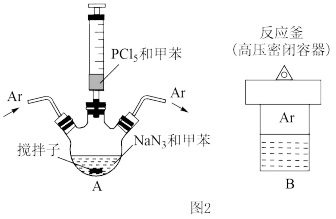
②经冷却、离心分离和洗涤得到产品,洗涤时先后使用乙醇和水,依次洗去的物质是
③所得纳米球状红磷的平均半径R与B装置中气体产物的压强p的关系如图3所示。欲控制合成R=125nm的红磷,气体产物的压强为
您最近一年使用:0次
2023-02-22更新
|
5588次组卷
|
10卷引用:2022年重庆高考真题化学试题
2022年重庆高考真题化学试题(已下线)2022年重庆高考真题化学试题变式题(实验探究题)重庆市第一中学校2023-2024学年高一下学期定时练习化学试题(已下线)专题16 化学实验综合题-2022年高考真题模拟题分项汇编(已下线)专题19 实验综合题(已下线)专题19 实验综合题(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)广东省佛山市第四中学2023-2024学年上学期高二开学考试化学试题(已下线)题型四 以无机物制备为载体的综合实验-备战2024年高考化学答题技巧与模板构建
名校
解题方法
6 . 已知钴在加热时易被氧化,CoCl2易潮解,实验室制备CoCl2的装置示意图如图所示(加热装置略):
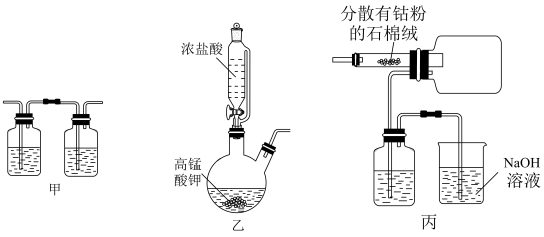
下列说法错误的是

下列说法错误的是
| A.装置乙中,盛装反应物原料的是滴液漏斗和双口烧瓶 |
| B.先加热装有石棉绒的硬质玻璃管,再滴加浓盐酸 |
| C.石棉绒的作用是增大反应接触面积 |
| D.3个洗气瓶中所盛装的试剂有2种 |
您最近一年使用:0次
名校
解题方法
7 . 下列实验操作中,装置选择不合理的是
| A | B | C | D |
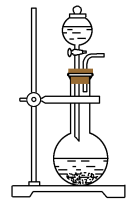 | 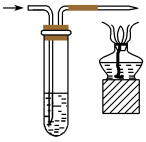 | 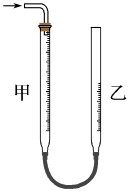 | 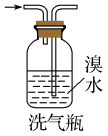 |
制备 | CO的尾气处理 | 测量H2的体积 | 除去 中的Cl2 中的Cl2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-12更新
|
305次组卷
|
2卷引用:重庆市南开中学2022-2023学年高一上期期末考试化学试题
名校
解题方法
8 . 下列图示实验(部分夹持装置省略)正确的是
| A | B | C | D |
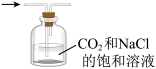 | 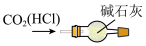 | 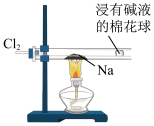 |  |
| 制备NaHCO3 | 除CO2中的HCl | 探究钠与Cl2反应 | 制备氢氧化亚铁 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 下列有关实验的操作以及描述,正确的是
A.检查装置气密性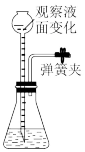 |
B.点燃酒精灯  |
C.制备氢气并检验H2的可燃性 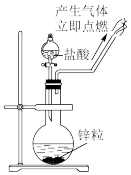 |
D.除去杂质气体CO2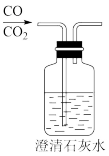 |
您最近一年使用:0次
解题方法
10 . 硫酸镁还原热解制备高纯氧化镁是一种新的探索,以解决氧化镁在医药、建筑等行业的应用广泛。现以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
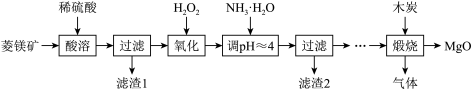
(1)酸溶所涉及反应的离子方程式为_________________________________________ 、_________________________________________________________ 。
(2)加入H2O2氧化的作用是_________________ ,滤渣2的成分是___________ (填化学式)。
(3)煅烧过程存在以下反应:
2MgSO4+C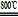 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+C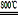 MgO+SO2↑+CO↑
MgO+SO2↑+CO↑
MgSO4+3C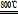 MgO+S↑+3CO↑
MgO+S↑+3CO↑
利用下图装置对煅烧产生的气体进行分步吸收或收集。
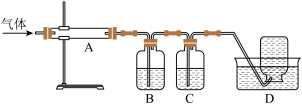
①B中盛放的溶液可以是______ (填字母)。
a.NaOH 溶液 b.Na2CO3溶液 c. KMnO4溶液 d. 稀硝酸
②C装置的作用是______________________ ,D中收集的气体可以是 _______ (填化学式)。
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:________________________________________________ 。

(1)酸溶所涉及反应的离子方程式为
(2)加入H2O2氧化的作用是
(3)煅烧过程存在以下反应:
2MgSO4+C
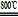 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑MgSO4+C
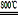 MgO+SO2↑+CO↑
MgO+SO2↑+CO↑MgSO4+3C
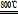 MgO+S↑+3CO↑
MgO+S↑+3CO↑利用下图装置对煅烧产生的气体进行分步吸收或收集。

①B中盛放的溶液可以是
a.NaOH 溶液 b.Na2CO3溶液 c. KMnO4溶液 d. 稀硝酸
②C装置的作用是
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:
您最近一年使用:0次



