1 . 下列实验操作能达到相应实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 向 (含少量 (含少量 杂质)的混合溶液中加入足量铁粉,待充分反应后过滤 杂质)的混合溶液中加入足量铁粉,待充分反应后过滤 | 提纯 |
| B | 向 溶液中通入过量的 溶液中通入过量的 气体,有白色沉淀生成 气体,有白色沉淀生成 | 验证元素非金属性:C>Si |
| C | 向稀的NaOH溶液中滴加 的饱和溶液 的饱和溶液 | 制备 胶体 胶体 |
| D | 向酸性 溶液中通入过量的 溶液中通入过量的 气体 气体 | 验证 具有漂白性 具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-05-26更新
|
290次组卷
|
2卷引用:重庆市巴蜀中学2022届高三适应性月考化学试题
2 . 下列实验设计思路正确的是
A.用湿润的pH试纸检验 是否为酸性气体 是否为酸性气体 |
| B.直接加热饱和氯化铁溶液制氢氧化铁胶体 |
| C.除去氨气中混有的氢气,将混合气体通过灼热的氧化铜 |
| D.检验铜和浓硫酸在加热条件下是否生成铜离子,往混合溶液中加入水,观察溶液颜色是否变蓝 |
您最近一年使用:0次
3 . 下列由实验得出的结论正确的是
| 实验 | 结论 | |
| A | 甲烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红 | 生成的有机物具有酸性 |
| B | 将乙烯通入溴的四氯化碳溶液,溶液最终变为无色透明 | 生成的 1,2-二溴乙烷无色、可溶于四氯化碳 |
| C | 乙烷中混有杂质乙烯,可将混合气体通入溴水溶液中,除去杂质乙烯 | 乙烯被溴水氧化 |
| D | 乙醇和水都可与金属钠反应产生可燃性气体 | 乙醇分子中的氢与水分子中的氢具有相同的活性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 下列除去杂质的方法中,正确的是
| 选项 | 物质(括号内为杂质) | 去除杂质的方法 |
| A | 粗盐( ) ) | 加入适量的KOH溶液、过滤 |
| B |  | 饱和 溶液、洗气 溶液、洗气 |
| C | 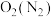 | 通过灼热的铜网 |
| D | NaCl固体( ) ) | 加热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . I.氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。
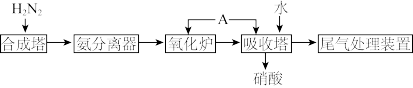
(1)写出氧化炉中的化学反应方程式_______ 。
(2)向吸收塔中通入A的作用_______ 。
(3)工业制硝酸的尾气是酸性气体,实验室模拟该流程时,为防止环境污染,最好选用_______ (填化学式)溶液吸收。
II.为除去KCl溶液中少量的Mg2+、 ,可选用Ba(OH)2、HCl和K2CO3三种溶液按如下步骤操作:
,可选用Ba(OH)2、HCl和K2CO3三种溶液按如下步骤操作:
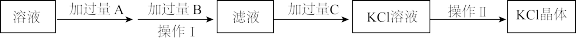
(4)上述试剂中,A是_______ ,C是_______ 。(填化学式)
(5)操作I的名称是_______ 。
(6)加过量A时发生有关反应的离子方程式为_______ 、_______ 。
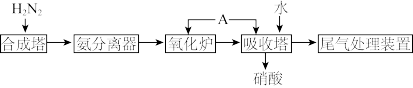
(1)写出氧化炉中的化学反应方程式
(2)向吸收塔中通入A的作用
(3)工业制硝酸的尾气是酸性气体,实验室模拟该流程时,为防止环境污染,最好选用
II.为除去KCl溶液中少量的Mg2+、
 ,可选用Ba(OH)2、HCl和K2CO3三种溶液按如下步骤操作:
,可选用Ba(OH)2、HCl和K2CO3三种溶液按如下步骤操作: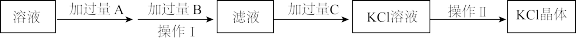
(4)上述试剂中,A是
(5)操作I的名称是
(6)加过量A时发生有关反应的离子方程式为
您最近一年使用:0次
名校
6 . 除去氯化钠溶液中混有的Ca2+、Mg2+、SO 等杂质离子,通常采用以下四种试剂:①Na2CO3 ②NaOH ③BaCl2 ④盐酸,加入试剂顺序合理的是
等杂质离子,通常采用以下四种试剂:①Na2CO3 ②NaOH ③BaCl2 ④盐酸,加入试剂顺序合理的是
 等杂质离子,通常采用以下四种试剂:①Na2CO3 ②NaOH ③BaCl2 ④盐酸,加入试剂顺序合理的是
等杂质离子,通常采用以下四种试剂:①Na2CO3 ②NaOH ③BaCl2 ④盐酸,加入试剂顺序合理的是| A.③②①④ | B.①③②④ | C.④②①③ | D.①②③④ |
您最近一年使用:0次
2022-04-07更新
|
115次组卷
|
2卷引用:重庆市长寿中学校2021-2022学年高一下学期阶段性考试(一)化学试题
名校
解题方法
7 . 重钢集团含钛高炉渣(主要成分为 ,还含有少量
,还含有少量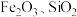 )可以用于生产
)可以用于生产 ,其工艺流程有如下两种:
,其工艺流程有如下两种:
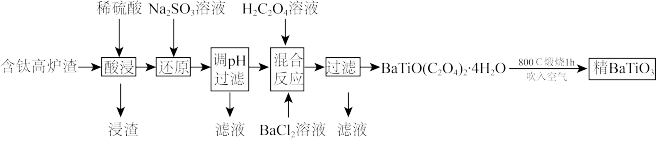
流程Ⅰ:
已知:a.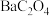 难溶于水,能溶于强酸;
难溶于水,能溶于强酸;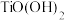 难溶于水,具有两性,溶于草酸生成
难溶于水,具有两性,溶于草酸生成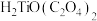 ;
;
b.相关离子[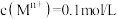 ]形成氢氧化物沉淀的
]形成氢氧化物沉淀的 范围如下表:
范围如下表:
(1)“浸渣”的成分主要是_______ 。
(2)“酸浸”后 以
以 形式存在,该反应的离子方程式为
形式存在,该反应的离子方程式为_______ 。
(3)“还原”的最终目的是_______ 。
(4)“混合反应”时,试剂添加顺序合理的是_______ (填序号)。
A.先加入过量 溶液,再加入适量
溶液,再加入适量 溶液
溶液
B.先加入过量 溶液,再加入适量
溶液,再加入适量 溶液
溶液
C.先按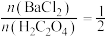 混合后,再加入反应体系中
混合后,再加入反应体系中
流程Ⅱ:
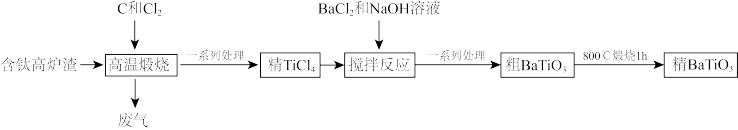
(5)实验测得,粗 的纯度为
的纯度为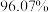 ,其中含
,其中含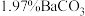 、
、 杂质,煅烧
杂质,煅烧 后,最终产品的产率和纯度(仅含微量
后,最终产品的产率和纯度(仅含微量 杂质)均明显提高。试回答下列问题:
杂质)均明显提高。试回答下列问题:
①用化学方程式解释“800℃煅烧”时产率提高的原因:_______ 。
②最终产品的纯度为_______ %(保留1位小数)。
(6)流程Ⅰ_______ (填“优于”或“劣于”)流程Ⅱ,理由是_______ 。
 ,还含有少量
,还含有少量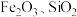 )可以用于生产
)可以用于生产 ,其工艺流程有如下两种:
,其工艺流程有如下两种:流程Ⅰ:

已知:a.
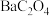 难溶于水,能溶于强酸;
难溶于水,能溶于强酸;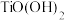 难溶于水,具有两性,溶于草酸生成
难溶于水,具有两性,溶于草酸生成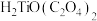 ;
;b.相关离子[
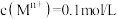 ]形成氢氧化物沉淀的
]形成氢氧化物沉淀的 范围如下表:
范围如下表:| 离子 |  |  |  |
开始沉淀的 | 0.5 | 6.3 | 1.5 |
完全沉淀的 | 2.5 | 8.3 | 2.8 |
(1)“浸渣”的成分主要是
(2)“酸浸”后
 以
以 形式存在,该反应的离子方程式为
形式存在,该反应的离子方程式为(3)“还原”的最终目的是
(4)“混合反应”时,试剂添加顺序合理的是
A.先加入过量
 溶液,再加入适量
溶液,再加入适量 溶液
溶液B.先加入过量
 溶液,再加入适量
溶液,再加入适量 溶液
溶液C.先按
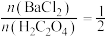 混合后,再加入反应体系中
混合后,再加入反应体系中流程Ⅱ:

(5)实验测得,粗
 的纯度为
的纯度为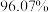 ,其中含
,其中含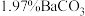 、
、 杂质,煅烧
杂质,煅烧 后,最终产品的产率和纯度(仅含微量
后,最终产品的产率和纯度(仅含微量 杂质)均明显提高。试回答下列问题:
杂质)均明显提高。试回答下列问题:①用化学方程式解释“800℃煅烧”时产率提高的原因:
②最终产品的纯度为
(6)流程Ⅰ
您最近一年使用:0次
名校
8 . 下列实验操作能达到对应目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 将 通入漂白粉溶液中 通入漂白粉溶液中 | 证明 的酸性强于 的酸性强于 |
| B | 向混合溶液加入氢氧化钠,反应后静置、分液 | 除去溴苯中混有的 |
| C | 向 溶液中滴加酸性高锰酸钾溶液 溶液中滴加酸性高锰酸钾溶液 | 证明 的氧化性强于 的氧化性强于 |
| D | 将表面打磨过的铝片迅速投入正在沸腾的水中 | 验证 是否和沸水发生反应 是否和沸水发生反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 实验室一般用苯和液溴在溴化铁的催化作用下制备溴苯。某兴趣小组设计了如下流程提纯制得的粗溴苯。下列说法错误的是
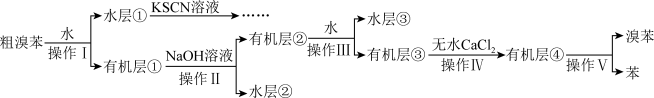
| A.操作Ⅰ、Ⅱ、Ⅲ用到的主要玻璃仪器是分液漏斗 |
| B.操作Ⅳ、操作Ⅴ分别是过滤和蒸馏 |
| C.加入NaOH溶液的目的是除去有机层①中的单质溴 |
| D.水层①中加入KSCN溶液后显红色,说明溴化铁已完全被除尽 |
您最近一年使用:0次
2022-04-03更新
|
554次组卷
|
13卷引用:重庆市第六十六中学2020-2021学年高二下学期第二次月考化学试题
重庆市第六十六中学2020-2021学年高二下学期第二次月考化学试题湖北省巴东县第一高级中学2020-2021学年高二下学期第一次月考化学试题黑龙江省大庆市实验中学2021-2022学年高二4月月考化学试题河北省武安市第一中学2021-2022学年高三上学期第五次调研考试化学试题黑龙江省勃利县高级中学2022-2023学年高二下学期5月月考化学试题河北省衡水第一中学2021届高三第二次联合考试化学试题山东师范大学附属中学2020-2021学年高二下学期期中学分认定考试化学试题河北省秦皇岛市青龙一中2021届高三高考适应性考试化学试题河北省石家庄市第二中学2021-2022学年高三上学期10月第二次考试化学试题广东省广州市第五中学2020-2021学年高二下学期期末考试化学试题黑龙江省大庆铁人中学2021-2022学年高二下学期开学考试化学试题黑龙江省哈尔滨市德强高中2021-2022学年高二下学期期中考试化学试题湖北省枣阳市第一中学2022届高三下学期5月第三次模拟考试化学试题
名校
10 . I.已知 和
和 两支试管所盛的溶液中共含有
两支试管所盛的溶液中共含有 、
、 、
、 、
、 、
、 、
、 六种离子,向试管
六种离子,向试管 的溶液中滴入酚酞试液呈粉红色。请回答下列问题:
的溶液中滴入酚酞试液呈粉红色。请回答下列问题:
(1)试管 的溶液中所含的上述离子有
的溶液中所含的上述离子有___________ 。
(2)若将试管 和试管
和试管 中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为
中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为___________ 、___________ 。(不考虑氢氧化银的存在)
(3)若向由试管 溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量
溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量 溶液,则发生反应的离子方程式为
溶液,则发生反应的离子方程式为___________ 。
II.为除去粗盐中的 、
、 、
、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
称取粗盐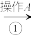
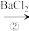
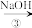
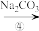
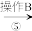 滤液
滤液
 精盐
精盐
(4)第①步中,操作 是
是___________ ,第⑤步中,操作
___________ ;
(5)第④步中,写出相应的离子方程式(设粗盐溶液中 的主要存在形式为CaCl2)
的主要存在形式为CaCl2)___________ ,___________ ;
(6)若先用盐酸调 再过滤,将对实验结果产生影响,其原因是
再过滤,将对实验结果产生影响,其原因是___________ 。
 和
和 两支试管所盛的溶液中共含有
两支试管所盛的溶液中共含有 、
、 、
、 、
、 、
、 、
、 六种离子,向试管
六种离子,向试管 的溶液中滴入酚酞试液呈粉红色。请回答下列问题:
的溶液中滴入酚酞试液呈粉红色。请回答下列问题:(1)试管
 的溶液中所含的上述离子有
的溶液中所含的上述离子有(2)若将试管
 和试管
和试管 中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为
中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为(3)若向由试管
 溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量
溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量 溶液,则发生反应的离子方程式为
溶液,则发生反应的离子方程式为II.为除去粗盐中的
 、
、 、
、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):称取粗盐
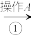
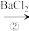
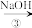
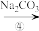
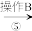 滤液
滤液
 精盐
精盐(4)第①步中,操作
 是
是
(5)第④步中,写出相应的离子方程式(设粗盐溶液中
 的主要存在形式为CaCl2)
的主要存在形式为CaCl2)(6)若先用盐酸调
 再过滤,将对实验结果产生影响,其原因是
再过滤,将对实验结果产生影响,其原因是
您最近一年使用:0次
2022-03-27更新
|
210次组卷
|
2卷引用:重庆市第七中学校2021-2022学年高一下学期3月月考化学试题



