1 . 钨是国防及高新技术应用中极为重要的功能材料之一,由黑钨矿[主要成分是钨酸亚铁( )、钨酸锰(
)、钨酸锰( ),以及少量的Si、As元素]冶炼钨的流程如下:
),以及少量的Si、As元素]冶炼钨的流程如下:
①钨酸( )酸性很弱,难溶于水。
)酸性很弱,难溶于水。
②水浸液中含有 、
、 、
、 、
、 等阴离子。
等阴离子。
回答下列问题:
(1)“焙烧”前,需将黑钨矿粉碎,目的是_______ 。
(2)“焙烧”过程中,生成 的化学方程式为
的化学方程式为_______ 。
(3)“净化”过程中, 的作用是
的作用是_______ 。
(4)“酸化”过程中,发生反应的离子方程式为_______ 。
(5)“高温还原”过程中,被还原的物质与被氧化的物质的物质的量之比为_______ 。
(6)硬质合金刀具中含碳化钨(WC,碳元素为-4价),利用电解法可以从碳化钨废料中回收钨。电解时,用碳化钨做阳极,不锈钢做阴极,HCl溶液为电解液,阳极析出钨酸沉淀并放出 气体,则阳极的电极反应式为
气体,则阳极的电极反应式为_______ 。
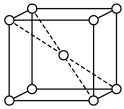
(7)钨晶胞为体心立方晶胞,晶胞结构如图所示(注:晶胞体对角线的W原子相切),则钨晶胞的原子空间利用率为_______(填标号。晶胞的原子空间利用率=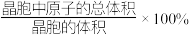 )。
)。
 )、钨酸锰(
)、钨酸锰( ),以及少量的Si、As元素]冶炼钨的流程如下:
),以及少量的Si、As元素]冶炼钨的流程如下:
①钨酸(
 )酸性很弱,难溶于水。
)酸性很弱,难溶于水。②水浸液中含有
 、
、 、
、 、
、 等阴离子。
等阴离子。回答下列问题:
(1)“焙烧”前,需将黑钨矿粉碎,目的是
(2)“焙烧”过程中,生成
 的化学方程式为
的化学方程式为(3)“净化”过程中,
 的作用是
的作用是(4)“酸化”过程中,发生反应的离子方程式为
(5)“高温还原”过程中,被还原的物质与被氧化的物质的物质的量之比为
(6)硬质合金刀具中含碳化钨(WC,碳元素为-4价),利用电解法可以从碳化钨废料中回收钨。电解时,用碳化钨做阳极,不锈钢做阴极,HCl溶液为电解液,阳极析出钨酸沉淀并放出
 气体,则阳极的电极反应式为
气体,则阳极的电极反应式为(7)钨晶胞为体心立方晶胞,晶胞结构如图所示(注:晶胞体对角线的W原子相切),则钨晶胞的原子空间利用率为_______(填标号。晶胞的原子空间利用率=
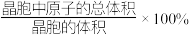 )。
)。
A. | B.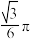 | C. | D. |
您最近一年使用:0次
2 . 钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及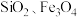 。采用以下工艺流程可由黏土矿制备
。采用以下工艺流程可由黏土矿制备 。
。
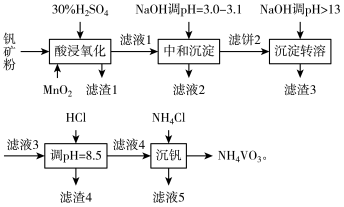
该工艺条件下,溶液中金属离子开始和完全沉淀的pH值如下表所示:
回答下列问题:
(1)“酸浸氧化”时需要加热,其目的是___________ 。
(2)“酸浸氧化”中,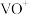 和
和 均被氧化成
均被氧化成 ,同时还有
,同时还有___________ 离子被氧化。写出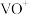 被氧化成
被氧化成 反应的离子方程式
反应的离子方程式___________ 。
(3)“中和沉淀”中,钒水解并沉淀为 。随滤液2可除去金属离子
。随滤液2可除去金属离子 和
和___________ ,以及部分的___________ 。
(4)“沉淀转溶”中, 转化为钒酸盐溶解。滤渣3的主要成分是
转化为钒酸盐溶解。滤渣3的主要成分是___________ 。
(5)用HCl“调 ”时有沉淀生成,生成该滤渣4反应的化学方程式为
”时有沉淀生成,生成该滤渣4反应的化学方程式为___________ 。
(6)“沉钒”反应的离子方程式为___________ 。
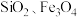 。采用以下工艺流程可由黏土矿制备
。采用以下工艺流程可由黏土矿制备 。
。
该工艺条件下,溶液中金属离子开始和完全沉淀的pH值如下表所示:
| 金属离子 |  |  |  |  |
| 开始沉淀的pH值 | 1.9 | 7.0 | 3.0 | 8.1 |
| 完全沉淀的pH值 | 3.2 | 9.0 | 4.7 | 10.1 |
回答下列问题:
(1)“酸浸氧化”时需要加热,其目的是
(2)“酸浸氧化”中,
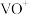 和
和 均被氧化成
均被氧化成 ,同时还有
,同时还有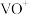 被氧化成
被氧化成 反应的离子方程式
反应的离子方程式(3)“中和沉淀”中,钒水解并沉淀为
 。随滤液2可除去金属离子
。随滤液2可除去金属离子 和
和(4)“沉淀转溶”中,
 转化为钒酸盐溶解。滤渣3的主要成分是
转化为钒酸盐溶解。滤渣3的主要成分是(5)用HCl“调
 ”时有沉淀生成,生成该滤渣4反应的化学方程式为
”时有沉淀生成,生成该滤渣4反应的化学方程式为(6)“沉钒”反应的离子方程式为
您最近一年使用:0次
名校
解题方法
3 . 以红土镍矿(主要含有Fe2O3、FeO、NiO、SiO2等)为原料,获取净水剂黄钠铁矾[NaFe3(SO4)2(OH)6]和纳米镍粉的部分工艺流程如图:
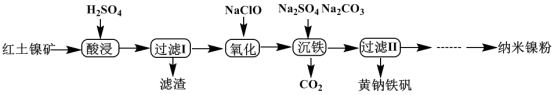
已知:Fe3+在pH约为3.7时可完全转化为Fe(OH)3,Fe2+在pH约为9时可完全转化为Fe(OH)2
下列说法错误的是

已知:Fe3+在pH约为3.7时可完全转化为Fe(OH)3,Fe2+在pH约为9时可完全转化为Fe(OH)2
下列说法错误的是
| A.“滤渣”的主要成分是SiO2 |
| B.为提高镍、铁元素的利用率,可将“过滤I”的滤液和滤渣洗涤液合并 |
| C.“氧化”过程发生的离子方程式为2H++2Fe2++ClO-=2Fe3++Cl-+H2O |
| D.“沉铁”过程中加入碳酸钠的作用是调节溶液的酸碱度,应将pH控制在3.7~9 |
您最近一年使用:0次
2021-03-18更新
|
1179次组卷
|
6卷引用:广西河池市高级中学2021-2022学年高三上学期第二次月考化学试题
广西河池市高级中学2021-2022学年高三上学期第二次月考化学试题湖北省八市2021届高三下学期(3月)联考化学试题(已下线)押山东卷第09题 化工生产流程选择题-备战2021年高考化学临考题号押题(山东卷)(已下线)考向06 钠及其重要化合物-备战2022年高考化学一轮复习考点微专题湖南省郴州市永兴县第一中学2021-2022学年高三下学期期中考试化学试题安徽省蚌埠第三中学2021-2022学年高二下学期开学测试化学试题
解题方法
4 . CoC2O4是制备氧化钴和金属钴的原料。一种利用含钴废料(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、CaO、MgO、碳及有机物等)制取CoC2O4的工艺流程如下:
(1)为了加快“碱浸”速率,可采用的方法有______ (写两种)。反应的主要化学方程式为______ 。
(2)“钴浸出”过程中加入Na2SO3的作用是______ 。
(3)“除杂1”过程中,在40~50℃加入H2O2,写出加入H2O2反应的主要离子方程式:______ 。
(4)“除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+ )=1.0×10-5mol/L,则滤液中c(Mg2+ )为______ [已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10]。
(5)萃取剂对金属离子的萃取率与pH的关系如图所示,经过萃取可除去Mn2+,则控制溶液的pH范围是______ (填字母)。

A.1.0~2.0 B.2.0~3.0 C.3.0~3.5

(1)为了加快“碱浸”速率,可采用的方法有
(2)“钴浸出”过程中加入Na2SO3的作用是
(3)“除杂1”过程中,在40~50℃加入H2O2,写出加入H2O2反应的主要离子方程式:
(4)“除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+ )=1.0×10-5mol/L,则滤液中c(Mg2+ )为
(5)萃取剂对金属离子的萃取率与pH的关系如图所示,经过萃取可除去Mn2+,则控制溶液的pH范围是

A.1.0~2.0 B.2.0~3.0 C.3.0~3.5
您最近一年使用:0次
解题方法
5 . 工业上以软锰矿(主要成分是MnO2,还含有少量SiO2、Fe2O3)为主要原料制备高性能的磁性材料碳酸锰(MnCO3)。其工业流程如图所示,下列说法错误的是


| A.滤渣I可用于制造光导纤维、滤渣II可用于制作颜料 |
| B.“浸锰”过程MnO2参与反应的化学方程式为MnO2十SO2=MnSO4 |
| C.“沉锰”时,反应体系的温度越高,越有利于生成MnCO3 |
| D.检验高纯碳酸锰是否洗涤干净,可选用BaCl2溶液和盐酸试剂 |
您最近一年使用:0次
名校
解题方法
6 . 钴(Co)及其化合物在工业上广泛应用于磁性材料、电池材料及超硬材料等领域。某学习小组欲从某工业废料中回收钴,设计工艺流程如下:(废料中含有Al、Co2O3和Fe2O3等物质)。
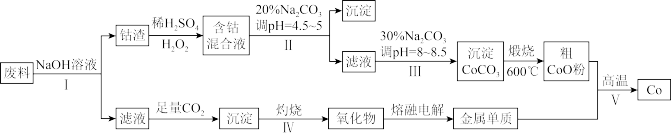
请回答:
(1)废料用NaOH溶液处理前通常先将废料粉碎,其目的是____________ 。
(2)过程Ⅱ用稀H2SO4和H2O2溶液与Co2O3反应而达到浸出钴的目的,请写出该反应的离子方程式___________ 。在实验室模拟工业生产时,也可用盐酸浸出钴,但实际工业生产中不用盐酸,请分析不用盐酸浸出钴的主要原因______________ 。
(3)碳酸钠溶液在过程Ⅱ和Ⅲ中所起作用有所不同,请写出碳酸钠在过程Ⅱ中发生反应生成沉淀的离子方程式__________________________________ 。
(4) 若在实验室中完成过程Ⅳ,则沉淀物需在__________________ (填仪器名称)中灼烧;写出在过程Ⅴ中发生反应的化学方程式__________________________________ 。
(5)将1.0×10-3 mol/LCoSO4与1.2×10-3mol/L的Na2CO3等体积混合,此时溶液中的Co2+的浓度为__________ mol/L。(已知:CoCO3的溶度积为:Ksp=1.0×10-13)
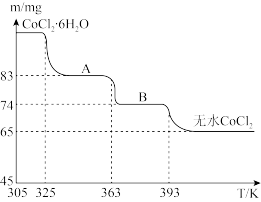
(6)CoO与盐酸反应可得粉红色的CoCl2溶液。CoCl2晶体因结晶水数目不同而呈现不同颜色,利用蓝色的无水CoCl2吸水变色这一性质可制成变色水泥和显隐墨水。如图是粉红色的CoCl2·6H2O晶体在烘箱中受热分解时,剩余固体质量随温度变化的曲线,物质A的化学式是____________________ 。

请回答:
(1)废料用NaOH溶液处理前通常先将废料粉碎,其目的是
(2)过程Ⅱ用稀H2SO4和H2O2溶液与Co2O3反应而达到浸出钴的目的,请写出该反应的离子方程式
(3)碳酸钠溶液在过程Ⅱ和Ⅲ中所起作用有所不同,请写出碳酸钠在过程Ⅱ中发生反应生成沉淀的离子方程式
(4) 若在实验室中完成过程Ⅳ,则沉淀物需在
(5)将1.0×10-3 mol/LCoSO4与1.2×10-3mol/L的Na2CO3等体积混合,此时溶液中的Co2+的浓度为
(6)CoO与盐酸反应可得粉红色的CoCl2溶液。CoCl2晶体因结晶水数目不同而呈现不同颜色,利用蓝色的无水CoCl2吸水变色这一性质可制成变色水泥和显隐墨水。如图是粉红色的CoCl2·6H2O晶体在烘箱中受热分解时,剩余固体质量随温度变化的曲线,物质A的化学式是

您最近一年使用:0次
2019-12-05更新
|
342次组卷
|
4卷引用:广西河池高级中学2022届高三下学期4月考试理科综合化学试题
广西河池高级中学2022届高三下学期4月考试理科综合化学试题湖北省示范高中2019~2020学年高三11月月考理综化学试题(已下线)考点17 化工生产诸要素及流程图分析-2020年高考化学命题预测与模拟试题分类精编陕西省西安市长安区第一中学2022-2023学年高三上学期第二次质量检测化学试题
解题方法
7 . 苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:

制备苯乙酸的装置示意图如右(加热和夹持装置等略):
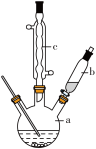
已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是____________________ 。
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130 ℃继续反应。在装置中,仪器c的作用是____________________ ;仪器b的名称是____________________ ,其作用是____________________ 。反应结束后加适量冷水,再分离出苯乙酸粗品。加入冷水的目的是____________________ 。下列仪器中可用于分离苯乙酸粗品的是(填标号)。____________________
A 分液漏斗 B 漏斗 C 烧杯 D 直形冷凝管 E 玻璃棒
(3)提纯粗苯乙酸的方法是____________________ ,最终得到44g纯品,则苯乙酸的产率是____________________ 。
(4)用CuCl2•2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是____________________ 。
(5)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是____________________ 。
(6)在实际操作时,发现b中液体不容易滴下来,你认为应将b改为____________________ (填仪器名称)即可解决此问题。

制备苯乙酸的装置示意图如右(加热和夹持装置等略):

已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130 ℃继续反应。在装置中,仪器c的作用是
A 分液漏斗 B 漏斗 C 烧杯 D 直形冷凝管 E 玻璃棒
(3)提纯粗苯乙酸的方法是
(4)用CuCl2•2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是
(5)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是
(6)在实际操作时,发现b中液体不容易滴下来,你认为应将b改为
您最近一年使用:0次
名校
8 . 某化工厂为了综合利用生产过程中的副产品CaSO4,与相邻的合成氨厂联合设计了以下制备(NH4)22SO4的工艺流程:

请回答以下问题:
(1)工业合成氨反应的条件是_____________________ 。沉淀池中发生的主要反应方程式是________________________ 。该反应能够发生的原因是__________________________ 。
(2)提纯滤液以获得(NH4)2SO4晶体,必要的操作步骤是:__________ (填序号)。
A.萃取 B.蒸发浓缩 C.冷却结晶 D.蒸馏
(3)上述生产流程中,有关NH3的作用及说明正确的是:__________ (填序号)。
A.提供制备所需的氮元素
B.增大CO32-的浓度促进反应发生
C.作反应的催化剂
D.生产1 mol (NH4)2SO4,至少消耗2 mol NH3
(4)该生产过程中的副产品是_______________ ,从绿色化学和资源综合利用的角度说明上述流程的主要优点是______________ .缺点是_____________ 。

请回答以下问题:
(1)工业合成氨反应的条件是
(2)提纯滤液以获得(NH4)2SO4晶体,必要的操作步骤是:
A.萃取 B.蒸发浓缩 C.冷却结晶 D.蒸馏
(3)上述生产流程中,有关NH3的作用及说明正确的是:
A.提供制备所需的氮元素
B.增大CO32-的浓度促进反应发生
C.作反应的催化剂
D.生产1 mol (NH4)2SO4,至少消耗2 mol NH3
(4)该生产过程中的副产品是
您最近一年使用:0次



